常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-19 09:00:00 细胞资源库平台 访问量:121
荧光素酶报告基因系统是一种基于荧光素酶催化底物氧化反应产生生物发光的检测技术,广泛应用于细胞生物学研究。其中,萤火虫荧光素酶(firefly luciferase, Fluc)因其高灵敏度、宽线性检测范围(约7~8个数量级)以及较短的半衰期(在哺乳动物细胞中约为3小时,在植物细胞中约为3.5小时)而成为最常用的报告基因。其发光信号强度在酶浓度为10⁻¹⁶ mol/L至10⁻⁸ mol/L的范围内与酶活性呈线性关系,并且在理想条件下可检测到低至10⁻²⁰ mol/L的荧光素酶活性。此外,荧光素酶报告基因系统具有非放射性、检测快速、灵敏度高(比氯霉素乙酰转移酶CAT高100倍)等优点,特别适用于高通量筛选和活细胞检测。通过将荧光素酶报告基因载体转染至宿主细胞后,可利用荧光素酶检测系统灵敏且便捷地监测基因表达水平,已成为细胞生物学研究中的重要工具。逸漠生物自主研发了近200种表达Fluc的细胞系,均经过荧光素酶活性检测验证,可满足科研人员的多样化需求,欢迎咨询。
英文标题:Lighting up PNETs: Creating Murine Models with a Novel Bioluminescent Cell Line
中文标题:点亮胰腺神经内分泌肿瘤:利用新型生物发光细胞系构建小鼠模型
发表期刊:《ONCOLOGY LETTERS》
影响因子:3.5
作者单位:
1.Department of Surgery, Cooper University Health Care, Camden, NJ;
2.Department of Pathology, Cooper University Health Care, Camden, NJ;
3.Department of Surgery, Rowan University School of Medicine, Camden, NJ;
4.Camden Cancer Research Center, Camden, NJ;
5.MD Anderson Cancer Center at Cooper, Camden, NJ
作者信息:
Matthew C. Moccia, Rachel Nation
胰腺神经内分泌肿瘤(PNETs)是一种罕见恶性肿瘤,除手术外晚期治疗手段有限,其显著的生物学异质性由肿瘤进展过程中复杂分子信号通路失调驱动,目前领域内缺乏能方便实时监测肿瘤进展和追踪单个肿瘤细胞、兼具生物学相关性与成本效益的临床前模型;同时现有 PNET 治疗因肿瘤分子异质性和内在复杂性存在诸多障碍,常用的细胞系来源异种移植(CDX)模型临床相关性有限,PNET 特异性异种移植模型的建立还因肿瘤低发病率、惰性生长及异质性面临细胞系稀缺、无创实时追踪困难等问题,而 STC-1 肠内分泌肿瘤细胞系与人类 PNET 细胞具有关键形态和功能特征,为构建相关模型提供了基础,因此本研究旨在开发基于该细胞系的可生物发光和荧光追踪的 PNET 模型。
本研究首先构建稳定共表达萤火虫荧光素酶(F-Luc)和增强型绿色荧光蛋白(EGFP)的 STC-1 小鼠细胞系,通过慢病毒转导结合嘌呤霉素筛选和荧光激活细胞分选(FACS)纯化获得双标记细胞;随后将 1×10⁶个双标记细胞与基质胶混合,以皮下、肾被膜、胰腺原位三种注射方式植入免疫缺陷 Nu/J 小鼠体内,设胰腺注射基质胶和 PBS 的对照组,严格遵循动物实验伦理规范饲养监测小鼠;接着利用活体生物发光成像系统(IVIS)每周监测肿瘤生长至 6 周,通过荧光素底物注射、划定感兴趣区域量化肿瘤负荷;实验结束后收集肿瘤和远端器官,进行苏木精 - 伊红(H&E)染色、免疫组化(IHC)和共免疫荧光分析,检测 Ki-67、突触素等神经内分泌标志物及 EGFP 表达,并以人类高分化 PNET 组织为参照,用 ImageJ 量化染色密度和强度;最后采用 GraphPad Prism 10 的方差分析(ANOVA)进行组间统计比较,p<0.05 为差异有统计学意义。
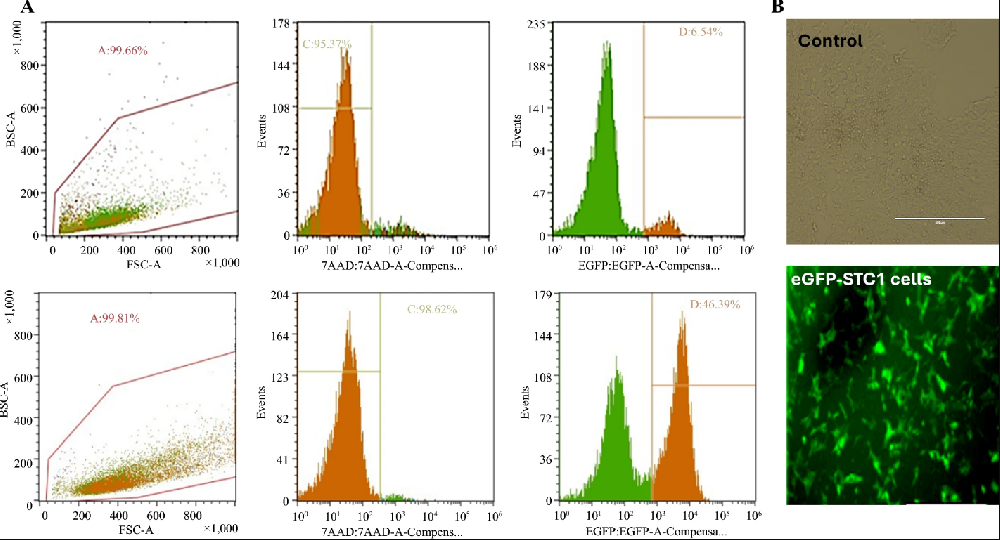
图1:增强型绿色荧光蛋白(EGFP)转导效率及体内肿瘤成像表征
该图通过流式细胞术和显微镜观察验证 STC-1 细胞的转导效果,流式结果显示对照组 EGFP 阳性细胞仅 6.54%,实验组达 46.39% 且细胞存活率超 95%,相差显微镜与荧光显微镜对比可见转导后细胞呈现强烈绿色荧光,未转导细胞无荧光信号;同时转导后的 STC-1 细胞能稳定表达转基因超过 6 个月,细胞形态和生长特性未发生显著改变,证明慢病毒转导成功且未对细胞生物学特性产生不利影响。
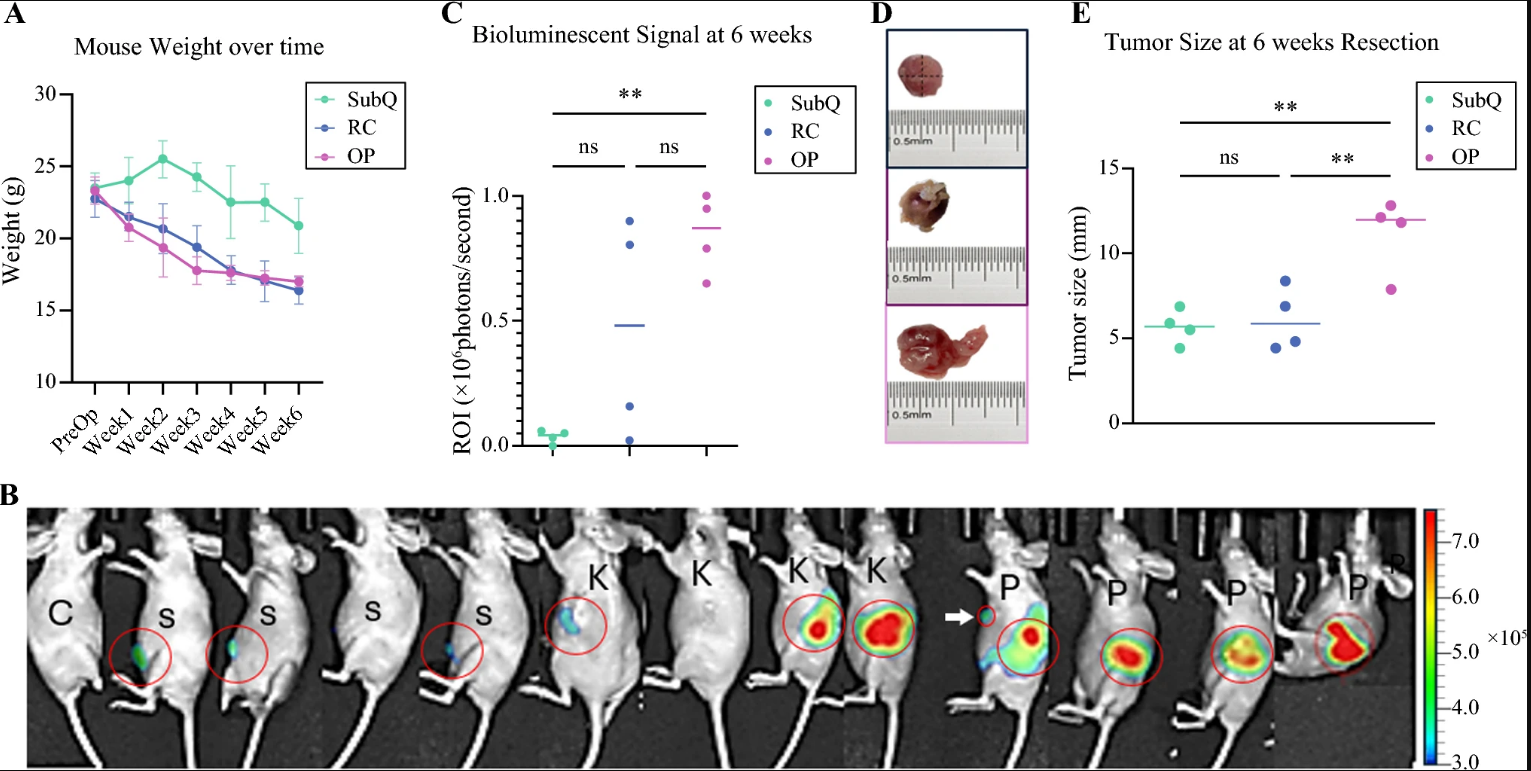
图2:皮下 - 肾 - 胰腺模型的肿瘤生长及小鼠体重动态变化
该图显示实验期间三组模型小鼠均出现体重下降,其中肾被膜(RC)和胰腺原位(OP)模型小鼠体重下降程度显著高于皮下(SubQ)模型,且 OP 模型从术后 2 周开始即出现显著体重下降,提示其肿瘤负荷对小鼠生理影响更显著;6 周时生物发光成像显示三组均有可检测的信号,且 OP 模型有一只小鼠出现转移播散,OP 模型感兴趣区域的生物发光信号显著高于 SubQ 模型;离体肿瘤大小测量显示,SubQ 和 RC 模型肿瘤平均直径分别为 5.78mm、6.23mm,OP 模型达 11.33mm,显著大于前两者,生物发光信号与肿瘤实际大小结果一致,验证了生物发光成像作为肿瘤进展可靠指标的有效性。
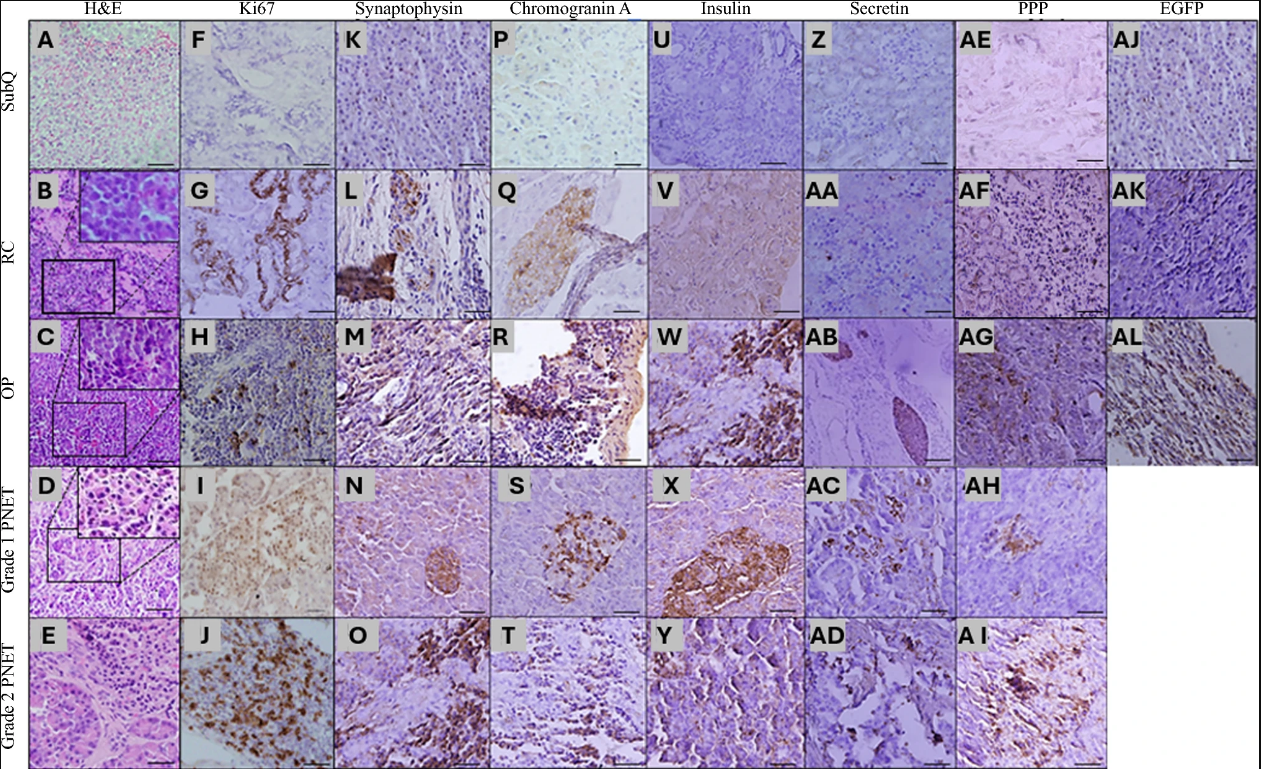
图3:小鼠胰腺神经内分泌肿瘤异种移植模型的组织学和免疫组化分析
该图以人类 1、2 级 PNET 为参照,对三组模型肿瘤进行 H&E 染色和 Ki-67、突触素、嗜铬粒蛋白 A 等标志物及 EGFP 的免疫组化检测,结果显示 RC 和 OP 模型肿瘤的形态学特征符合人类 1 级 PNET;免疫组化染色可见 OP 模型在各神经内分泌标志物表达上均呈现出更显著的阳性信号,EGFP 染色也能在三组模型肿瘤中识别出植入的 STC-1 细胞,而 SubQ 模型的标志物阳性信号较弱,直观体现了不同移植部位肿瘤的组织学和分子表型差异。
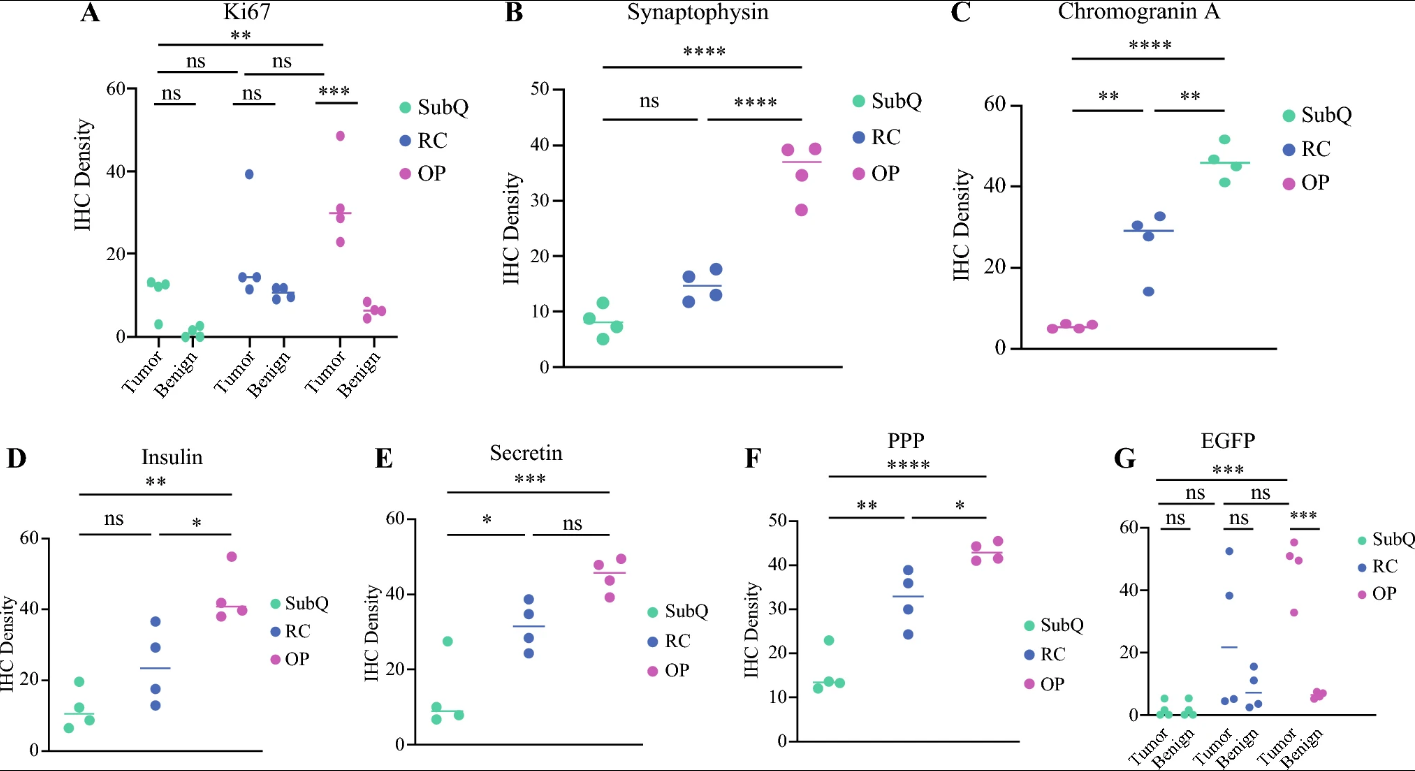
图4:不同肿瘤模型间免疫组化(IHC)标志物密度比较
该图通过定量分析三组模型肿瘤的 IHC 标志物密度,发现 OP 模型的 Ki-67 增殖指数显著高于 SubQ 模型,且与邻近正常组织相比差异有统计学意义,符合人类 1 级 PNET 的 Ki-67 表达特征;OP 模型的突触素、嗜铬粒蛋白 A、胰岛素、胰多肽等神经内分泌标志物密度均显著高于 SubQ 和 RC 模型,分泌素表达显著高于 SubQ 模型,与 RC 模型无显著差异;同时 OP 模型的 EGFP 阳性细胞密度显著高于 SubQ 模型和邻近正常组织,而 SubQ 和 RC 模型的肿瘤与邻近正常组织 EGFP 表达无显著差异,量化证实了 OP 模型肿瘤的神经内分泌分化程度和 STC-1 细胞植活效率更高。
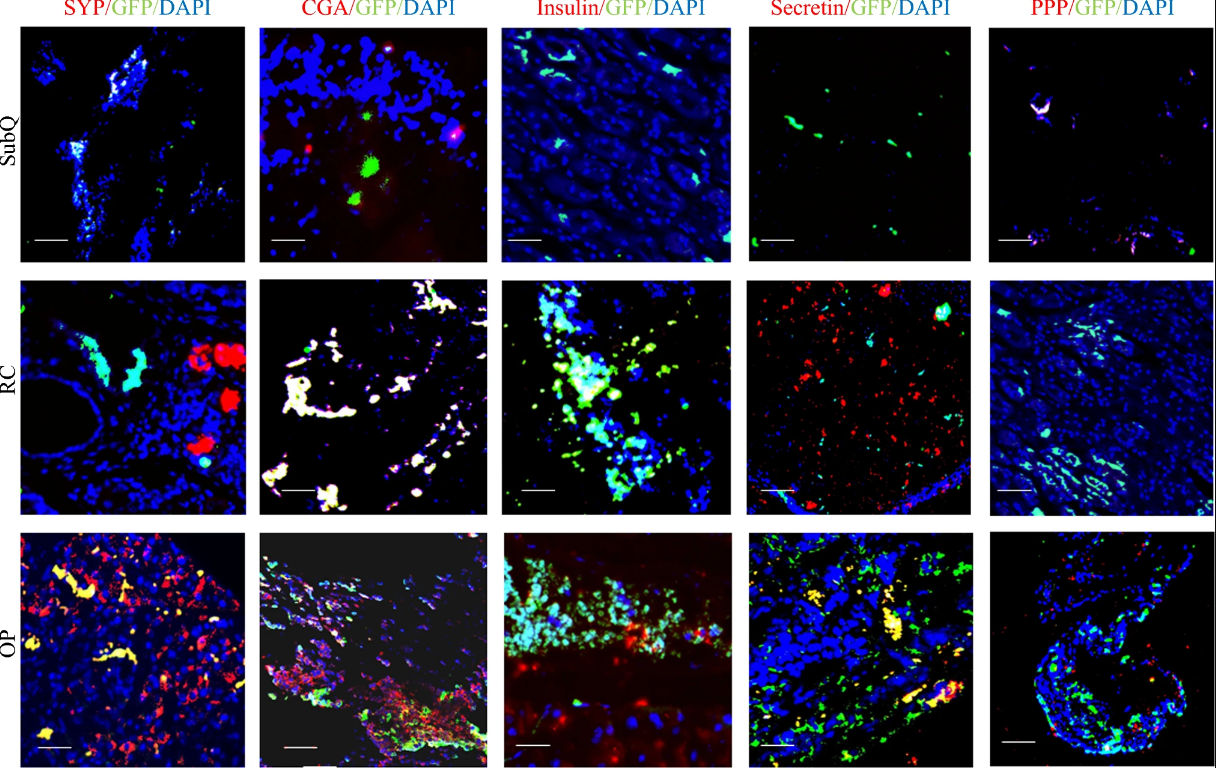
图5:小鼠胰腺神经内分泌肿瘤模型中神经内分泌标志物的共免疫荧光分析
该图通过突触素、嗜铬粒蛋白 A 等神经内分泌标志物(红色)、EGFP(绿色)和 DAPI 核染色(蓝色)的共免疫荧光染色,观察标志物与 EGFP 的共定位情况,黄色和白色区域为显著共定位部位;结果显示 OP 模型中 EGFP 阳性细胞与各神经内分泌标志物的共定位程度显著高于 SubQ 和 RC 模型,RC 模型与 SubQ 模型相比也有一定程度的共定位提升,直观反映了不同移植微环境对 STC-1 细胞神经内分泌分化的影响,且胰岛素与 EGFP 的共定位在各模型中均较少。
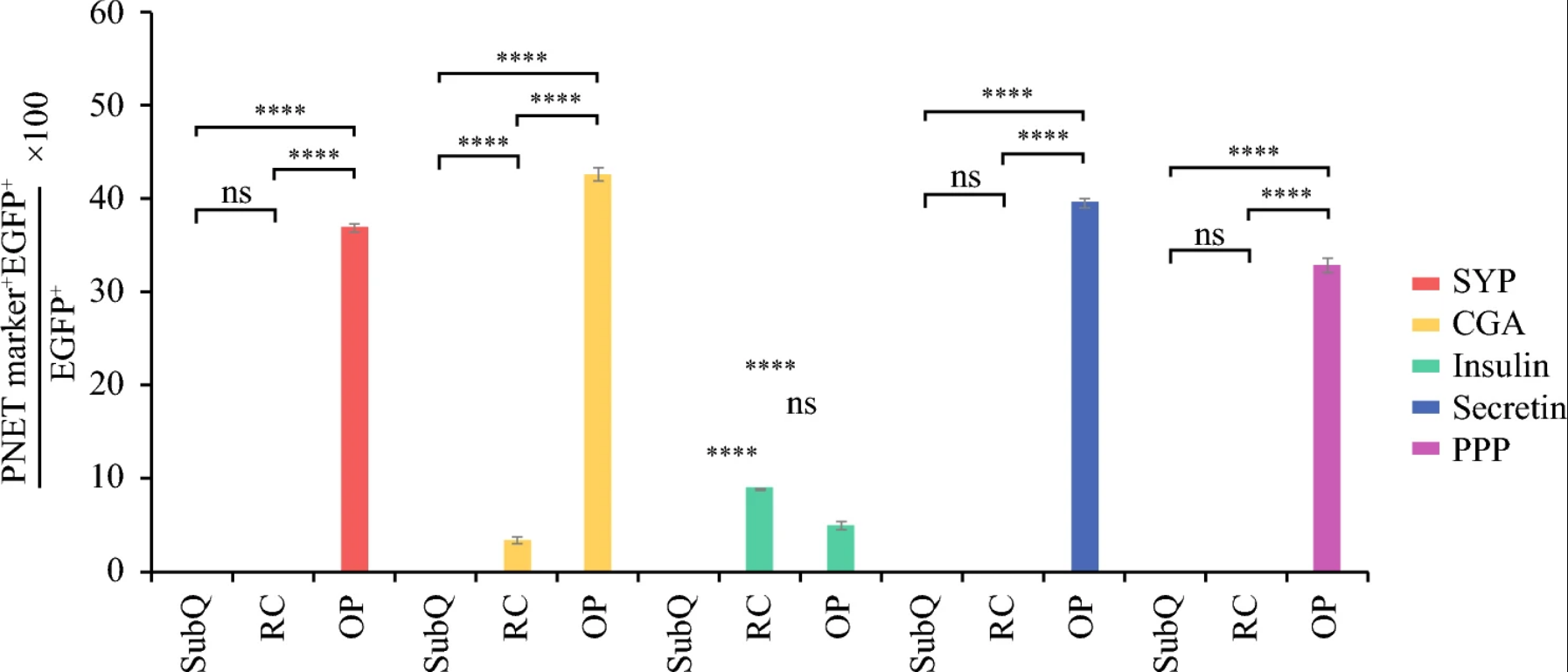
图6:胰腺神经内分泌肿瘤模型中 EGFP 标记的 STC-1 细胞谱系追踪
该图定量分析了 EGFP 阳性细胞与各类 PNET 标志物共表达的比例,结果显示 OP 模型中 EGFP 阳性细胞与突触素、嗜铬粒蛋白 A、分泌素、胰多肽的共表达比例均显著高于 SubQ 模型,与 RC 模型相比也有统计学优势;RC 模型中 EGFP 阳性细胞与嗜铬粒蛋白 A、胰岛素的共表达比例显著高于 SubQ 模型;而胰岛素与 EGFP 的共表达比例在三组模型中均较低且无显著差异,证实胰腺原位微环境最能促进 STC-1 细胞向 PNET 样细胞分化,且胰岛素并非 STC-1 来源肿瘤的主要功能表型。
本研究成功构建了稳定共表达萤火虫荧光素酶和 EGFP 的双标记 STC-1 小鼠细胞系,并建立了皮下、肾被膜、胰腺原位三种胰腺神经内分泌肿瘤(PNET)异种移植小鼠模型,通过活体生物发光成像、组织学和分子生物学检测系统比较了不同模型的肿瘤生长、表型特征及与人类 PNET 的相似性,发现胰腺原位模型表现出旺盛的肿瘤生长能力,其组织形态、Ki-67 增殖指数和神经内分泌标志物表达最接近人类 1 级高分化 PNET,且 STC-1 细胞植活效率和神经内分泌分化程度最高,还能观察到罕见的转移现象,而皮下和肾被膜模型因微环境限制,无法充分模拟人类 PNET 的生物学特征;该胰腺原位模型不仅能实现肿瘤的无创实时监测和细胞谱系追踪,还因 STC-1 细胞的小鼠背景可用于构建免疫健全的同基因模型,为研究 PNET 生物学机制、评估新型治疗策略提供了兼具生物学相关性和实用性的临床前平台,同时研究也指出该模型存在物种特异性差异、难以模拟晚期转移性疾病、目前基于免疫缺陷小鼠无法研究免疫相关机制等局限性,未来需结合单细胞测序进一步探究分子机制,并构建免疫健全模型开展免疫治疗相关研究,该模型也可与现有人源 PNET 细胞系异种移植模型互补,丰富 PNET 转化研究的工具库。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:乙型肝炎病毒 preS1 结构域的多步骤受体结合机制
下一篇:粘液罗斯菌膜囊泡稳定不稳定铁以减轻UVB诱导的铁死亡