常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-18 17:00:55 细胞资源库平台 访问量:194
乙肝病毒(HBV)感染是全球主要公共卫生问题之一,有超过2.5亿人慢性感染HBV。而其中有超三分之一的人口集中在我国,人数接近1亿人。NTCP工具细胞,特别是外源表达NTCP的肝癌细胞系如HepG2-NTCP和Huh7-NTCP,因其易操作、短周期、重现性佳的特点,在乙肝病毒(HBV)研究中扮演着至关重要的角色。这些细胞模型能够有效模拟HBV的感染过程,为研究HBV的生命周期、宿主限制因子、病毒复制以及药物筛选提供了一个强大而便捷的体外平台。它们不仅有助于揭示HBV感染的分子机制,如DDX3作为宿主限制因子阻碍cccDNA转录,GPC5作为附着因子在感染入胞过程中的作用,还能通过直接与NTCP相互作用或下调NTCP表达来筛选和验证抗病毒药物的活性,例如环孢菌素A及其衍生物、雷帕霉素及其衍生物等。此外,这些工具细胞还促进了对HBV宿主特异性分子的发现,为发展支持HBV感染的小动物模型提供了可能,这对于乙肝相关研究和药物开发具有重大意义。
英文标题:Multistep receptor binding of the hepatitis B virus preS1 domain
中文标题:乙型肝炎病毒preS1 结构域的多步骤受体结合机制
发表期刊:《Nature Communications》
影响因子:15.7
作者单位:
1.Department of Drug Development, National Institute of Infectious Diseases, Japan Institute for Health Security, Tokyo, Japan;
2.Department of Virology II, National Institute of Infectious Diseases, Japan Institute for Health Security, Tokyo, Japan;
3.Department of Applied Biological Science, Tokyo University of Science, Noda, Japan
作者信息:
Chisa Kobayashi, Toru Ekimoto, Koji Ooka, Junki Mifune, Kayo Matsuzawa
乙型肝炎病毒(HBV)和丁型肝炎病毒(HDV)具有狭窄的宿主范围,仅感染人类和黑猩猩等有限物种的肝细胞,这种组织和物种嗜性主要由病毒表面蛋白与宿主细胞受体的高亲和力相互作用介导。病毒大表面蛋白(LHBs)的 N 端 preS1 结构域是识别宿主受体 —— 牛磺胆酸钠共转运多肽(NTCP)的关键,其中 N 端豆蔻酰化的 2-48 位氨基酸(myr-2-48¹ᵖʳᵉˢ¹)负责与 NTCP 结合,该相互作用决定了 HBV/HDV 的病毒感染性、传播效率、发病机制和宿主嗜性等关键病毒学特征。preS1 是一种内在无序肽(IDP),具有构象灵活性,与许多其他病毒的稳定结构表面蛋白不同,其如何通过构象变化实现与 NTCP 的高亲和力结合机制尚不清楚。尽管冷冻电镜(cryo-EM)已解析出 myr-2-48¹ᵖʳᵉˢ¹ 与 NTCP 复合物的结构,显示 preS1 形成套索状结构并与 NTCP 的胆汁酸通道和细胞外表面接触,但这种复杂构象的形成过程仍不明确。因此,本研究通过结合基于结构的分子模拟与病毒学实验,旨在揭示 preS1 与 NTCP 结合的多步骤机制,为理解 HBV/HDV 独特的感染过程及开发新型治疗和预防策略提供重要见解。
本研究结合病毒学实验、冷冻电镜结构分析、分子动力学(MD)模拟和统计力学分析,系统探究 preS1 与 NTCP 的结合机制。首先,将 preS1 分为 myr-2-19¹ᵖʳᵉˢ¹、20-32¹ᵖʳᵉˢ¹ 和 33-48¹ᵖʳᵉˢ¹ 三个片段,通过 TAMRA 荧光标记肽结合实验、肽竞争实验和 HDV 感染竞争实验,评估各片段对 NTCP 的结合能力。针对 preS1 的 7-19 位氨基酸进行丙氨酸突变,通过荧光结合实验和 HDV 感染实验筛选关键结合位点;对 NTCP 中与 preS1 关键残基距离 4.5Å 内的候选氨基酸进行突变,结合 preS1 结合实验、HDV 感染实验、胆汁酸转运实验和细胞表面蛋白表达分析,鉴定 NTCP 侧的关键相互作用残基。进行全原子 MD 模拟(每组 3 个独立 1μs 模拟),通过主成分分析(PCA)、距离频率分析、氢键分析和接触频率分析,探究 preS1 关键残基对复合物稳定性的影响;构建携带 preS1 关键残基突变的 HDV 变体,在细胞培养(HepG2-NTCP 细胞)和体内模型(hNTCP 转基因小鼠)中评估病毒感染性。通过 MD 模拟分析 33-48¹ᵖʳᵉˢ¹ 区域与 NTCP 的接触特征,结合突变实验验证该区域的关键残基功能;利用 WSME-L 粗粒度统计力学模型预测 preS1 的折叠过程和结合顺序。实验数据采用 GraphPad Prism 进行统计分析,通过单因素方差分析判断组间差异,p<0.05 为差异有统计学意义,所有实验至少独立重复三次。
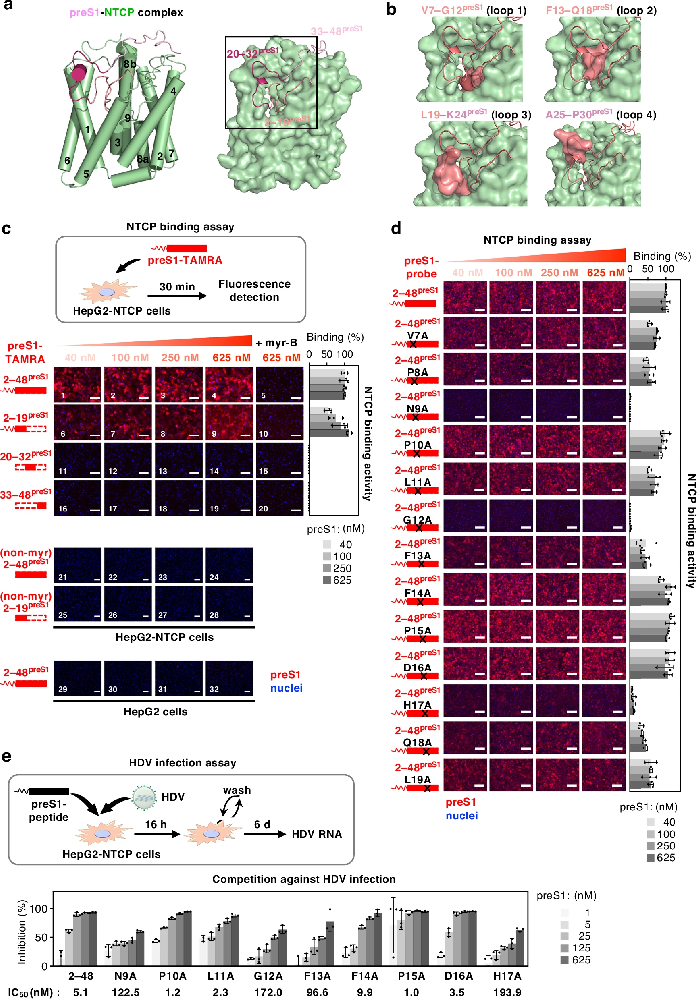
图1:preS1 的豆蔻酰化 2-19 位氨基酸区域是与 NTCP 初始结合的关键
该图展示了 preS1-NTCP 复合物的结构示意图,preS1 的 2-32 位氨基酸形成四环结构嵌入 NTCP 的胆汁酸通道,33-48 位氨基酸与 NTCP 细胞外表面接触。荧光结合实验显示,myr-2-48¹ᵖʳᵉˢ¹ 可特异性结合 NTCP 表达细胞,该结合可被 HBV 附着抑制剂 myrcludex-B(myr-B)阻断,而无 NTCP 表达的 HepG2 细胞无结合信号;myr-2-19¹ᵖʳᵉˢ¹ 可浓度依赖性结合 NTCP,但结合信号低于 myr-2-48¹ᵖʳᵉˢ¹,20-32¹ᵖʳᵉˢ¹ 和 33-48¹ᵖʳᵉˢ¹ 无结合活性,且非豆蔻酰化的 2-19¹ᵖʳᵉˢ¹ 和 2-48¹ᵖʳᵉˢ¹ 也无结合活性。肽竞争实验和 HDV 感染竞争实验证实,myr-2-19¹ᵖʳᵉˢ¹ 可剂量依赖性抑制 myr-2-48¹ᵖʳᵉˢ¹ 与 NTCP 的结合及 HDV 感染,而其他片段无此作用。丙氨酸突变实验显示,N9¹ᵖʳᵉˢ¹、G12¹ᵖʳᵉˢ¹ 和 H17¹ᵖʳᵉˢ¹ 突变几乎完全丧失 NTCP 结合能力和 HDV 感染抑制活性,F13¹ᵖʳᵉˢ¹ 和 Q18¹ᵖʳᵉˢ¹ 突变则中度降低相关活性。
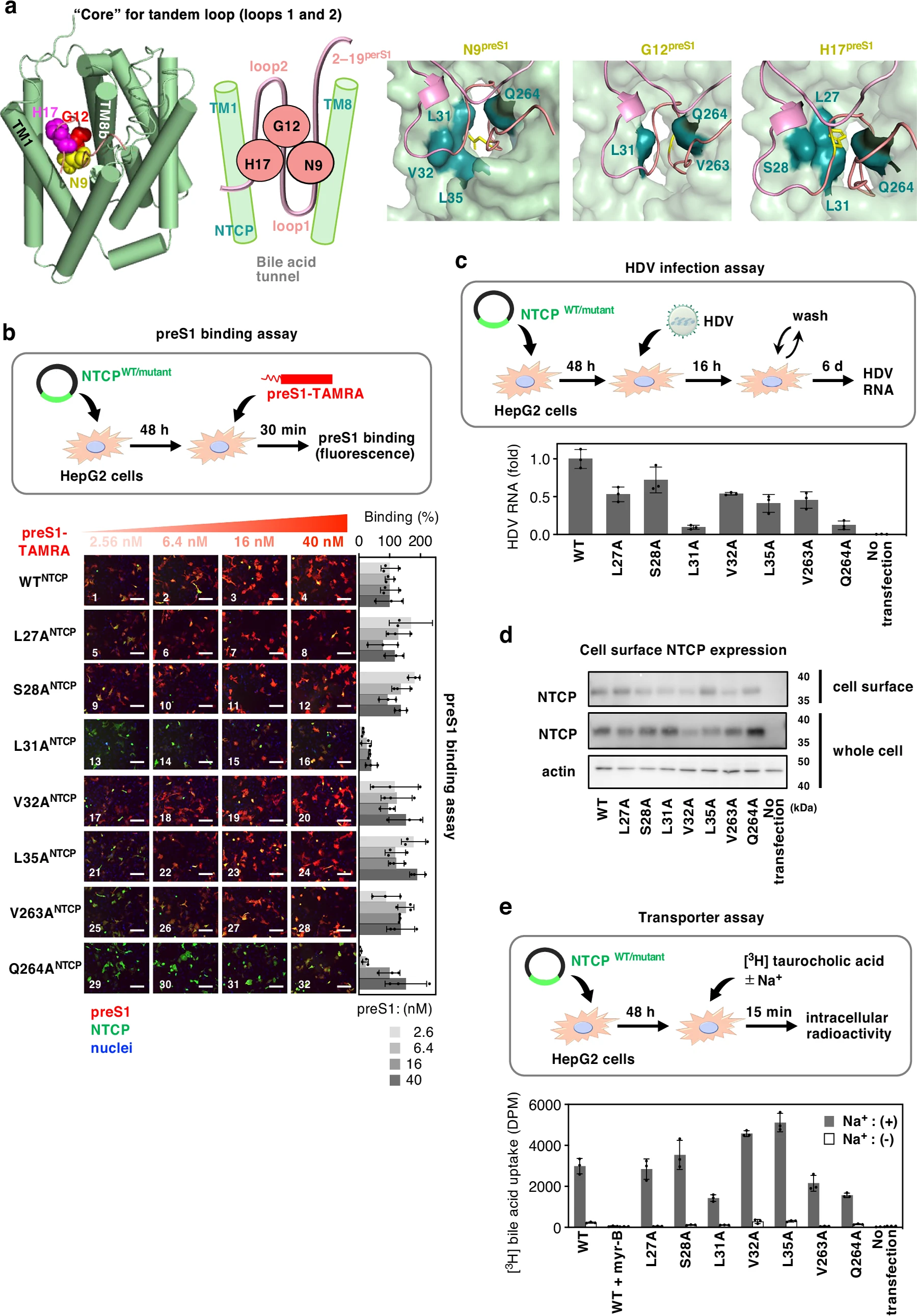
图2:NTCP 的 Leu31 和 Gln264 是 preS1 核心结构的关键结合位点
该图显示 preS1 的 N9¹ᵖʳᵉˢ¹、G12¹ᵖʳᵉˢ¹ 和 H17¹ᵖʳᵉˢ¹ 形成核心结构,与 NTCP 的 TM1 和 TM8b 区域相互作用。NTCP 突变实验显示,L31ᴺᵀᶜᴾ和 Q264ᴺᵀᶜᴾ突变显著降低 preS1 结合能力和 HDV 感染敏感性,而其他候选残基(L27ᴺᵀᶜᴾ、S28ᴺᵀᶜᴾ等)突变无显著影响。细胞表面表达分析显示,L31ᴺᵀᶜᴾ和 Q264ᴺᵀᶜᴾ突变体的细胞表面表达水平未明显受损;胆汁酸转运实验显示,两者仍保留部分转运活性,表明其功能缺陷特异性针对病毒受体作用,而非蛋白整体功能丧失。结构分析表明,L31ᴺᵀᶜᴾ(TM1)和 Q264ᴺᵀᶜᴾ(TM8b)是唯一与 preS1 的 N9¹ᵖʳᵉˢ¹、G12¹ᵖʳᵉˢ¹ 和 H17¹ᵖʳᵉˢ¹ 均距离 4.5Å 内的 NTCP 残基,形成对 preS1 核心结构的紧密夹持。
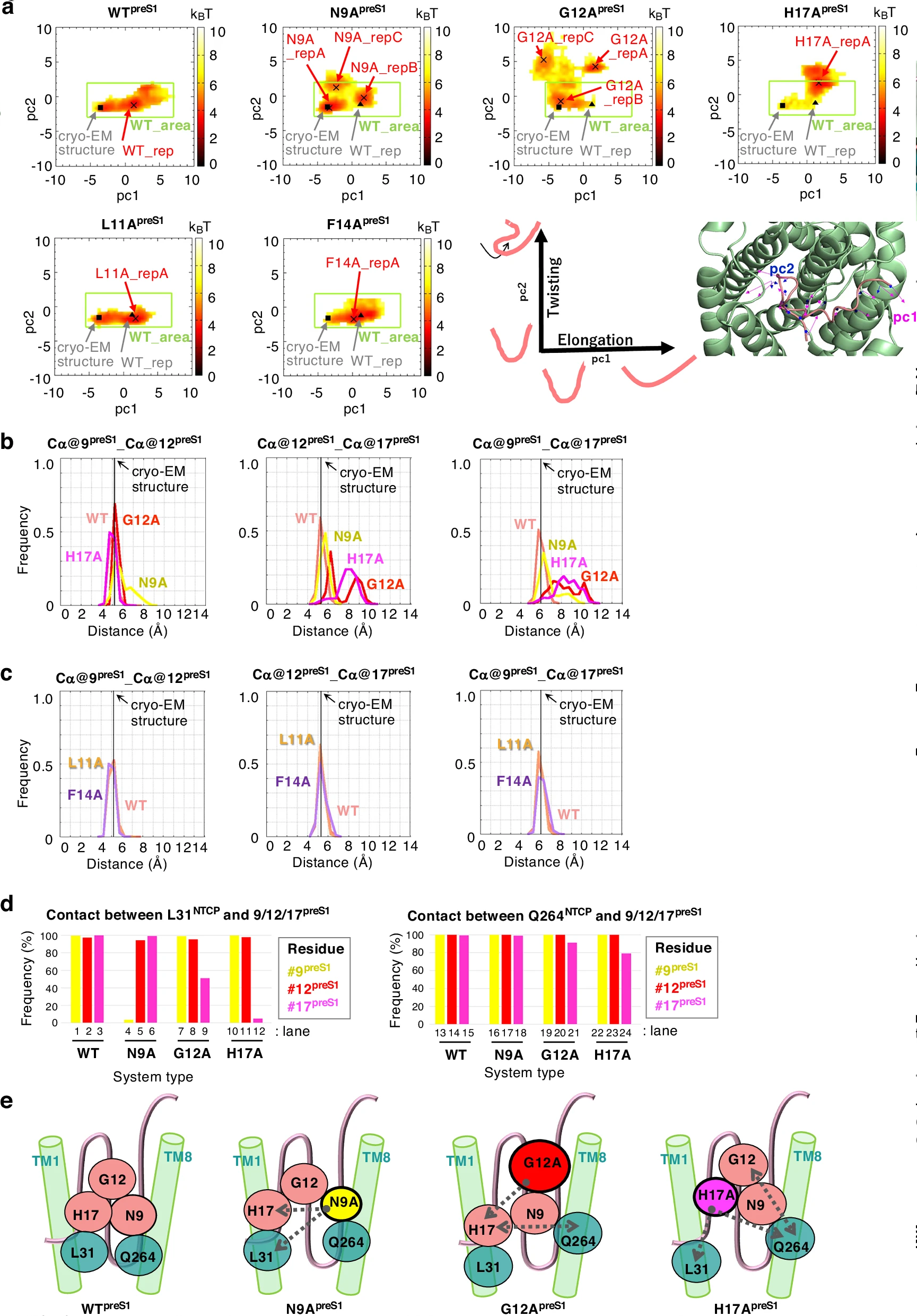
图3:分子动力学模拟揭示 preS1 核心残基对复合物稳定性的作用
该图通过 PCA 分析显示,野生型(WT)preS1 (2-19) 的结构分布集中在靠近冷冻电镜结构的区域,而 N9A、G12A 和 H17A 突变体的结构分布更分散,且远离 WT 区域,L11A 和 F14A 突变体(保留结合能力)的分布与 WT 相似。距离频率分析显示,WT 的 N9-G12、G12-H17 和 N9-H17 的 Cα 原子距离稳定在 4-7Å,而 N9A、G12A 和 H17A 突变体的这些距离更具多样性且整体增大。氢键分析表明,N9A 突变破坏了与 L11¹ᵖʳᵉˢ¹ 的氢键,H17A 突变破坏了与 F13¹ᵖʳᵉˢ¹ 和 F14¹ᵖʳᵉˢ¹ 的氢键,G12A 突变因空间位阻影响 H17 与 G12 的近距离接触。接触频率分析显示,N9A 突变降低了与 L31ᴺᵀᶜᴾ的接触频率,G12A 突变降低了 H17 与 L31ᴺᵀᶜᴾ的接触,H17A 突变降低了与 L31ᴺᵀᶜᴾ和 Q264ᴺᵀᶜᴾ的多重接触,证实这些残基通过维持分子内和分子间相互作用稳定复合物。
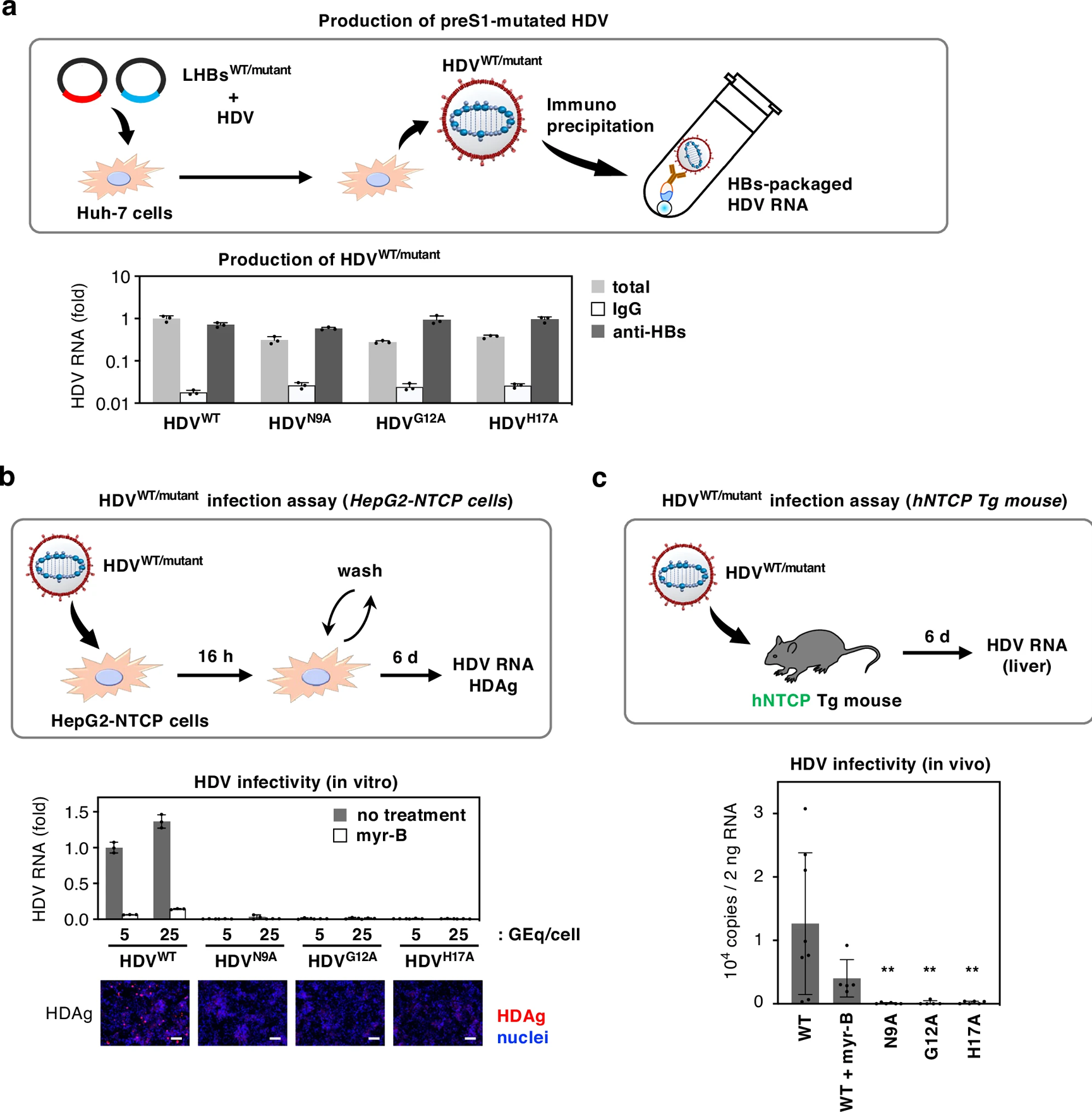
图4:preS1 的 N9、G12 和 H17 残基对病毒感染性至关重要
该图显示,携带 preS1 的 N9A、G12A 或 H17A 突变的 HDV 变体,其病毒颗粒产生不受影响(HBs 包装的 HDV RNA 水平与野生型相当)。细胞培养感染实验中,野生型 HDV 可剂量依赖性感染 HepG2-NTCP 细胞,检测到 HDV RNA 和 HDAg 表达,而三种突变体在任何接种剂量下均无明显感染信号。体内感染实验中,hNTCP 转基因小鼠接种野生型 HDV 后,肝脏中可检测到 HDV RNA,myr-B 预处理可抑制感染,而接种三种突变体后均未检测到 HDV RNA,证实这些核心残基的完整是病毒获得感染性的必要条件。
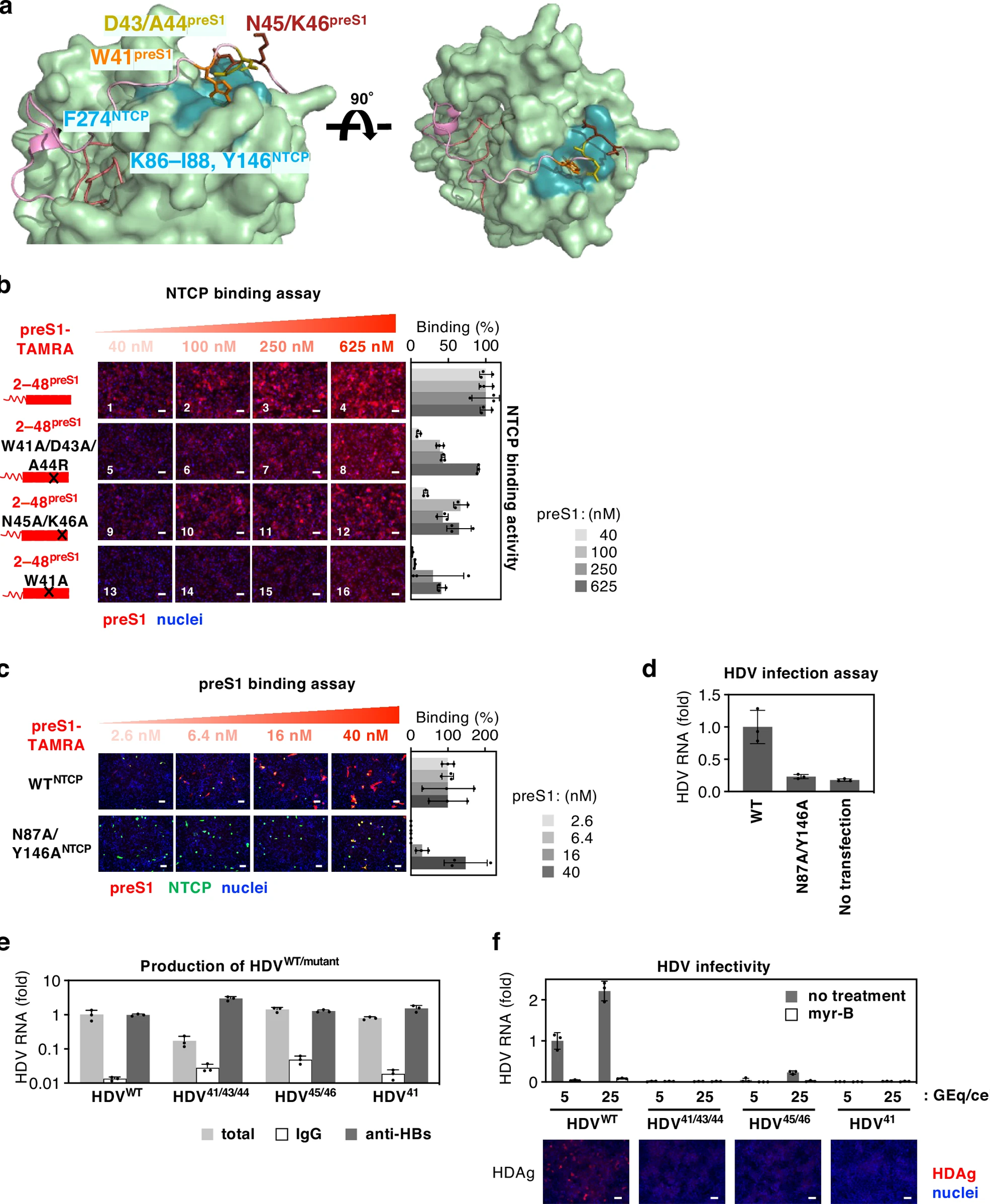
图5:preS1 的 Trp41 残基通过与 NTCP 细胞外表面相互作用稳定结合
该图显示,preS1 的 33-48 位区域中,W41¹ᵖʳᵉˢ¹、D43¹ᵖʳᵉˢ¹、A44¹ᵖʳᵉˢ¹、N45¹ᵖʳᵉˢ¹ 和 K46¹ᵖʳᵉˢ¹ 与 NTCP 的细胞外环(TM2-3、TM4-5、TM8-9 环)高频接触,其中 W41¹ᵖʳᵉˢ¹ 与 NTCP 的 N87ᴺᵀᶜᴾ和 Y146ᴺᵀᶜᴾ等关键位点相互作用。荧光结合实验显示,W41A/D43A/A44R、N45A/K46A 突变显著降低 preS1 与 NTCP 的结合能力,其中 W41A 单突变的抑制作用最显著。NTCP 的 N87A/Y146A 双突变显著降低 preS1 结合能力和 HDV 感染敏感性。携带 preS1 相关突变的 HDV 变体,其病毒产生正常,但感染 HepG2-NTCP 细胞的能力完全丧失,证实 33-48¹ᵖʳᵉˢ¹ 区域通过 W41¹ᵖʳᵉˢ¹ 等残基增强 preS1-NTCP 结合稳定性,对病毒感染至关重要。
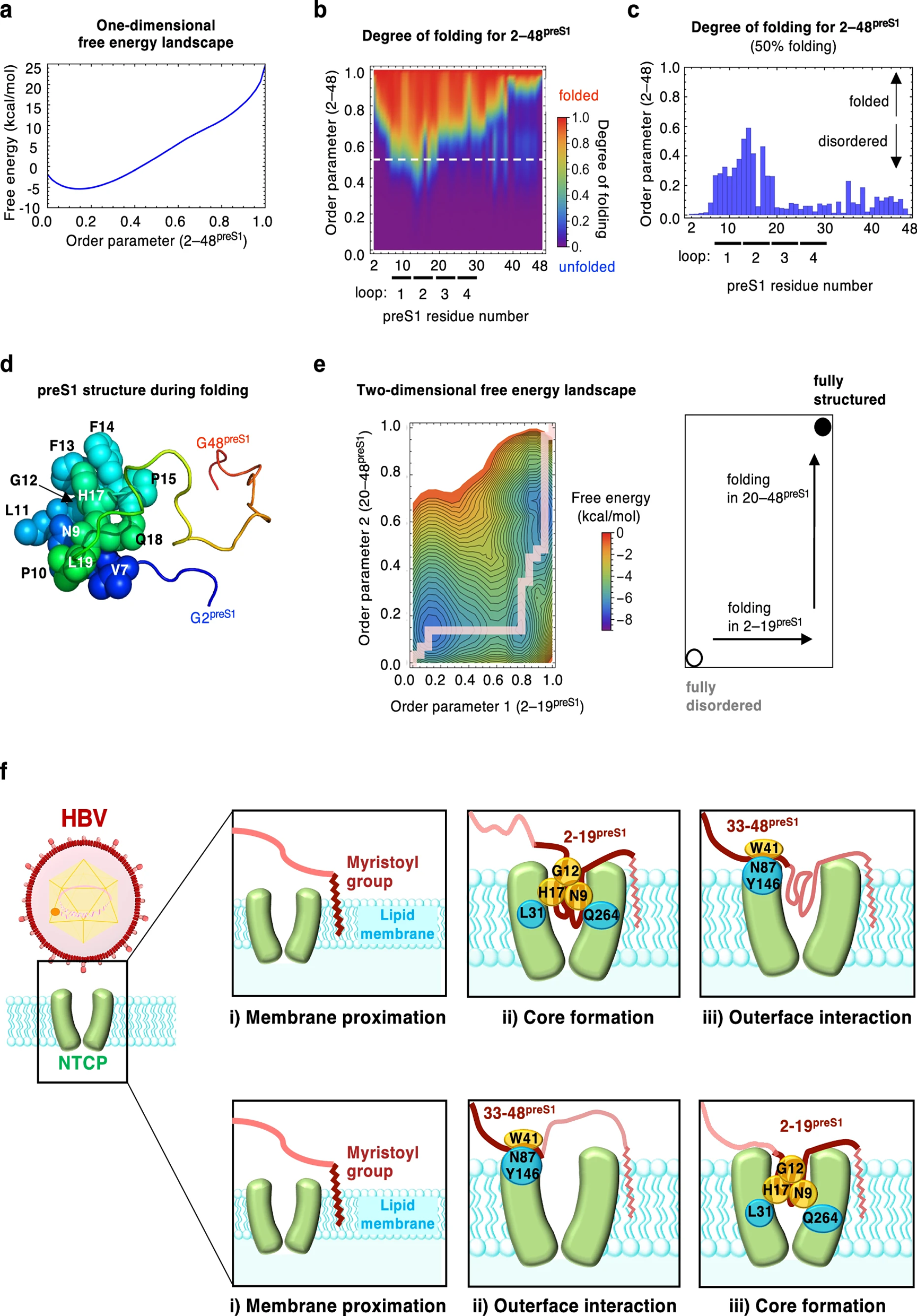
图6:统计力学模型揭示 preS1 的折叠和结合顺序
该图通过 WSME-L 模型预测,preS1 的一维自由能随折叠程度增加而升高,表明其为难以自发折叠的 IDP。残基特异性折叠程度分析显示,随着折叠进程推进,N 端 7-19 位氨基酸首先形成折叠结构,C 端 39-48 位氨基酸折叠最慢;当折叠程度为 50% 时,仅 7-15 位和 17-19 位氨基酸处于高折叠状态。二维自由能景观分析显示,preS1 从完全无序状态到完全结构化状态的最低自由能路径为:先发生 2-19 位氨基酸折叠,再发生 20-48 位氨基酸折叠。基于以上结果提出两种可能的结合模型:一是豆蔻酰基介导膜靠近→2-19 位氨基酸形成核心结构结合 NTCP 胆汁酸通道→33-48 位氨基酸与 NTCP 细胞外表面相互作用;二是膜靠近后先发生 33-48 位氨基酸与细胞外表面结合,再促进 2-19 位氨基酸核心结构形成和通道结合,两种模型均通过多步骤相互作用实现高亲和力结合。
本研究通过多学科手段揭示了 HBV preS1 结构域与宿主受体 NTCP 的多步骤结合机制,明确 preS1 作为内在无序肽,通过不同区域的协同作用实现高亲和力和特异性结合。preS1 的豆蔻酰化 2-19 位氨基酸区域是初始结合的关键,其中 N9¹ᵖʳᵉˢ¹、G12¹ᵖʳᵉˢ¹ 和 H17¹ᵖʳᵉˢ¹ 形成核心结构,通过分子内相互作用稳定串联环构象,进而与 NTCP 胆汁酸通道内的 L31ᴺᵀᶜᴾ和 Q264ᴺᵀᶜᴾ形成紧密相互作用,该核心结构的完整性是病毒感染的必要条件。preS1 的 33-48 位氨基酸区域虽不能单独结合 NTCP,但通过 W41¹ᵖʳᵉˢ¹ 与 NTCP 细胞外表面的 N87ᴺᵀᶜᴾ和 Y146ᴺᵀᶜᴾ相互作用,稳定 preS1 的动态构象,增强复合物结合强度。统计力学模型预测 preS1 的折叠遵循 N 端 7-19 位氨基酸先折叠、C 端后折叠的顺序,支持多步骤结合的诱导契合机制。preS1 的关键结合残基(N9、G12、H17、W41)在 HBV 菌株和灵长类嗜肝 DNA 病毒中高度保守,表明该结合机制具有进化保守性。本研究不仅阐明了 HBV/HDV 宿主嗜性的分子基础,还为开发靶向病毒受体结合过程的新型抗病毒药物提供了关键靶点和理论依据。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:TNFAIP2 调控新机制揭晓:Rac1-ERK-AP1 轴驱动 HIF1α 转录促进 TNBC 血管生成
下一篇:新型生物发光细胞系助力 PNETs 小鼠模型构建,为研究带来新工具!