常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-02-06 17:30:06 细胞资源库平台 访问量:161
检测细胞株广泛应用于药物发现、抗体开发、基因研究和毒性评估等领域。基于D-Luciferase的报告基因细胞株及其荧光素酶检测方法在药物初筛/复筛、表位竞争、药物生物活性检测等多方面展现了广泛的应用潜力。报告基因法已被药典收录,为国家认可的检测方法。报告基因细胞株多用于监测特定的生物过程或信号通路。
HEK293细胞因子报告基因细胞株是以HEK293为工具细胞,采用慢病毒感染的方式构建,不仅能够稳定表达细胞因子受体蛋白,并且能够表达荧光素酶报告基因,是基于转录因子信号通路构建的荧光素酶报告基因细胞系。当细胞因子结合受体蛋白后,细胞因子与受体蛋白相互作用,激活转录因子信号通路,从而激活荧光素酶的表达。荧光信号的强弱即代表信号通路的激活效果,因此可用于相关药物的体外效果评价,筛选抗体以及筛选信号通路的激活剂或抑制剂。
英文标题:Multi-omics driven genome-scale metabolic modeling improves viral vector yield in HEK293
中文标题:多组学驱动的基因组尺度代谢模型提高HEK293细胞的病毒载体产量
发表期刊:《Metabolic Engineering》
影响因子:6.8
作者单位:
1.Department for Analytical Chemistry, University of Vienna, Vienna, 1090, Austria
2.Doctoral School of Chemistry, University of Vienna, Vienna, 1090, Austria
3.Department of Applied Life Sciences, Bioengineering, University of Applied Sciences Campus Vienna, Vienna, 1100, Austria
Institute of Molecular Biotechnology, Institut für Molekulare Biotechnologie GmbH, Vienna, 1030, Austria
作者信息:
L. Zehetner,D. Széliová
HEK293 细胞是重组蛋白和腺相关病毒(AAV)等病毒载体生产的核心工具,但其活性病毒颗粒产量不足(仅 10% 含完整目的基因),限制了基因治疗应用。现有研究多依赖单组学分析,缺乏多组学整合与基因组尺度代谢模型(GSMM)的系统解析。本研究通过脂质组、外代谢组、转录组多组学分析,结合 GSMM 重建,对比高产(HP)和低产(LP)HEK293 菌株的代谢差异,识别产量限制瓶颈,发现低氧诱导因子 1α(HIF-1α)介导的假缺氧是 LP 菌株产量低的关键,为优化 AAV 生产工艺提供理论基础。
以 HEK293 细胞为模型,分 HP 和 LP 菌株,设转染(AAV 生产)和模拟转染组,在 5 个时间点(0、4、24、48、72 HPT)收集样本。核心实验包括:1)多组学检测:脂质组(LC-MS)、外代谢组(HILIC-HRMS)、转录组(复用已有数据);2)GSMM 构建:基于 human1 代谢模型,用 CORDA 算法整合多组学数据,生成 20 个条件特异性模型;3)动力学与通量分析:拟合生长速率、代谢物交换速率,通过无环通量采样和随机森林分类识别差异反应;4)验证实验:添加限制氨基酸(天冬氨酸、谷氨酸)或 HIF-1α 抑制剂(PX-478),检测 AAV 衣壳(ELISA)和基因组(ddPCR)产量;5)数据处理:用 R、Cobrapy 等软件进行建模与统计分析。
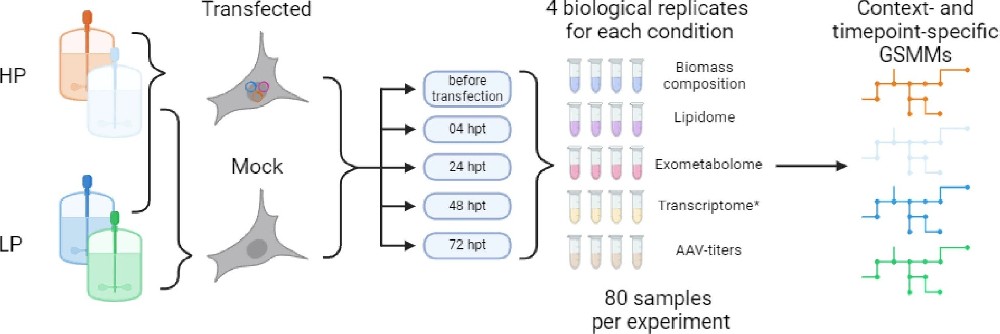
图 1:实验方法概览
整合多组学数据(脂质组、外代谢组、转录组)与 GSMM 重建,覆盖 80 个样本(2 菌株 ×2 条件 ×5 时间点 ×4 生物学重复),最终生成 16 个核心 GSMM,用于解析 AAV 生产的代谢调控机制(图 1)。
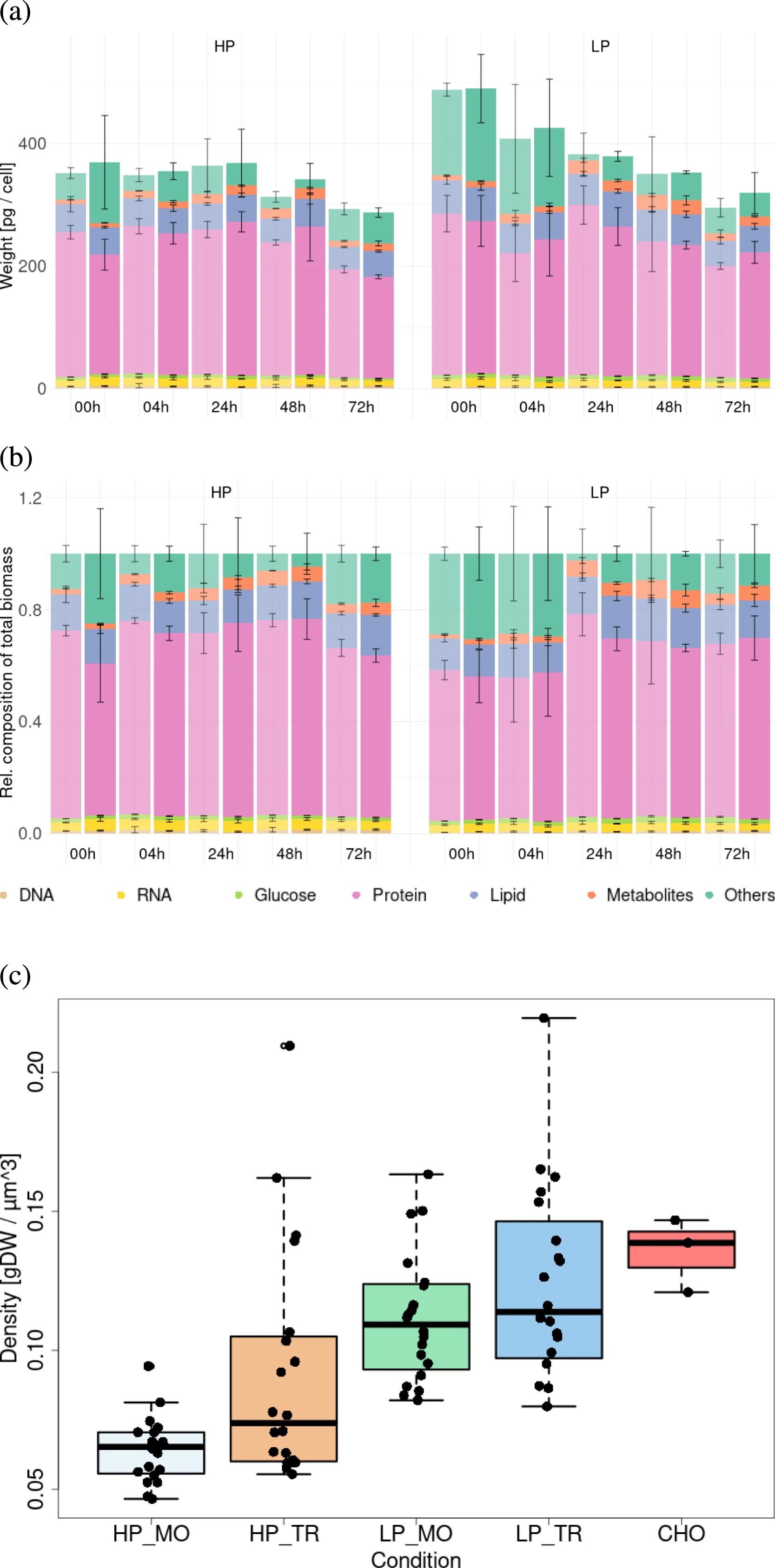
图 2:HP 与 LP 菌株的生物量差异
LP 菌株干重更高(平均 388.9 pg / 细胞)但体积更小,HP 菌株蛋白含量更高(转染后 4 HPT 尤为显著);LP 菌株 35% 干重为未知成分(可能为离子、多胺),HP 菌株成分更稳定(图 2a-c)。
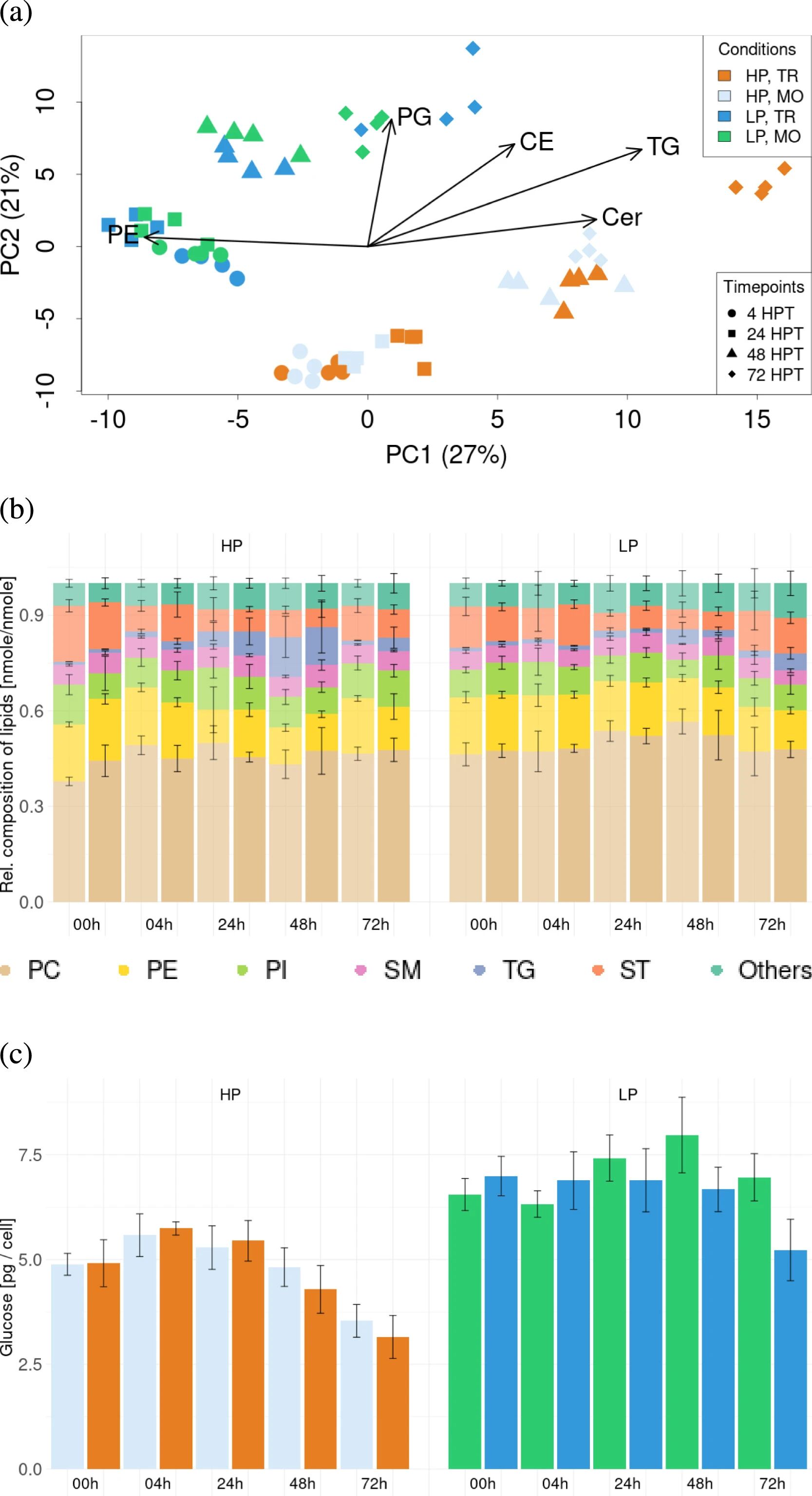
图 3:脂质组与能量储存差异
脂质组 PCA 清晰区分 HP 和 LP 菌株,核心驱动因素为甘油三酯(TG)、神经酰胺(Cer)等(图 3a);HP 菌株将葡萄糖转化为 TG 储存(TG 占比从 1% 升至 12%),LP 菌株则以糖原形式储存葡萄糖(图 3b-c),反映能量代谢策略差异。
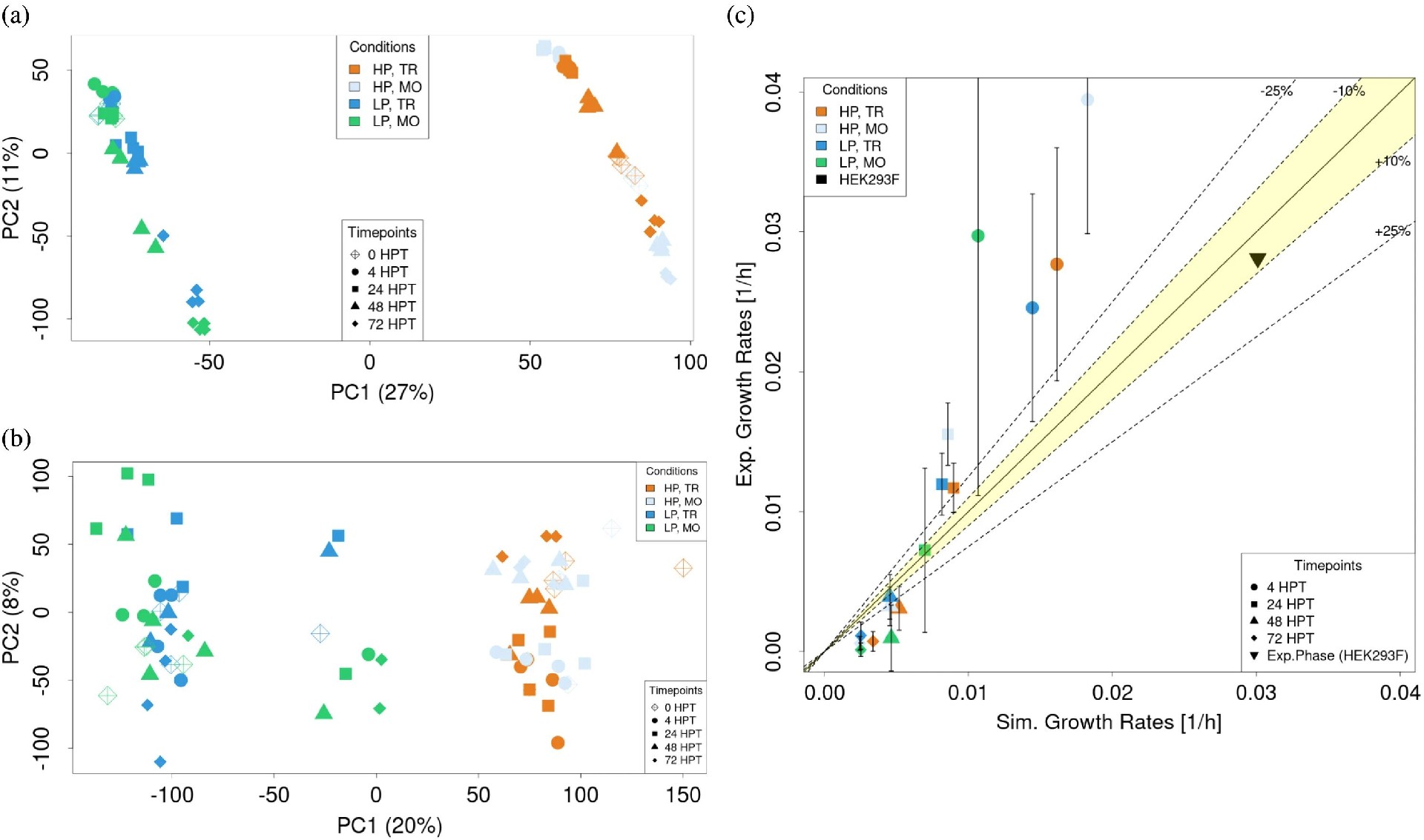
图 4:GSMM 的有效性验证
GSMM 的 LPCA 聚类与转录组 PCA 聚类趋势一致,能捕获菌株差异(图 4a-b);模拟生长速率与实验值误差 ±25%,可靠性良好(图 4c);HP 和 LP 菌株的 GSMM 包含约 9000 个反应、3100 个基因,覆盖核心代谢通路(表 3)。
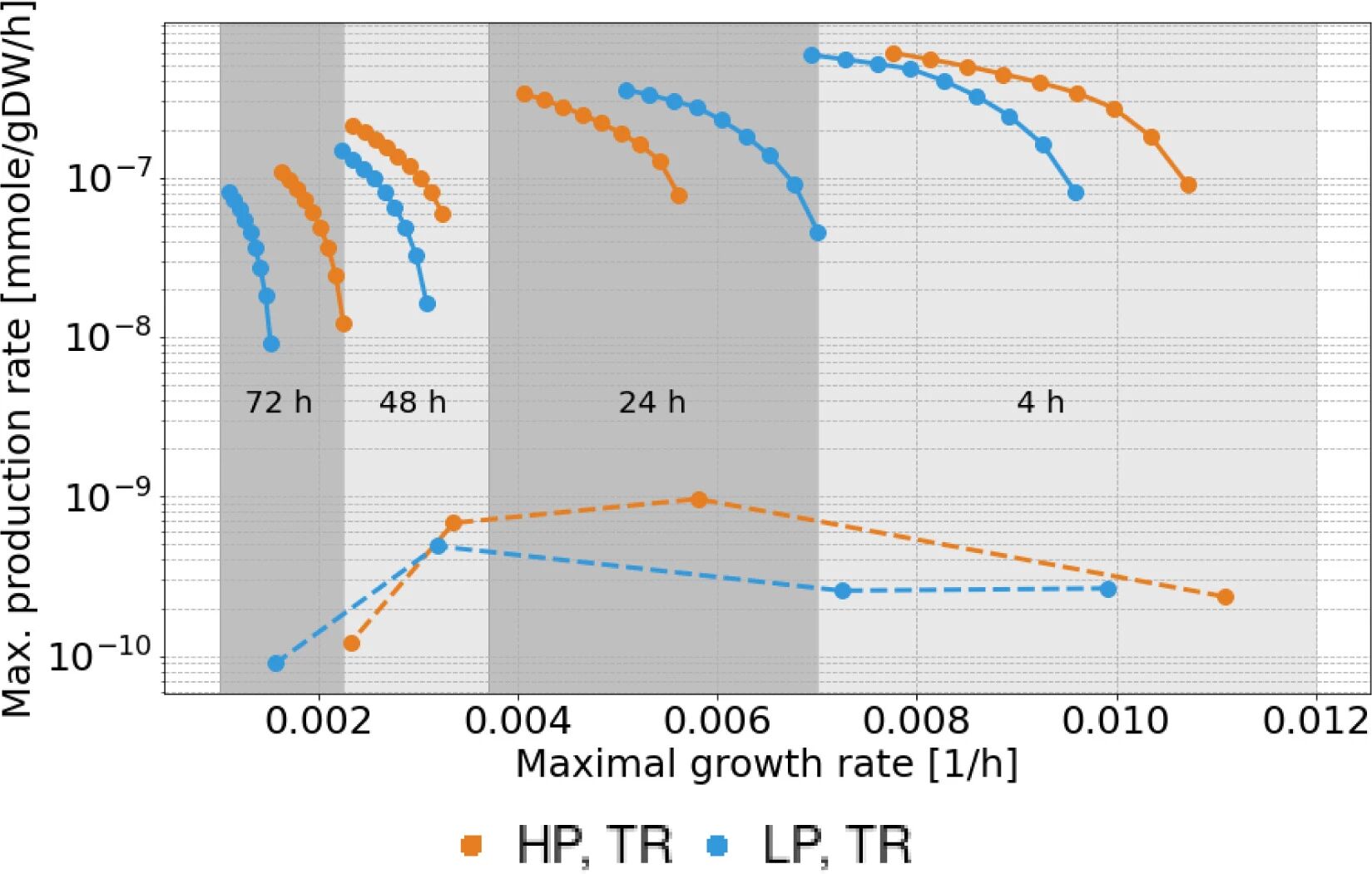
图 5:AAV 生产潜力分析
HP 和 LP 菌株的理论生产潜力(生产 envelope)接近,但实际产量仅为理论值的 1%(图 5);HP 菌株实际产量是 LP 的 6 倍,且两者均优先将资源分配给生长(>99.8%),而非 AAV 生产。
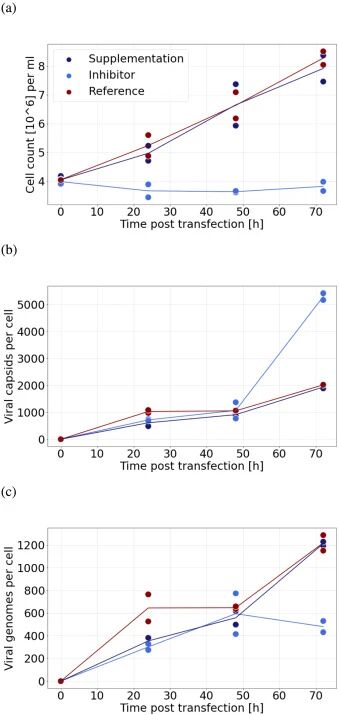
图 6:核心机制与验证结果
HIF-1α 激活:LP 菌株 HIF-1α 及其靶基因(PDK2/3/4、谷氨酰胺分解相关基因)显著上调(adj. p<10⁻¹⁶),伴随延胡索酸积累,形成假缺氧状态;
抑制剂验证:PX-478 抑制 HIF-1α 后,LP 菌株生长完全停滞,AAV 衣壳产量提升 2.5 倍,但病毒基因组产量下降,导致完整颗粒比例降低(图 6);
限制氨基酸:LP 菌株天冬氨酸、谷氨酸耗尽,HP 菌株丝氨酸耗尽,但补充该类氨基酸对产量无显著影响。
本研究通过多组学与 GSMM 整合,揭示 HEK293 细胞 AAV 生产的代谢调控机制,核心结论如下:1)HP 与 LP 菌株的代谢差异核心是能量储存方式(HP 为 TG,LP 为糖原)和假缺氧状态(LP 的 HIF-1α 激活);2)HIF-1α 是 LP 菌株产量限制关键,其激活通过抑制戊糖磷酸途径(PPP)减少核苷酸合成,导致基因组包装不足;3)HIF-1α 抑制可重分配资源提升衣壳产量,但需平衡衣壳组装与基因组复制;4)GSMM 能有效整合多组学数据,精准预测代谢瓶颈。研究为通过基因编辑(敲除 HIF-1α)或培养基优化(补充核苷酸)提高 AAV 产量提供了新策略。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:非人灵长类筛选 AAV2 展示肽库鉴定高效转导人血管内皮细胞的 “DWP” 基序变体