常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-01-24 17:34:19 细胞资源库平台 访问量:123
荧光素酶报告基因系统是一种基于荧光素酶催化底物氧化反应产生生物发光的检测技术,广泛应用于细胞生物学研究。其中,萤火虫荧光素酶(firefly luciferase, Fluc)因其高灵敏度、宽线性检测范围(约7~8个数量级)以及较短的半衰期(在哺乳动物细胞中约为3小时,在植物细胞中约为3.5小时)而成为最常用的报告基因。其发光信号强度在酶浓度为10⁻¹⁶ mol/L至10⁻⁸ mol/L的范围内与酶活性呈线性关系,并且在理想条件下可检测到低至10⁻²⁰ mol/L的荧光素酶活性。此外,荧光素酶报告基因系统具有非放射性、检测快速、灵敏度高(比氯霉素乙酰转移酶CAT高100倍)等优点,特别适用于高通量筛选和活细胞检测。通过将荧光素酶报告基因载体转染至宿主细胞后,可利用荧光素酶检测系统灵敏且便捷地监测基因表达水平,已成为细胞生物学研究中的重要工具。逸漠生物自主研发了近200种表达Fluc的细胞系,均经过荧光素酶活性检测验证,可满足科研人员的多样化需求,欢迎咨询。
英文标题:PET imaging of AAV9 and AAVBR1 trafficking in normal mice
中文标题:AAV9 和 AAVBR1 在正常小鼠体内转运的 PET 成像研究
发表期刊:《Scientific Reports》
影响因子:3.9
作者单位:
1.Division of Nuclear Medicine, Department of Radiology, Mayo Clinic, Rochester, MN 55905, USA
2.Mayo Clinic Comprehensive Cancer Center, Rochester, MN 55905, USA
3.Department of Pharmacology, Mayo Clinic, Rochester, MN 55905, USA
作者信息:
Aditya Bansal,Shalini Sharm,Manasa Kethamreddy
腺相关病毒(AAV)是基因治疗的重要载体,已获批用于眼部疾病、脊髓性肌萎缩等疾病治疗,但需非侵入性工具评估其靶向性、生物分布和清除情况。现有成像技术存在局限:光学成像组织穿透浅,MRI/CT 灵敏度低,124I 标记图像质量差,64Cu 半衰期短(12.7 小时)无法长期追踪。89Zr 半衰期(78.41 小时)适中、正电子能量低,适合长期高分辨率成像。本研究开发基于 89Zr-DBN 的 AAV 直接标记方法,追踪 AAV9(泛靶向)和 AAVBR1(脑靶向)在小鼠体内的转运,验证 PET 成像在 AAV 血清型筛选中的应用价值。
通过 89Y (p,n) 89Zr 反应制备 89Zr,与 DFO-Bn-NCS(DBN)螯合生成 [89Zr] Zr-DBN,在 pH 9.0 条件下与 AAV9-CMV-fLuc 和 AAVBR1-CMV-fLuc 的衣壳蛋白伯胺形成共价键,经凝胶过滤纯化(放射化学纯度 > 95%)。将标记后的 AAV 通过尾静脉注射到 BALB/c 小鼠体内,在注射后 5 分钟至 18 天内进行 PET 成像,检测不同器官标准化摄取值(SUV);18 天进行体外生物分布验证;注射后 3 周或 > 30 天通过生物发光成像检测荧光素酶表达,验证 AAV 感染效率。通过 SDS-PAGE 和放射自显影证实标记特异性,qPCR 定量 AAV 颗粒数,统计学分析采用独立样本 t 检验(P<0.05 为有意义)。
![图 1:[89Zr] Zr-AAV 细胞内转运示意图](/static/upload/image/20260116/1768542586290444.png)
图 1:[89Zr] Zr-AAV 细胞内转运示意图
该图阐明 AAV 感染的核心过程:标记后的 AAV 与细胞表面受体结合→内吞进入内体→内体逃逸→核进入→脱壳释放基因组→治疗基因表达,为 PET 追踪 AAV 转运提供理论框架。
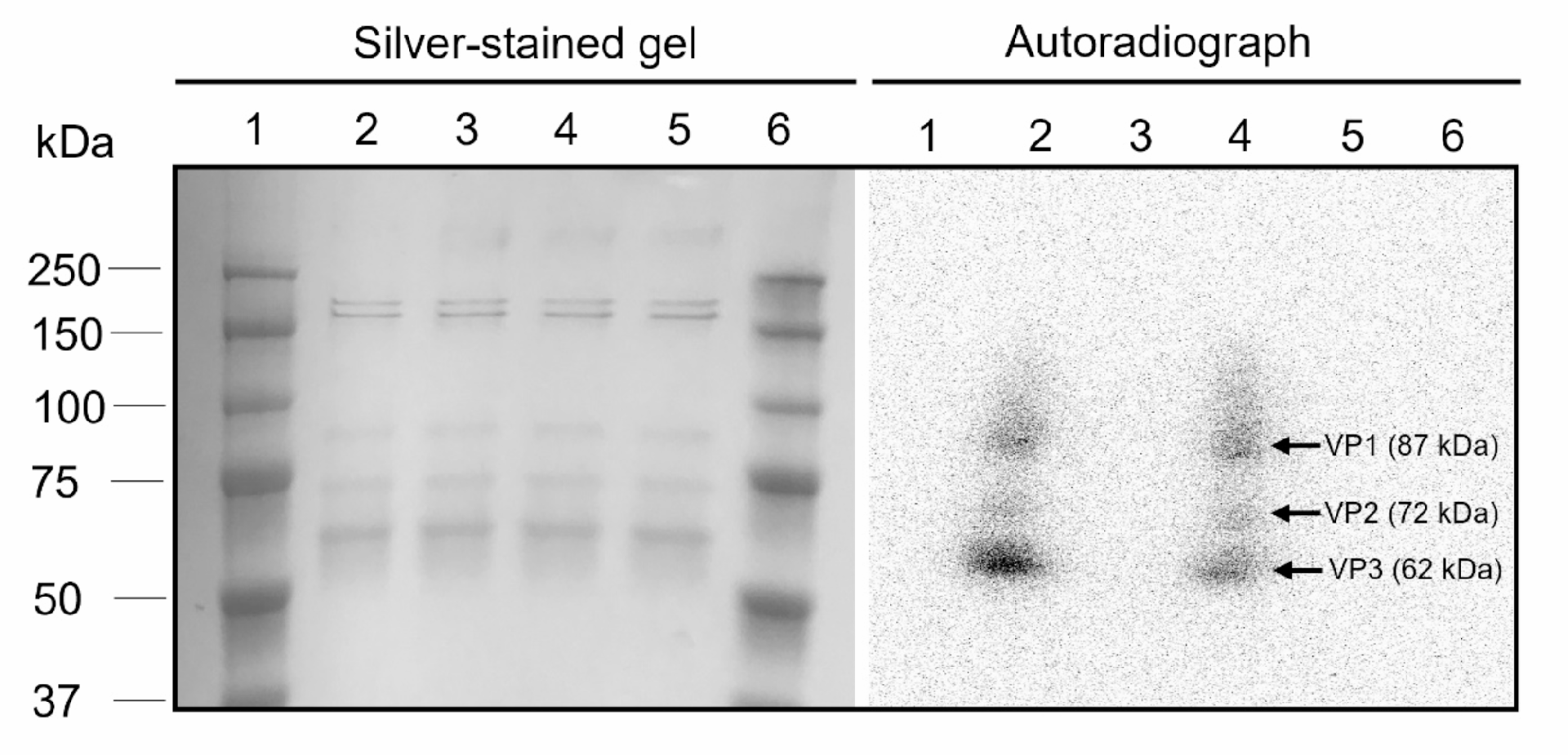
图 2:AAV 标记的 SDS-PAGE 与放射自显影验证
银染凝胶显示 AAV 衣壳蛋白 VP1(87 kDa)、VP2(72 kDa)、VP3(62 kDa)条带清晰;放射自显影证实 [89Zr] Zr-DBN 成功结合两种 AAV,标记特异性良好,未出现非特异性结合条带(图 2)。
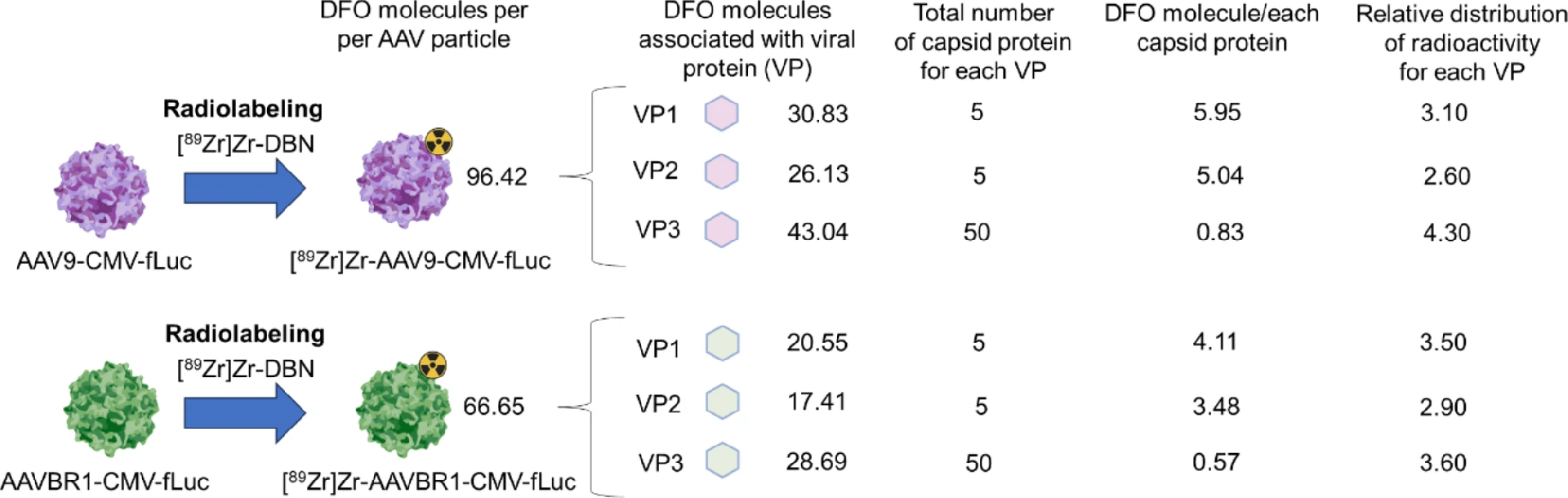
图 3:DFO 分子在 AAV 衣壳上的分布
每个 AAV9 颗粒平均结合 96.42 个 DFO 分子,AAVBR1 颗粒平均结合 66.65 个;VP1 和 VP2 的赖氨酸残基更易与 [89Zr] Zr-DBN 结合,放射性分布比例为 AAV9(VP1:VP2:VP3=3.1:2.6:4.3)、AAVBR1(3.5:2.9:3.6),与衣壳蛋白组成比例(1:1:10)不一致(图 3)。
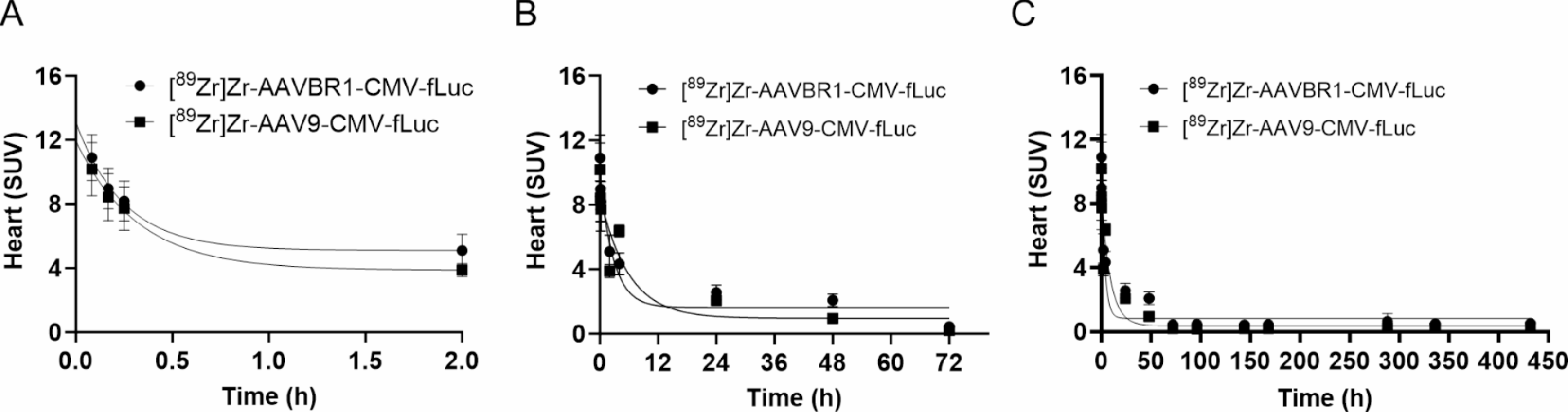
图 4:AAV 的血液清除曲线
两种 AAV 均呈双相清除:注射后 30 分钟内快速清除,随后缓慢清除至 72 小时,72 小时后血液中 PET 信号趋于稳定直至 18 天(图 4A-C)。[89Zr] Zr-AAV9 的早期清除速率略快于 [89Zr] Zr-AAVBR1,证实血清型差异影响体内动力学。
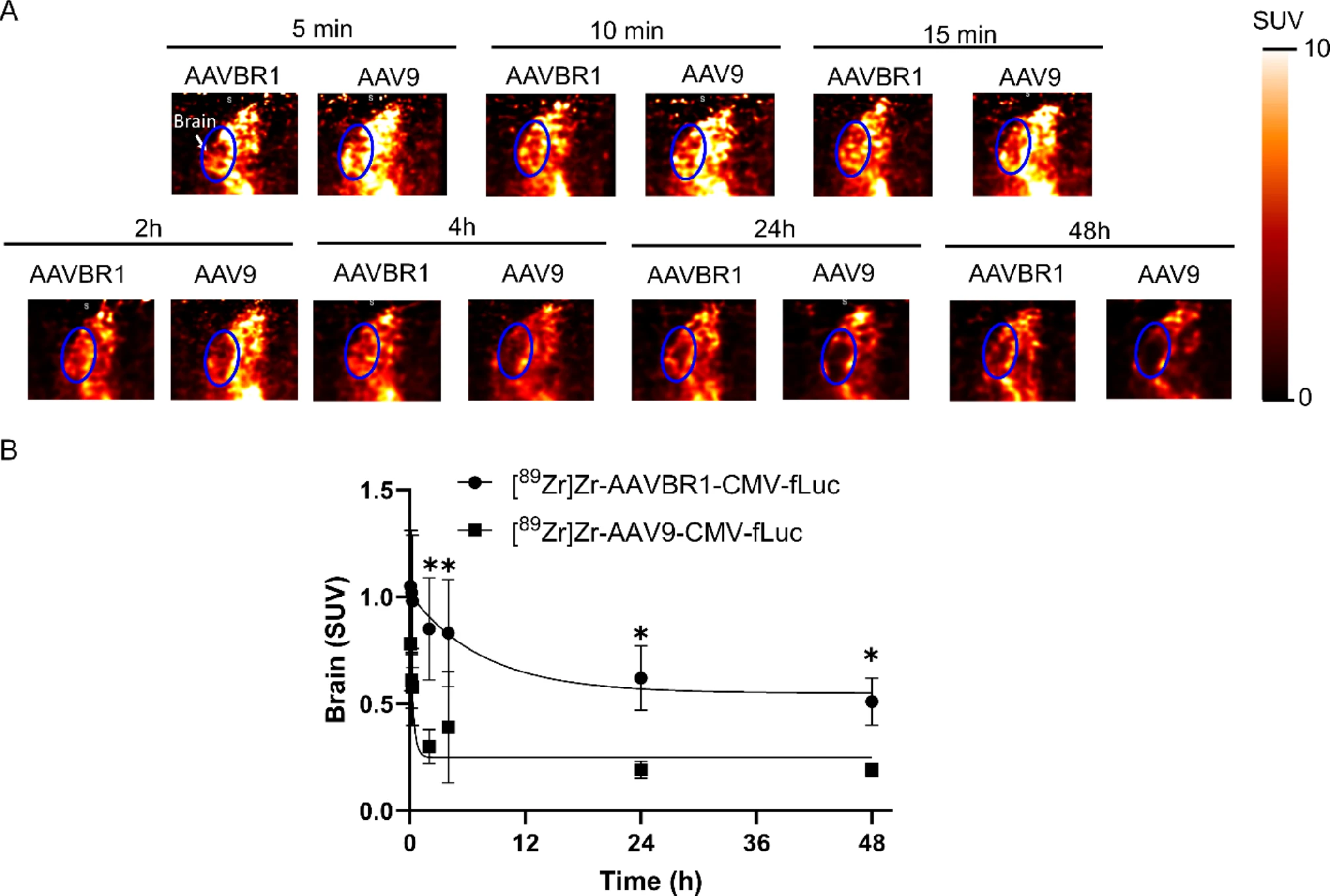
图 5:脑内摄取的 PET 成像与定量
注射后 10 分钟,AAVBR1 的脑 SUV(1.02±0.29)显著高于 AAV9(0.61±0.13,P=0.01);该差异持续至 18 天,体外生物分布进一步验证 AAVBR1 在脑内的特异性富集(图 5A-B),证实其脑靶向优势。
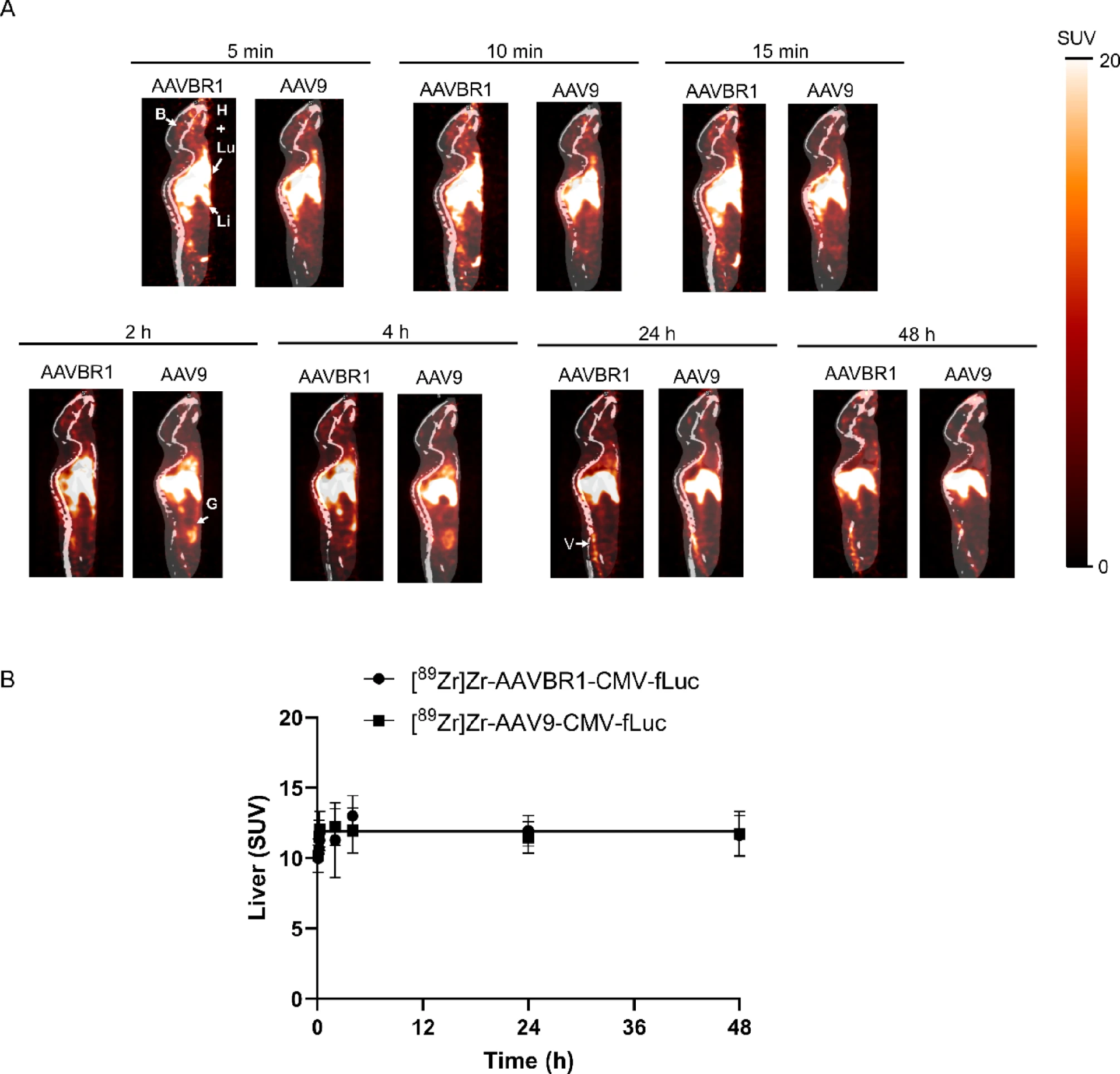
图 6:全身器官分布的 PET 成像
两种 AAV 在注射后 5 分钟即分布于肝、肺、脾、肾等器官;24 小时时差异最显著:AAVBR1 在肺、肾、肌肉、脑和脊椎的 SUV 更高,AAV9 在骨和脾的摄取更显著(图 6A-B);肝脏是两者主要富集器官,但无显著血清型差异。
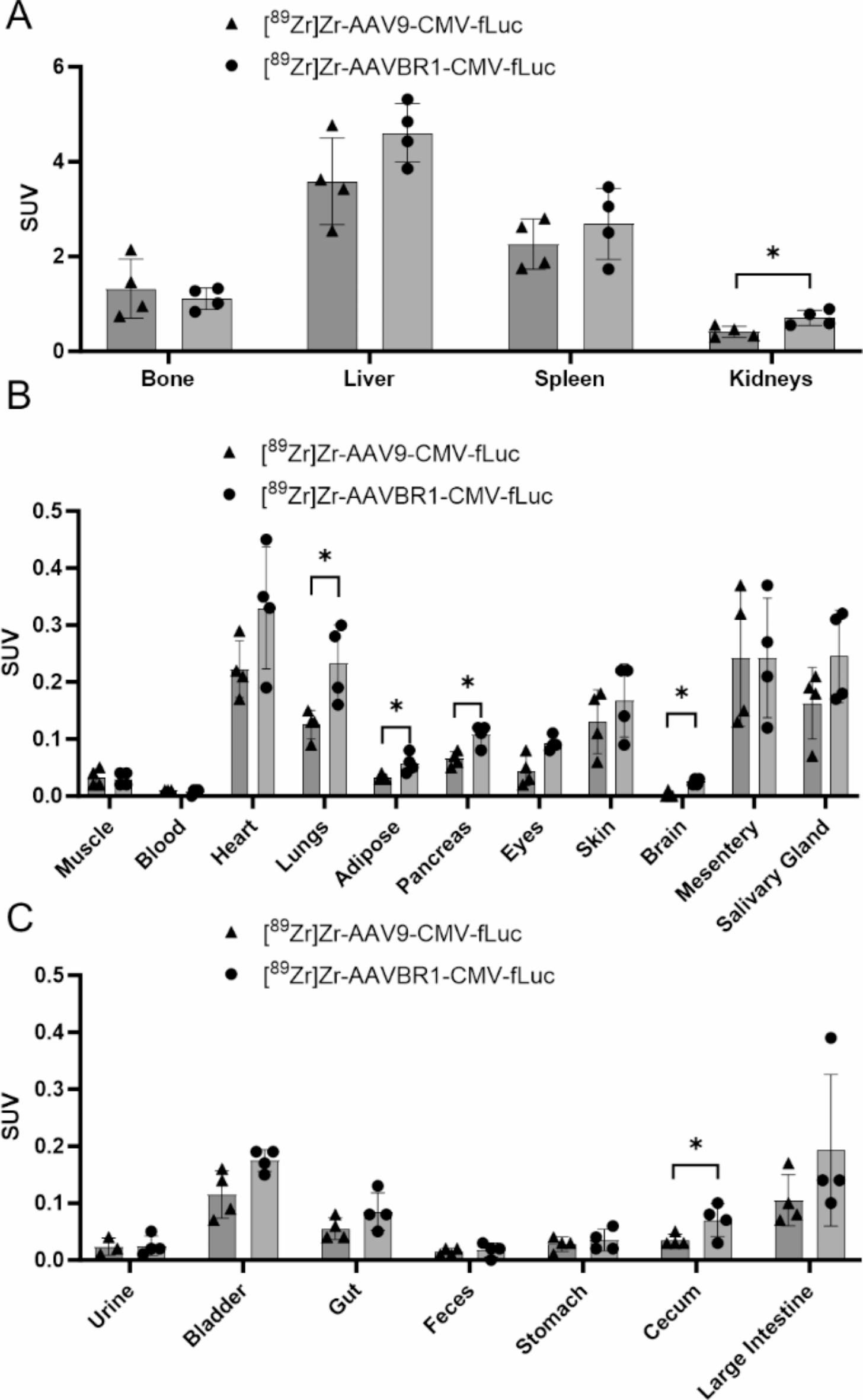
图 7:18 天体外生物分布验证
体外检测显示,肝、脾、肾的放射性最高;AAVBR1 在脑、肺、肾、胰腺、脂肪等器官的 SUV 显著高于 AAV9(P<0.05);性别差异存在:雌性小鼠肾摄取更高,雄性小鼠肌肉、皮肤等摄取更高(图 7A-C)。
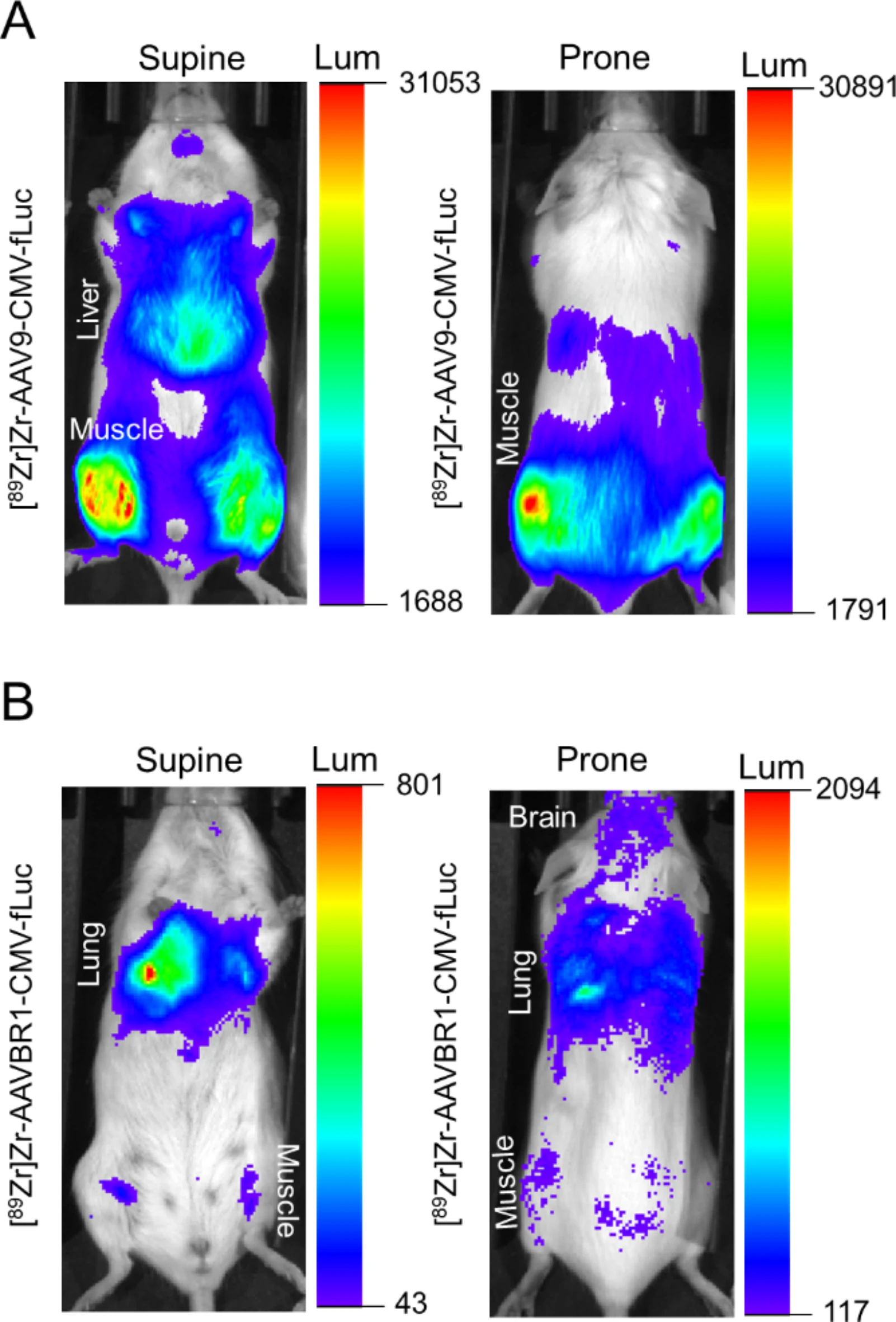
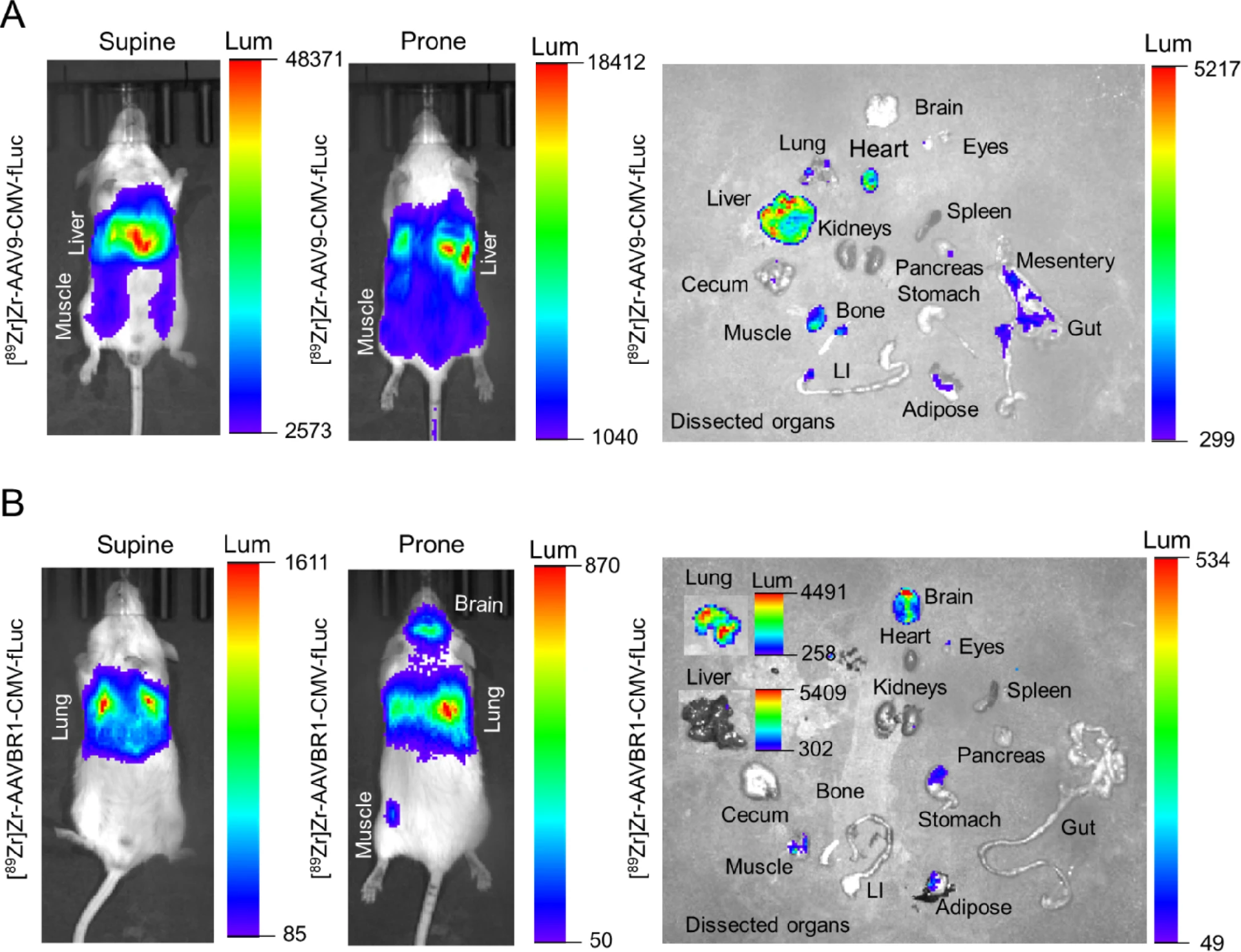
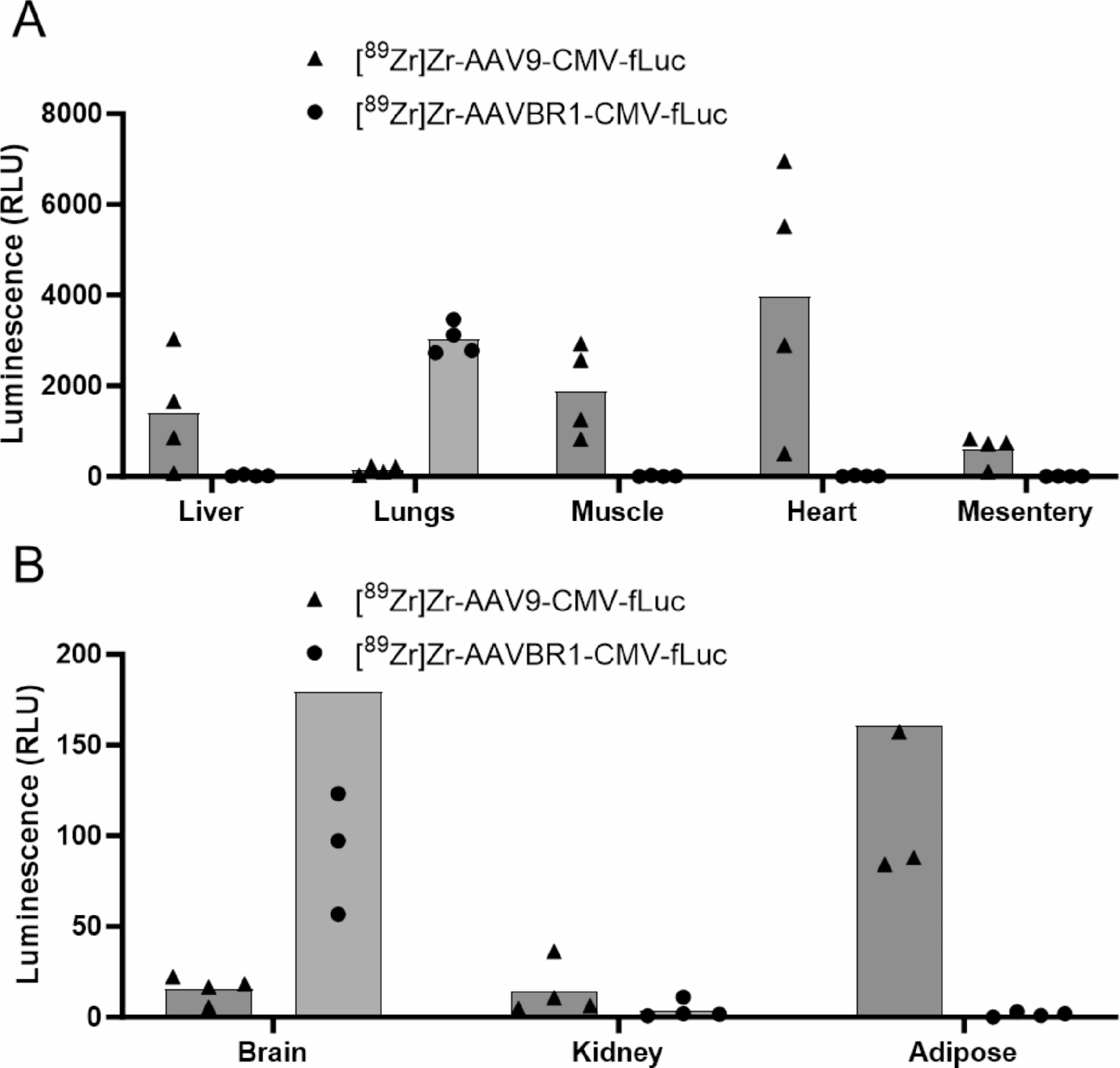
图 8-10:生物发光成像验证感染效率
注射后 3 周或 60 天,生物发光显示:AAVBR1 组脑和肺的荧光素酶信号更高,AAV9 组肝和肌肉信号更强(图 8-9);定量分析证实,脑、肾等器官的发光强度与 PET 成像及体外生物分布结果一致,肌肉中 AAV9 发光更强可能与 transduction 效率更高相关(图 10)。
本研究开发了基于 [89Zr] Zr-DBN 的 AAV 直接标记方法,放射化学纯度 > 95%,不影响 AAV 结构完整性和感染活性。通过 PET 成像实现了 18 天内对 AAV9 和 AAVBR1 的纵向追踪,证实:1)两种 AAV 呈双相血液清除,72 小时后体内分布稳定;2)AAVBR1 具有显著脑靶向性,脑摄取从 10 分钟至 18 天持续高于 AAV9;3)PET 成像数据与生物发光、体外生物分布结果高度一致,可准确反映 AAV 的体内转运和感染情况;4)存在性别差异,雌性肾摄取更高,雄性肌肉、皮肤等摄取更高。该方法为 AAV 血清型筛选、靶向性评估提供了非侵入性工具,助力基因治疗的临床转化。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:莫能菌素及其类似物在类器官模型中对乳腺癌干细胞的活性研究