常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-01-06 09:00:31 细胞资源库平台 访问量:200
三阴性乳腺癌(TNBC)是一种侵袭性强、治疗选择有限的乳腺癌亚型,化疗耐药率高,复发率高且预后差。传统治疗依赖化疗,但耐药性常导致治疗失败,而现有研究模型(如细胞系)难以模拟原发肿瘤的异质性和耐药特征。药物重定位(将已批准药物用于新适应症)为 TNBC 治疗提供了新思路,而患者来源类器官(PDO)能忠实再现肿瘤的分子特征和异质性,成为筛选有效药物的理想平台。本研究通过 TNBC 类器官筛选 FDA 批准药物,旨在发现能克服化疗耐药的潜在疗法。
来自泰国玛希隆大学 Ramathibodi 医院的团队在《Biomedicine & Pharmacotherapy》期刊发表了题为“Drug repurposing identifies proteasome inhibitors as antiproliferative agents counteracting inflammation-driven chemoresistance in triple-negative breast cancer organoids”的研究。
来源:从 4 例接受过化疗的 TNBC 患者的原发肿瘤和转移性皮肤病灶中获取组织,通过酶解和 Matrigel 包埋培养建立类器官,保留 ER、PR、HER2 阴性的 TNBC 表型及 Ki67 增殖特征,与原发肿瘤高度一致。
方法:对 133 种 FDA 批准的抗癌药物进行筛选,通过生长速率抑制(GR)分析和药物敏感性试验评估疗效;
结果:发现蛋白酶体抑制剂(硼替佐米 BTZ、卡非佐米 CFZ)为最有效的细胞毒性药物,在所有类器官中均表现出高 efficacy(GRₘₐₓ≤-0.95)和高 potency(GR₅₀≤0.28μM),优于传统化疗药(如多柔比星)。
抑制蛋白质翻译:通过蛋白质组学分析发现,BTZ 和 CFZ 显著下调核糖体蛋白(如 RPL12、RPS26),减少新生蛋白质合成,阻碍细胞增殖;
干扰细胞周期:诱导 G2/M 期阻滞(BTZ)或 S 期和 G2/M 期阻滞(CFZ),抑制肿瘤细胞分裂;
对抗炎症驱动的耐药性:转录组分析显示,多柔比星(DXR)诱导的炎症通路(如 TNF-α/NF-κB、I 型干扰素通路)在 BTZ 处理后被抑制,下调 IFITM1、CD74 等耐药相关基因,逆转炎症介导的化疗耐药。
药物响应动态实验显示,BTZ 和 CFZ 在模拟临床给药后的清除期仍能维持 cytotoxic 效应,有效抑制耐药细胞亚群(药物耐受持续细胞 DTPs);
为 TNBC 耐药患者提供了潜在治疗策略,支持蛋白酶体抑制剂在临床转化中的潜力,尤其是针对炎症驱动的耐药病例。
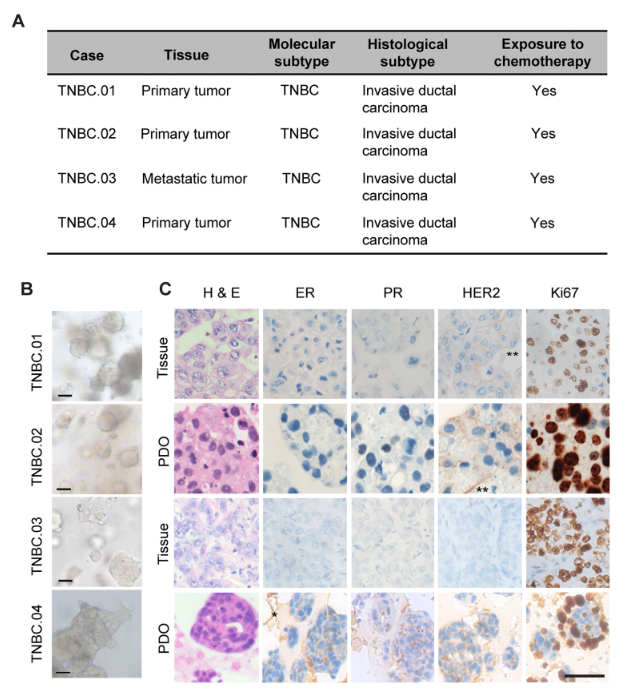
图 1:TNBC 患者来源类器官的表征
内容:展示 4 例 TNBC 患者的临床特征(肿瘤类型、化疗史),类器官的明场显微镜图像(呈不规则团状,尺度 50μm);通过 H&E 染色和免疫组化(ER、PR、HER2、Ki67)显示类器官与原发肿瘤在组织形态和分子表型上一致(ER、PR、HER2 阴性,Ki67 阳性率高)。
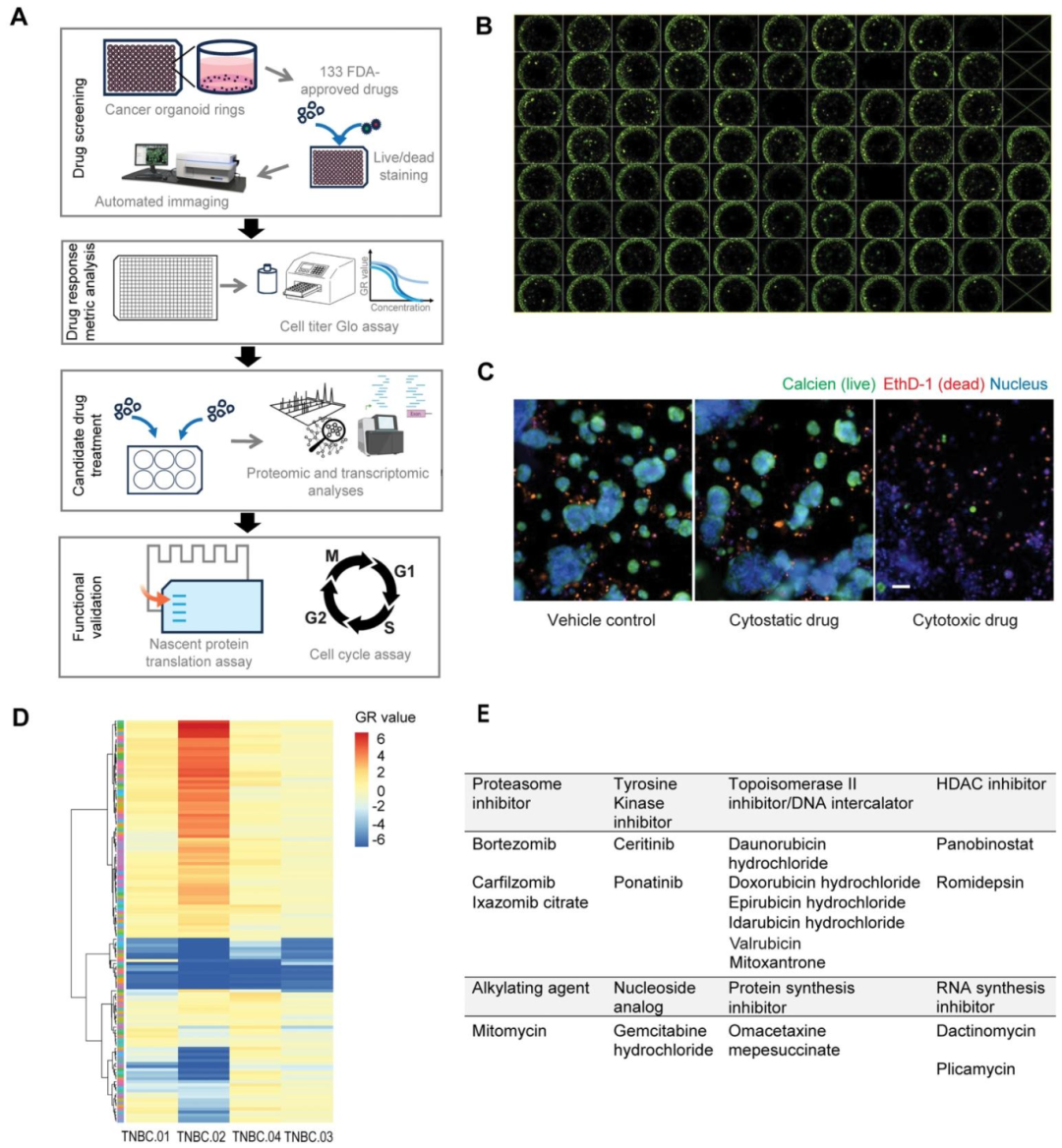
图 2:TNBC 类器官的高通量药物筛选流程
内容:概述筛选步骤 ——133 种 FDA 批准药物处理类器官(环形接种于 96 孔板),通过活 / 死染色(Calcein AM 标记活细胞,EthD-1 标记死细胞)和荧光成像分析;展示 GR 值分类(细胞毒性 GR<0、细胞抑制 GR=0、部分抑制 GR>0),并将 18 种有效药物分为 8 类(蛋白酶体抑制剂、酪氨酸激酶抑制剂等)。
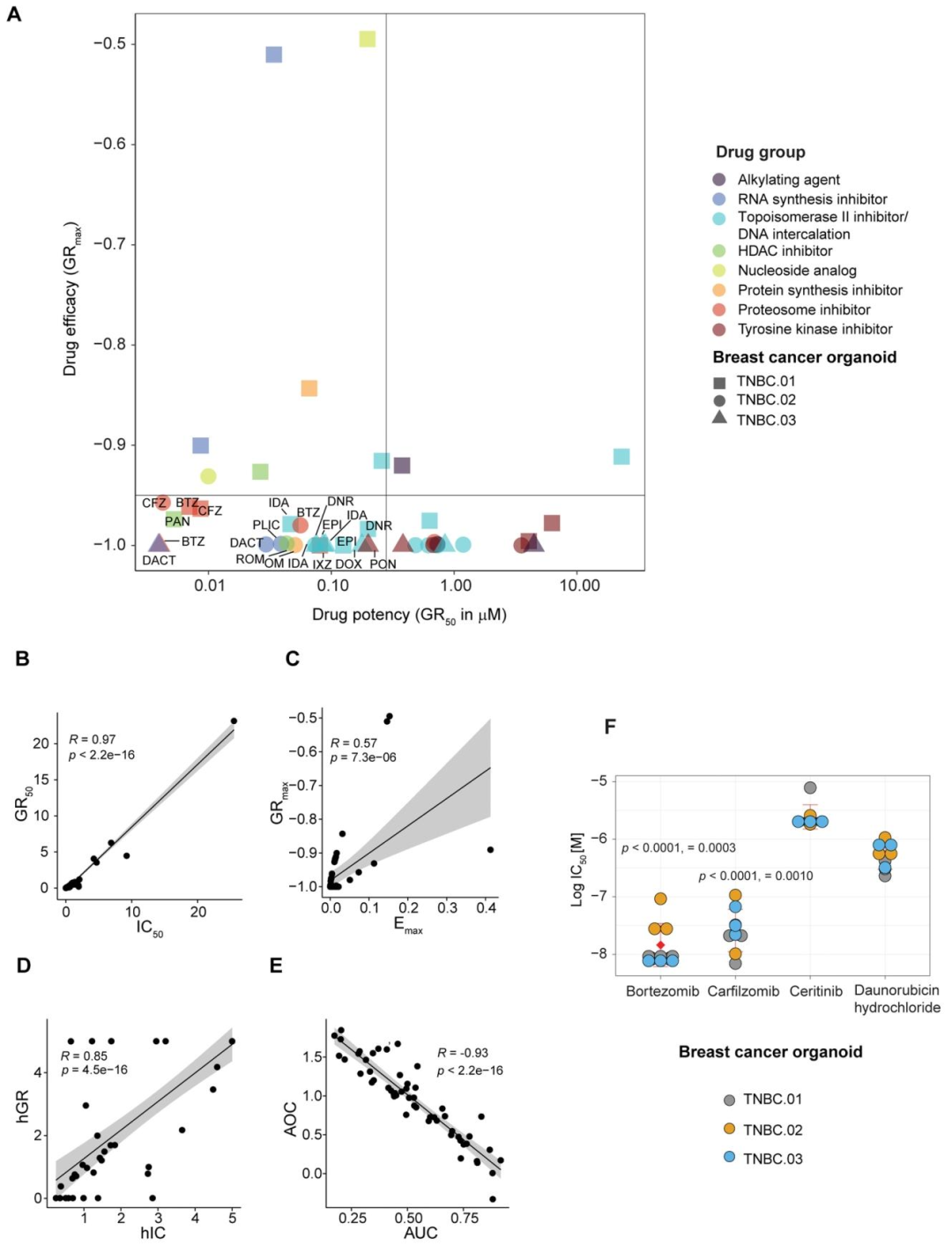
图 3:药物 efficacy 和 potency 分析
内容:热图显示 18 种药物在不同类器官中的 GR 值,蛋白酶体抑制剂(BTZ、CFZ)表现最优;散点图对比 GR 与 IC 指标的相关性(GR₅₀与 IC₅₀相关系数 0.97);柱状图显示 BTZ 和 CFZ 的 IC₅₀显著低于其他药物(P<0.0001),证实其高 potency。
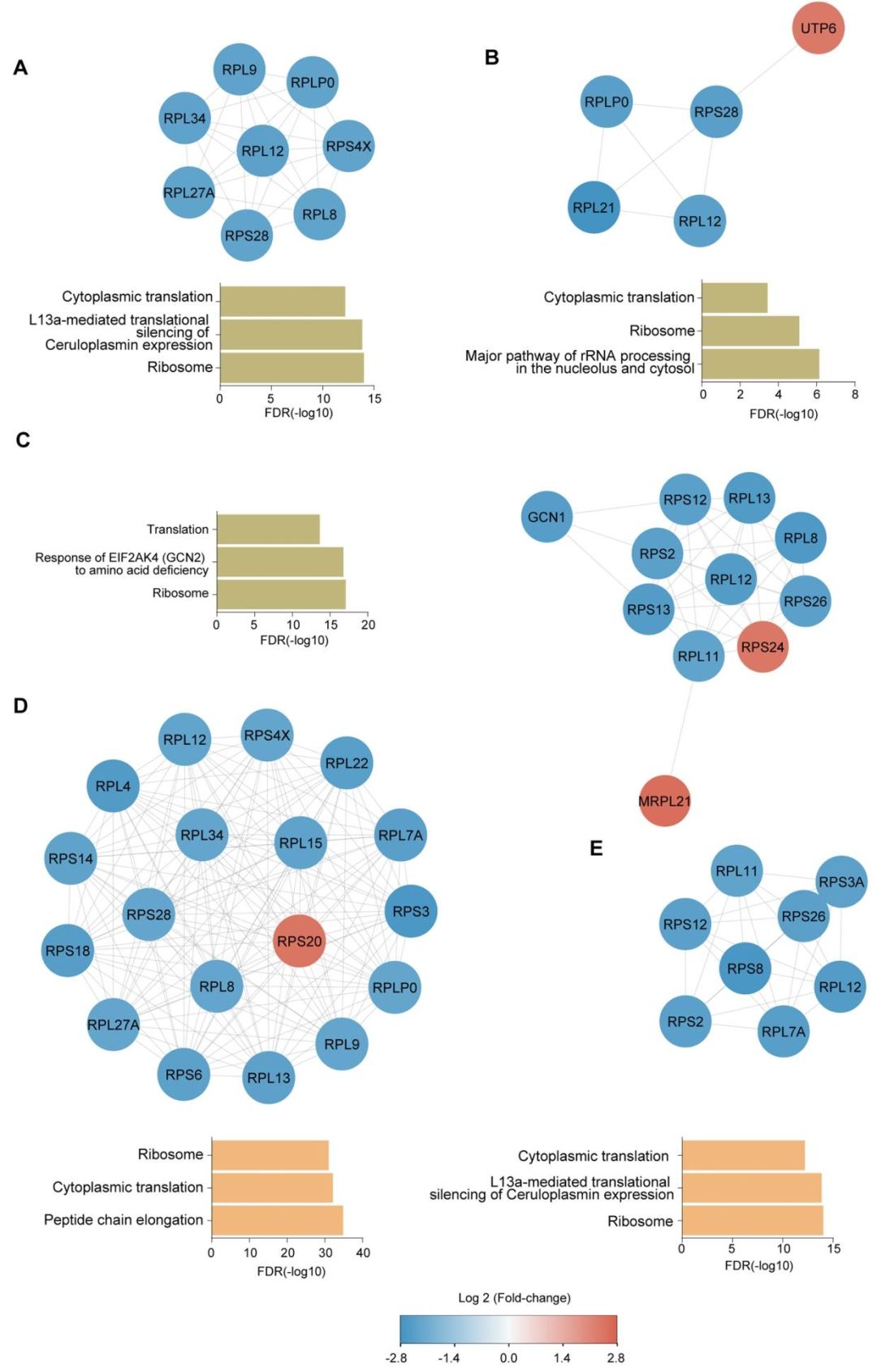
图 4:蛋白酶体抑制剂诱导的蛋白质相互作用网络
内容:展示 BTZ 和 CFZ 处理后差异表达蛋白的相互作用网络,核心为核糖体蛋白(RPL12、RPS28 等);GO 和 KEGG 富集分析显示显著富集 “核糖体”“细胞质翻译” 等通路,FDR 值 < 0.05。
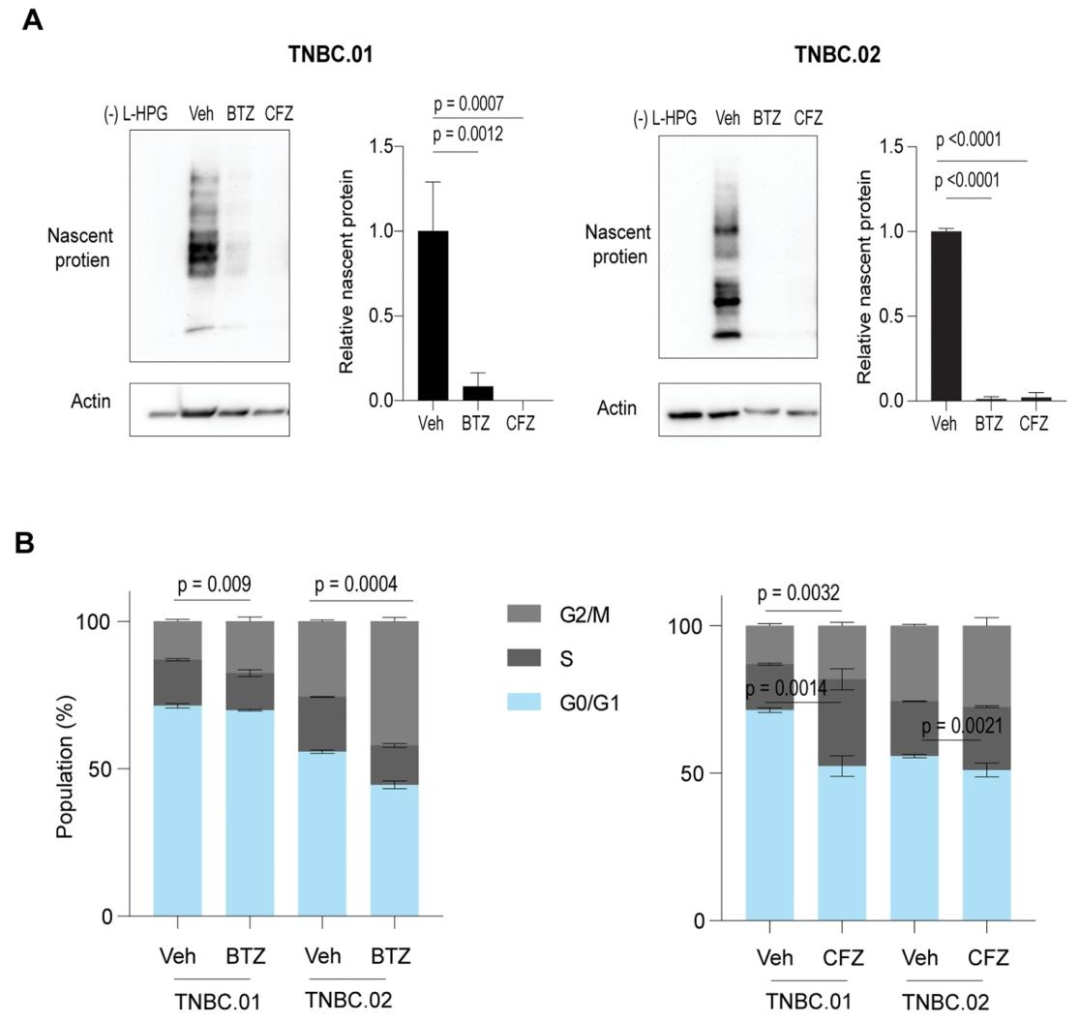
图 5:蛋白酶体抑制剂对蛋白质合成和细胞周期的影响
内容:新生蛋白检测显示 BTZ 和 CFZ 处理后 L-HPG 标记的蛋白水平显著降低(P<0.0001);细胞周期分析显示 BTZ 诱导 G2/M 期阻滞,CFZ 诱导 S 期和 G2/M 期阻滞(TNBC.01)或仅 S 期阻滞(TNBC.02)。
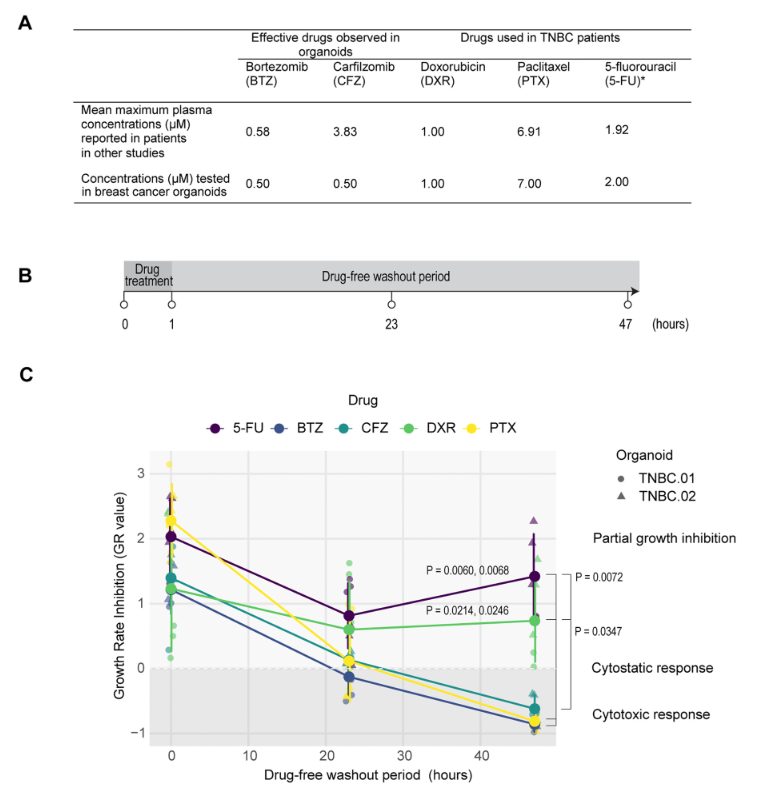
图 6:药物响应动态对比
内容:表格列出 BTZ、CFZ 与传统化疗药(DXR、PTX、5-FU)的血浆浓度;示意图展示给药 1 小时后 0、23、47 小时的洗脱期设计;GR 值曲线显示 DXR 和 5-FU 处理后 GR 在 47 小时反弹(提示耐药),而 BTZ 和 CFZ 持续保持 GR<0(持续 cytotoxic)。
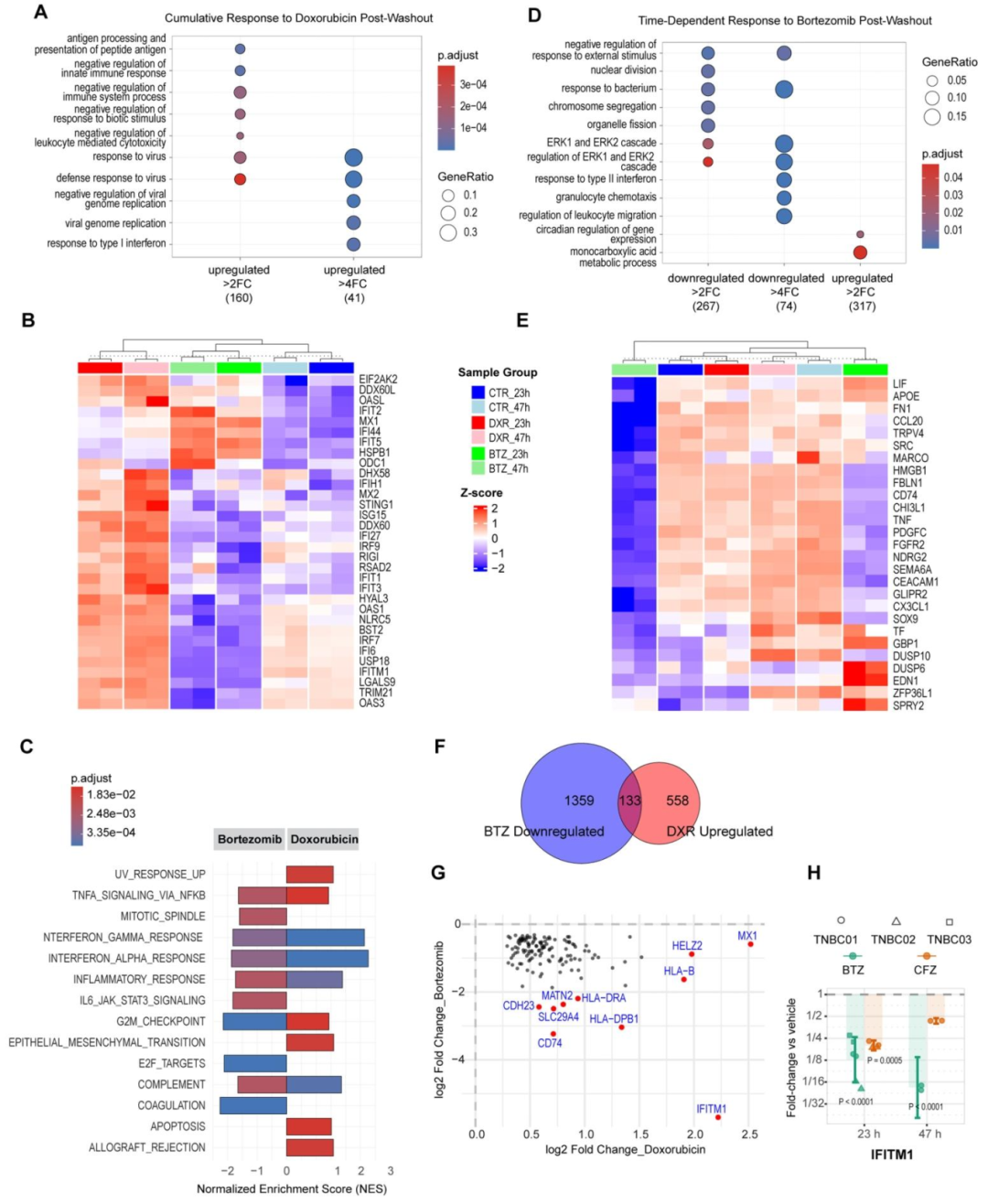
图 7:转录组分析揭示耐药机制及蛋白酶体抑制剂的作用
内容:DXR 处理后富集的 GO terms(如 “病毒应答”“I 型干扰素响应”)及相关基因(STING1、IRF7);GSEA 显示 DXR 激活 TNF-α/NF-κB、炎症反应等通路,而 BTZ 显著抑制这些通路;Venn 图显示 BTZ 下调 133 个 DXR 上调基因(如 IFITM1、CD74),RT-qPCR 验证 IFITM1 在洗脱期的表达显著降低(P<0.0001)。
本研究利用 TNBC 患者来源类器官(源自化疗耐药残留肿瘤)进行高通量药物筛选,发现蛋白酶体抑制剂(BTZ、CFZ)是克服化疗耐药的有效药物。其机制包括:下调核糖体蛋白抑制蛋白质合成、干扰细胞周期(G2/M 或 S 期阻滞),并通过抑制 TNF-α/NF-κB 和 I 型干扰素通路逆转炎症驱动的耐药。该研究证实类器官模型在药物重定位中的价值,为 TNBC 耐药患者提供了新的治疗方向,但需解决蛋白酶体抑制剂的肿瘤穿透性和临床分层问题,未来可结合生物标志物(如 STING 通路激活)开展亚型特异性临床试验。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
下一篇:MeCP2 失调通过抑制线粒体自噬损害皮质类器官神经发育的研究