常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-01-05 17:22:54 细胞资源库平台 访问量:250
胶质瘤是恶性程度高、预后极差的脑肿瘤,现有研究模型(如细胞系、患者来源异种移植模型)难以精准模拟肿瘤微环境(包括免疫细胞、基质细胞及细胞间互作),限制了对其发病机制的理解和治疗方案的开发。传统模型要么缺乏肿瘤异质性,要么无法保留免疫成分,导致药物筛选和疗效预测准确性不足。因此,构建能忠实再现胶质瘤微环境的体外模型,对个性化治疗和基础研究至关重要。
来自北京天坛医院、首都医科大学的团队在《Bioactive Materials》期刊发表了题为“A novel organoid model retaining the glioma microenvironment for personalized drug screening and therapeutic evaluation”的研究。
新型胶质瘤类器官模型(GlioME)的构建:
方法:将新鲜胶质瘤组织机械切碎(避免单细胞解离破坏细胞间连接),接种到低生长因子 Matrigel 中,采用无血清培养基培养,无需添加外源性生长因子(如 EGF、bFGF);
优势:成功率达 88.2%(34 例中 30 例成功),高于漂浮培养类器官(FG)的 76.5%,且能覆盖不同亚型(少突胶质细胞瘤、星形细胞瘤、胶质母细胞瘤)及 WHO 分级,包括 IDH 突变型和复发肿瘤。
模型验证:
分子一致性:通过 RNA 测序、全外显子测序、DNA 甲基化分析,证实 GlioME 与原发肿瘤在基因表达、突变谱、拷贝数变异及甲基化模式上高度一致(相关系数 > 0.89);
微环境保留:免疫荧光和流式细胞术显示,GlioME 较漂浮类器官保留更多肿瘤相关巨噬细胞(CD45+/CD68+)、T 细胞(CD4+/CD8+)等免疫细胞,更接近体内肿瘤免疫微环境。
临床应用:
药物筛选:GlioME 对化疗药(替莫唑胺)、靶向药(vebreltinib,MET 抑制剂)及免疫调节剂(pexidartinib,CSF1R 抑制剂)表现出剂量依赖性响应;
个性化治疗预测:成功预测 1 例 MET 扩增的复发星形细胞瘤患者对 vebreltinib 的临床响应,治疗后 MRI 显示残余病灶消失,证实模型的临床转化价值。
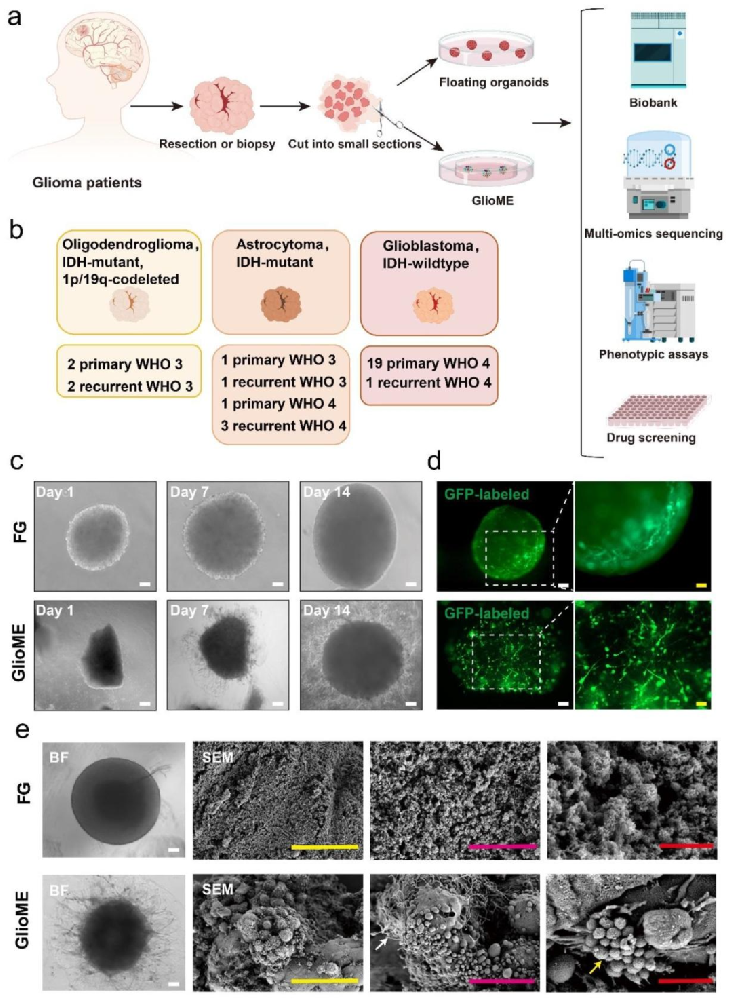
图 1:GlioME 的构建与形态特征
内容:展示 GlioME 与漂浮类器官(FG)的构建流程,显示 GlioME 通过机械切碎组织、Matrigel 包埋培养,而 FG 采用悬浮培养;呈现不同时间点(1 天、7 天、14 天)的形态,GlioME 沿基质形成触手状结构(体现侵袭性),FG 表面更光滑;通过 GFP 标记和扫描电镜(SEM)显示 GlioME 内部细胞互作更复杂,含肿瘤相关巨噬细胞和外泌体。
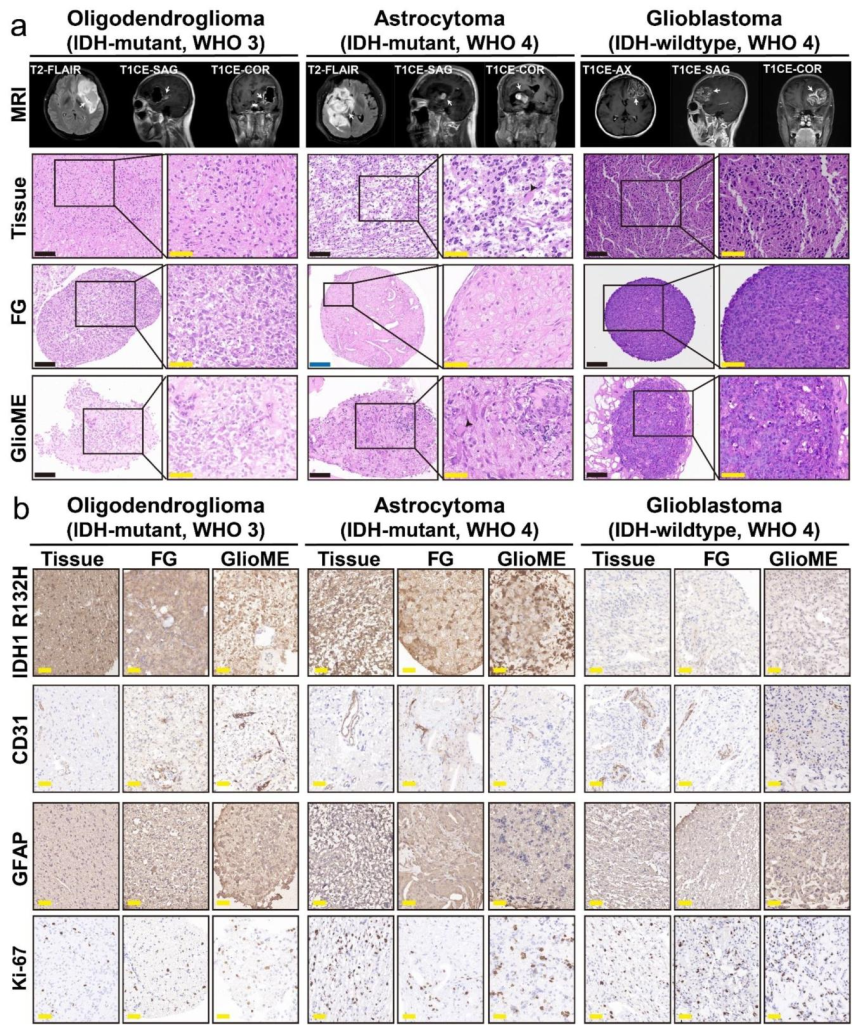
图 2:组织学与标志物一致性
内容:对比原发肿瘤与两种类器官的 HE 染色,GlioME 在 IDH 突变型星形细胞瘤中更易保留多核瘤细胞特征,而 FG 存在细胞组成偏差;免疫荧光显示 IDH1 R132H、GFAP、CD31(血管内皮)、Ki-67(增殖)等标志物在 GlioME 中与原发肿瘤表达模式一致。
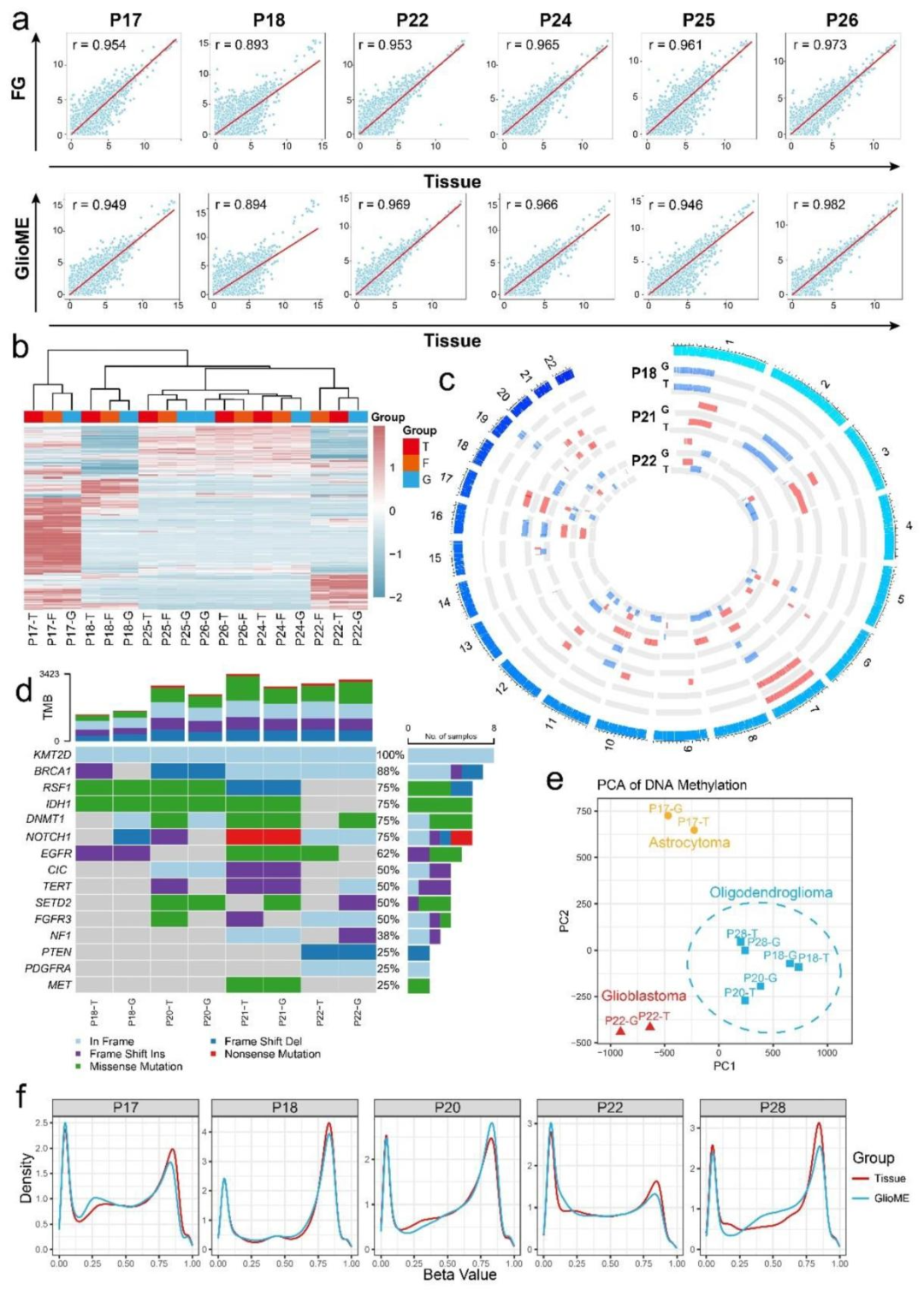
图 3:分子水平一致性验证
内容:RNA 测序相关性分析显示 GlioME 与原发肿瘤基因表达相关系数 > 0.95;全外显子测序证实两者拷贝数变异(CNV)和突变谱(如 KMT2D、NOTCH1 突变)高度相似;DNA 甲基化主成分分析(PCA)显示同亚型 GlioME 与肿瘤组织聚类,甲基化 β 值分布一致。
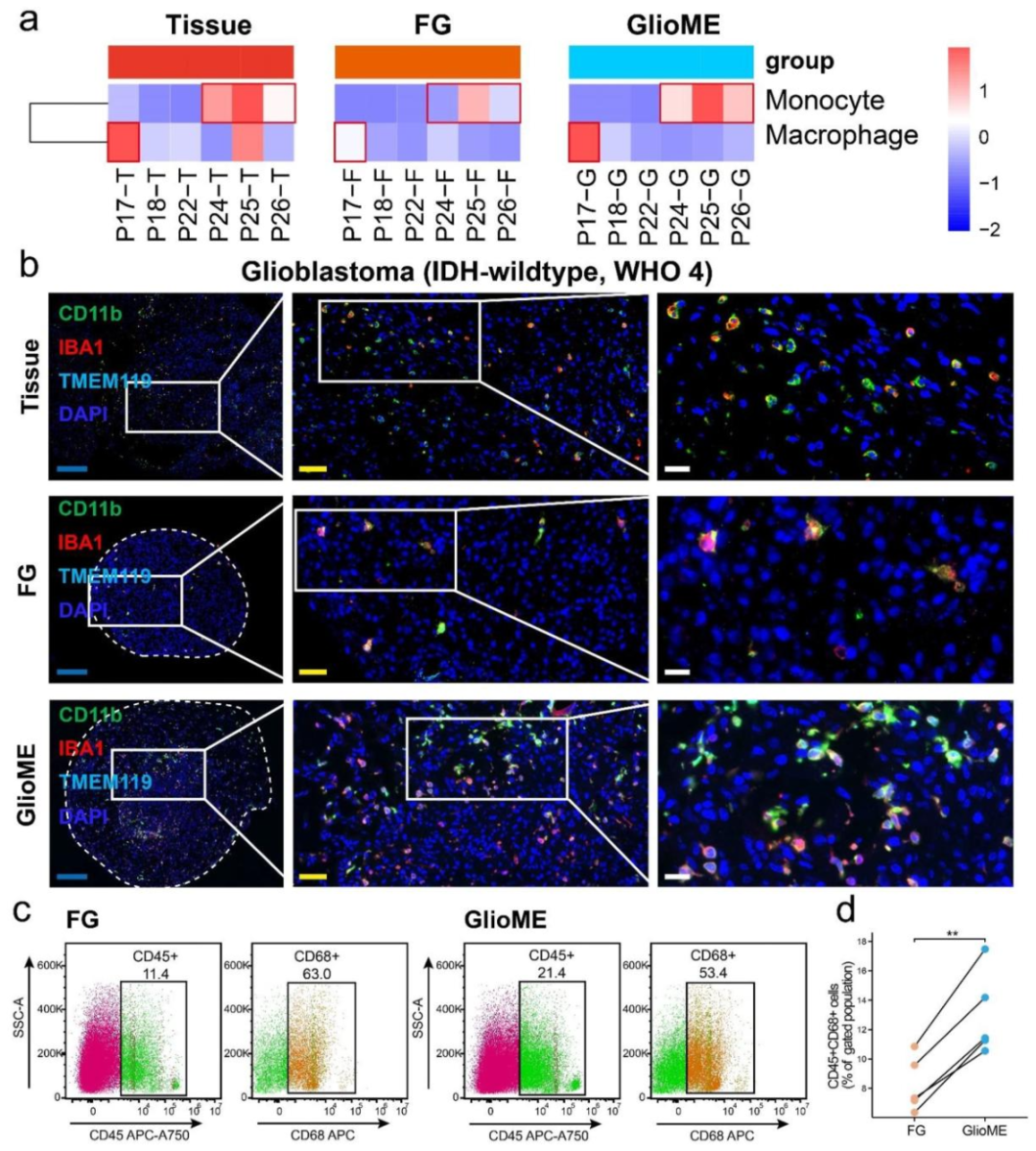
图 4:巨噬细胞保留能力
内容:CIBERSORT 算法分析显示 GlioME 中巨噬细胞比例更接近原发肿瘤;免疫荧光标记 CD11b、IBA1、TMEM119,证实 GlioME 巨噬细胞数量显著多于 FG;流式细胞术显示 GlioME 中 CD45+/CD68 + 巨噬细胞数量约为 FG 的 2 倍。
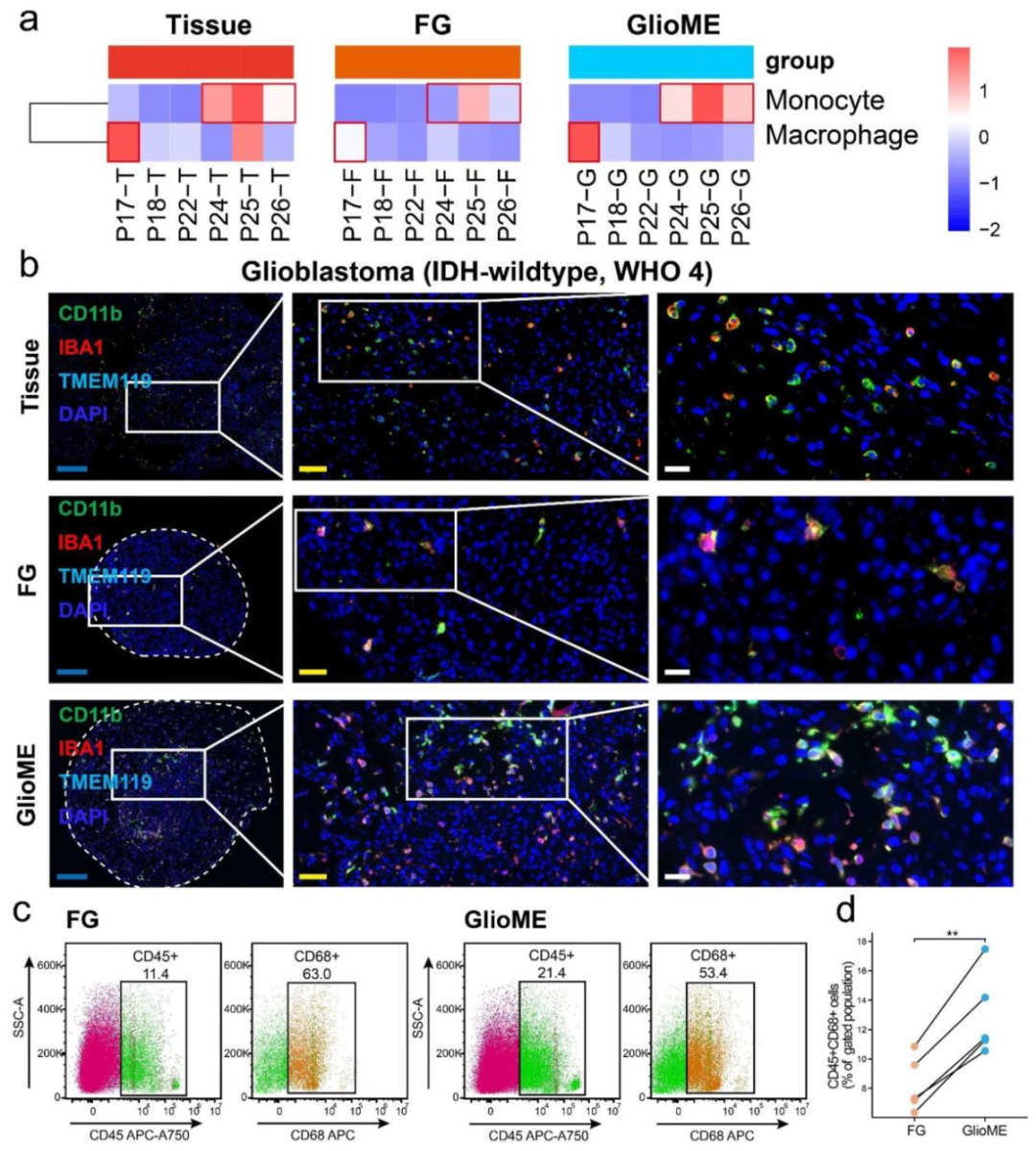
图 5:T 细胞保留能力
内容:ssGSEA 分析显示 GlioME 中 T 细胞相关通路(如 IFNG、GZMA 表达)更接近原发肿瘤;免疫荧光显示 GlioME 保留更多 CD4 + 和 CD8+ T 细胞;流式细胞术证实 GlioME 中 CD45+/CD3+ T 细胞比例显著高于 FG(P=0.0476)。
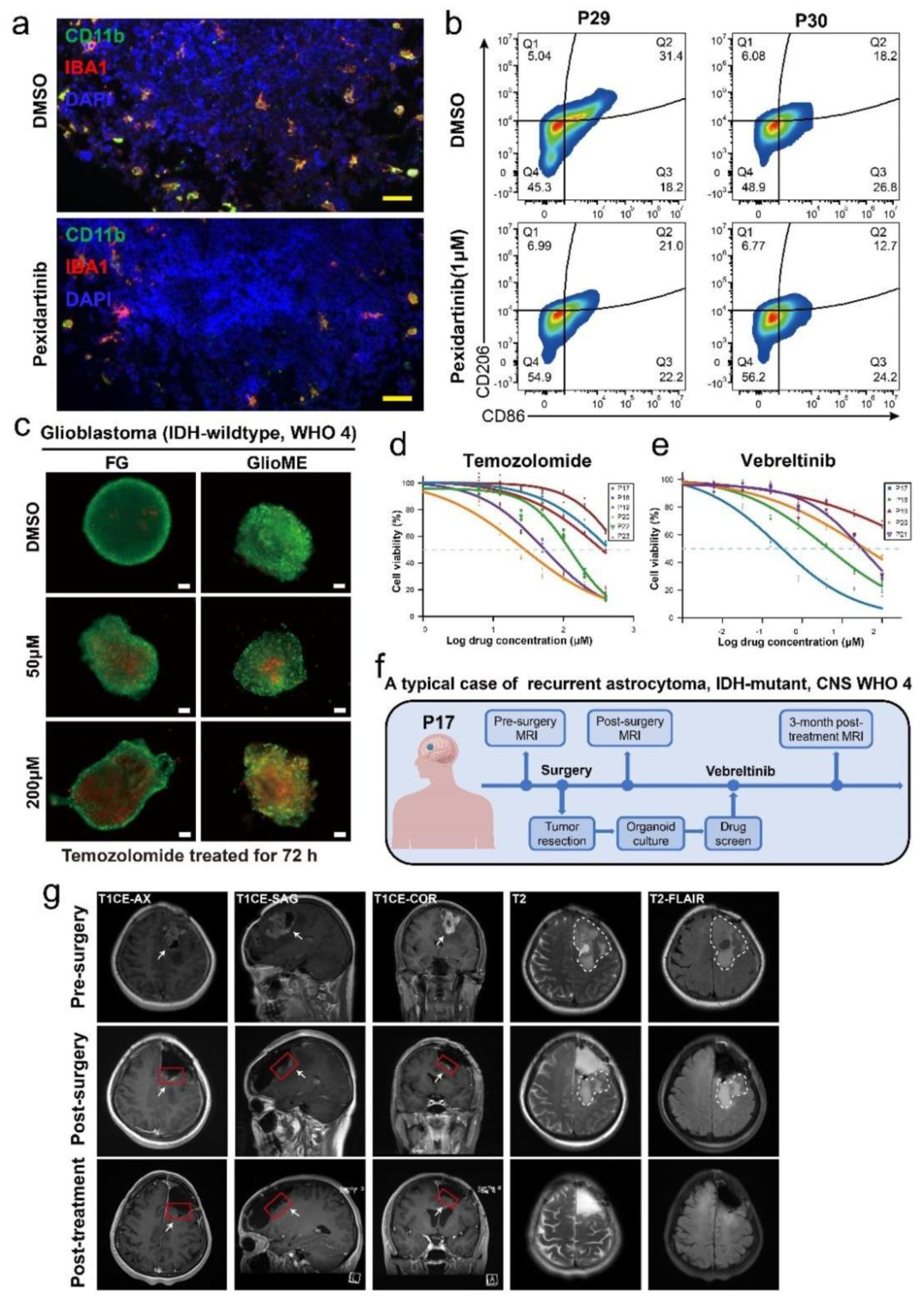
图 6:药物筛选与临床验证
内容:Pexidartinib 处理后,GlioME 中巨噬细胞数量减少,CD206+ M2 型巨噬细胞比例下降;替莫唑胺和 vebreltinib 处理显示剂量依赖性存活曲线;1 例 MET 扩增患者的 GlioME 对 vebreltinib 敏感,临床治疗后 MRI 显示病灶消失,验证模型预测价值。
本研究构建的 GlioME 模型通过机械切碎组织、Matrigel 包埋培养,成功保留了胶质瘤的微环境(尤其是免疫细胞)和分子特征,解决了传统模型无法兼顾肿瘤异质性与免疫成分的问题。该模型在药物筛选中表现出可靠的剂量响应,并能准确预测患者对靶向药的临床响应,为个性化治疗提供了理想平台。当前挑战包括血管化模拟不足(仅保留内皮细胞无血管腔),未来需优化培养系统以延长存活时间、整合血管网络,进一步提升模型的生理相关性。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:ActRII 或 BMPR 配体抑制骨骼肌成肌细胞分化,且 BMPs 促进小鼠骨骼肌异位骨化