常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-12-05 09:00:18 细胞资源库平台 访问量:195
检测细胞株广泛应用于药物发现、抗体开发、基因研究和毒性评估等领域。基于D-Luciferase的报告基因细胞株及其荧光素酶检测方法在药物初筛/复筛、表位竞争、药物生物活性检测等多方面展现了广泛的应用潜力。报告基因法已被药典收录,为国家认可的检测方法。报告基因细胞株多用于监测特定的生物过程或信号通路。
HEK293细胞因子报告基因细胞株是以HEK293为工具细胞,采用慢病毒感染的方式构建,不仅能够稳定表达细胞因子受体蛋白,并且能够表达荧光素酶报告基因,是基于转录因子信号通路构建的荧光素酶报告基因细胞系。当细胞因子结合受体蛋白后,细胞因子与受体蛋白相互作用,激活转录因子信号通路,从而激活荧光素酶的表达。荧光信号的强弱即代表信号通路的激活效果,因此可用于相关药物的体外效果评价,筛选抗体以及筛选信号通路的激活剂或抑制剂。
英文标题:Sprouty2 suppresses progression and correlates to favourable prognosis of intrahepatic cholangiocarcinoma via antagonizing FGFR2 signalling
中文标题:Sprouty2 通过拮抗 FGFR2 信号抑制肝内胆管癌进展并关联良好预后
发表期刊:《Journal of Cellular and Molecular Medicine》
影响因子:4.2
作者单位:
1. Department of General Surgery, Qilu Hospital of Shandong University, Jinan, China
2. Department of Pharmacology & Chemical Biology, University of Pittsburgh, Pittsburgh, Pennsylvania
3. Department of Emergency Medicine and Chest Pain Center, Qilu Hospital of Shandong University, Jinan, China
4. Department of Pathology, Qianfoshan Hospital of Shandong University, Jinan, China
5. Department of Radiation Oncology, Shandong Cancer Hospital Affiliated to Shandong University, Jinan, China
作者信息:
Yun-Fei Xu¹, Hong-Da Liu², Zeng-Li Liu¹, Chang Pan³, Xiao-Qing Yang⁴, Shang-Lei Ning¹, Zong-Li Zhang¹, Sen Guo¹*, Jin-Ming Yu⁵*
肝内胆管癌(ICC)发病率呈上升趋势,FGFR2 信号通路异常激活(如融合突变)是其进展和不良预后的关键驱动因素,相关抑制剂已进入临床研究。Sprouty(SPRY)家族是 FGFR 信号的经典负反馈抑制剂,其中 SPRY2 可通过抑制 ERK 磷酸化调控肿瘤进展,但在 ICC 中的表达、临床意义及作用机制尚未明确。本研究旨在探讨 SPRY 家族在 ICC 中的表达特征,明确 SPRY2 的预后价值及通过拮抗 FGFR2 信号抑制 ICC 进展的分子机制。
本研究经山东大学齐鲁医院伦理委员会批准,纳入 108 例 ICC 手术患者石蜡包埋组织(含完整随访数据,无术前放化疗史)及 20 对新鲜肿瘤 / 癌旁组织;采用 qPCR 检测新鲜组织中 SPRY1-4 mRNA 表达,免疫组化(IHC)分析石蜡组织中蛋白表达并确定临界值(SPRY2 为 4.5);Kaplan-Meier 法和 Cox 回归分析 SPRY2 的预后价值;Chi-square 检验分析其与临床病理特征的关联。体外实验采用 ICC 细胞系(RBE、HuCCT1、HCCC9810),通过 siRNA 沉默 SPRY2/FGFR2、过表达 SPRY2-WT(野生型)或 SPRY2-Y55F(磷酸化位点突变体),结合 FGF1 刺激和 FGFR2 抑制剂 AP24534,通过 Western blot 检测 ERK 磷酸化及 EMT 标志物(E-cadherin、Snail、Slug)表达,划痕愈合实验和 Transwell 实验检测细胞迁移侵袭能力。
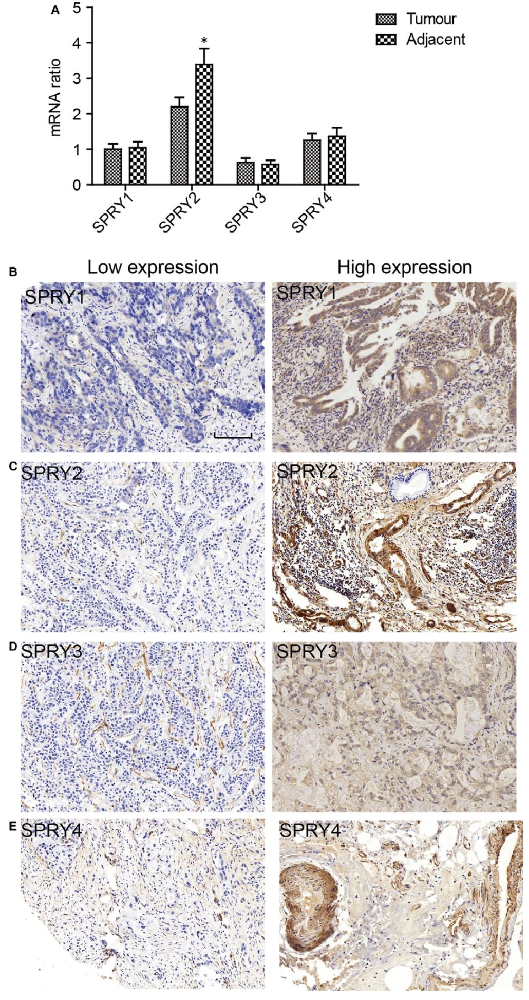
图1:SPRY 家族在 ICC 中的表达特征
该图显示 SPRY2 的表达差异:qPCR 结果显示,20 对新鲜组织中,SPRY2 在癌旁组织的 mRNA 水平显著高于肿瘤组织,且表达量高于其他 SPRY 家族成员(图 1A);IHC 结果显示,SPRY1-4 主要定位于 ICC 细胞胞质,根据 ROC 曲线确定的临界值可分为低表达和高表达两组(图 1B-E),提示 SPRY2 可能具有抑癌潜力。
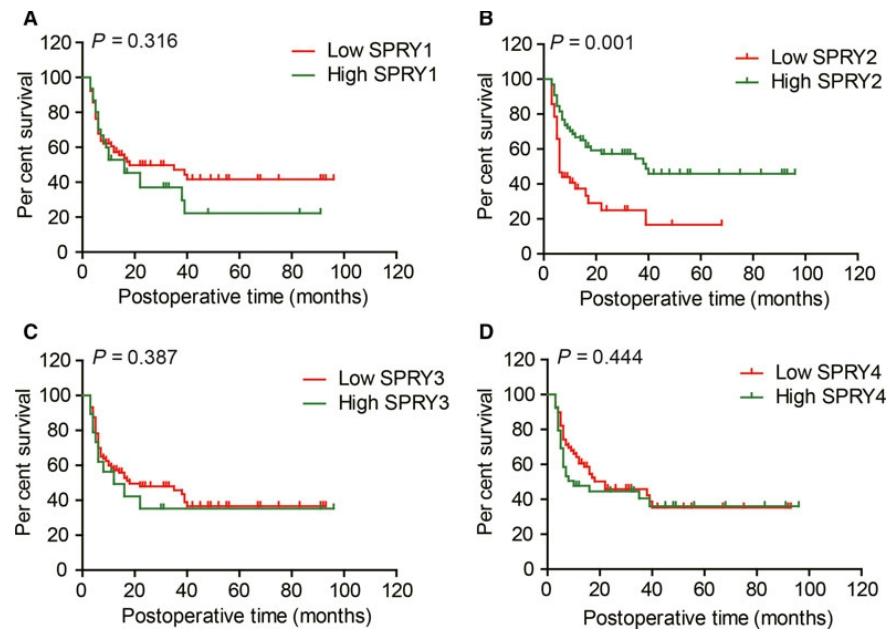
图2:SPRY 家族与 ICC 患者预后的关联
该图证实 SPRY2 的预后价值:Kaplan-Meier 生存分析显示,仅 SPRY2 高表达与 ICC 患者更长总生存期显著相关(P=0.001),高表达组 3 年生存率(54.5%)远高于低表达组(16.6%)(图 2B);而 SPRY1、SPRY3、SPRY4 的表达与患者预后无显著关联(P>0.3,图 2A、C、D)。
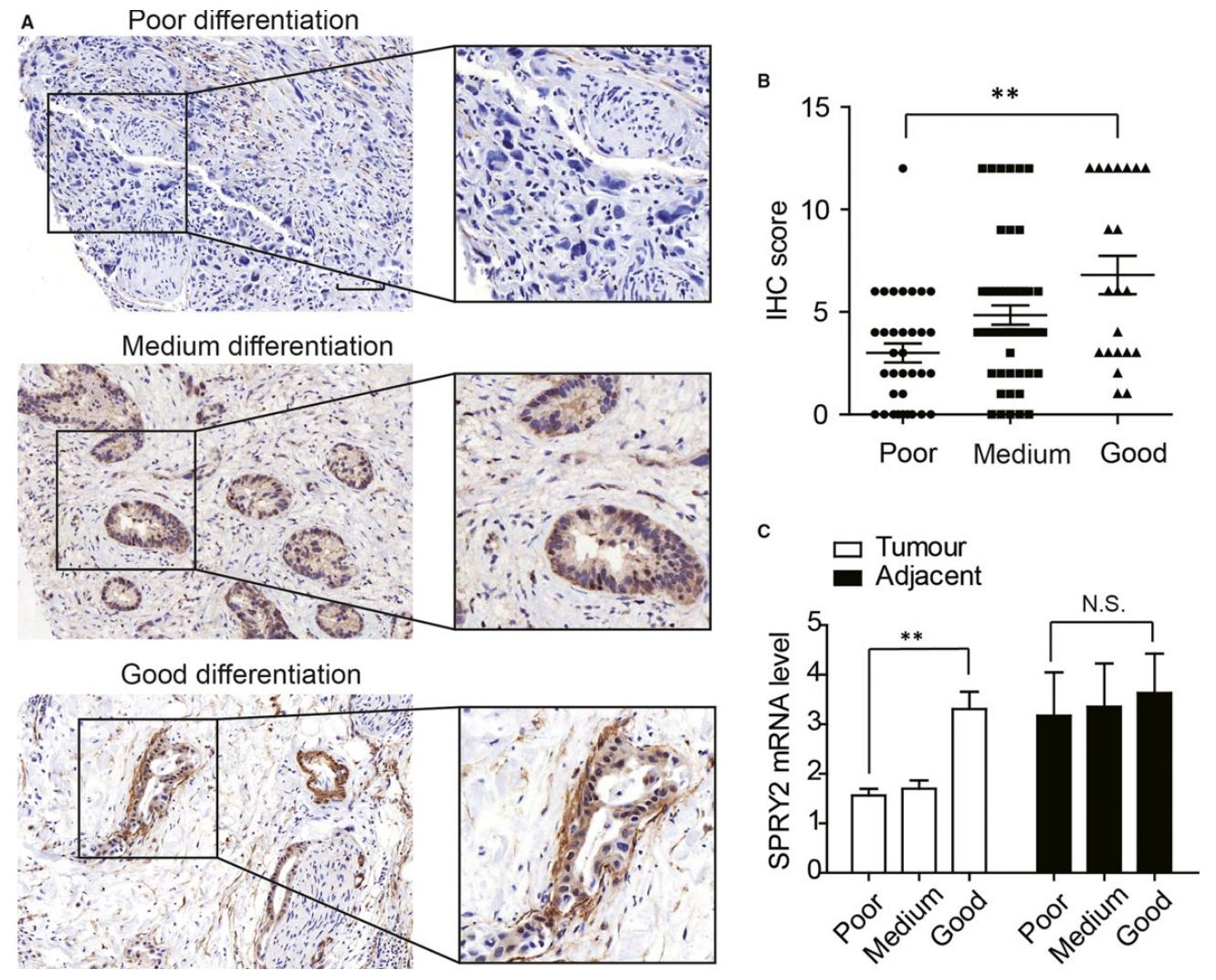
图3:SPRY2 表达与 ICC 分化程度的关联
该图明确 SPRY2 与分化的相关性:IHC 结果显示,高分化 ICC 组织中 SPRY2 表达显著高于低分化组织(图 3A-B);新鲜组织 qPCR 验证,低分化 ICC 的 SPRY2 mRNA 水平显著低于高分化组织,而癌旁组织中 SPRY2 表达无分化相关差异(图 3C),提示 SPRY2 可能参与调控 ICC 细胞分化过程。
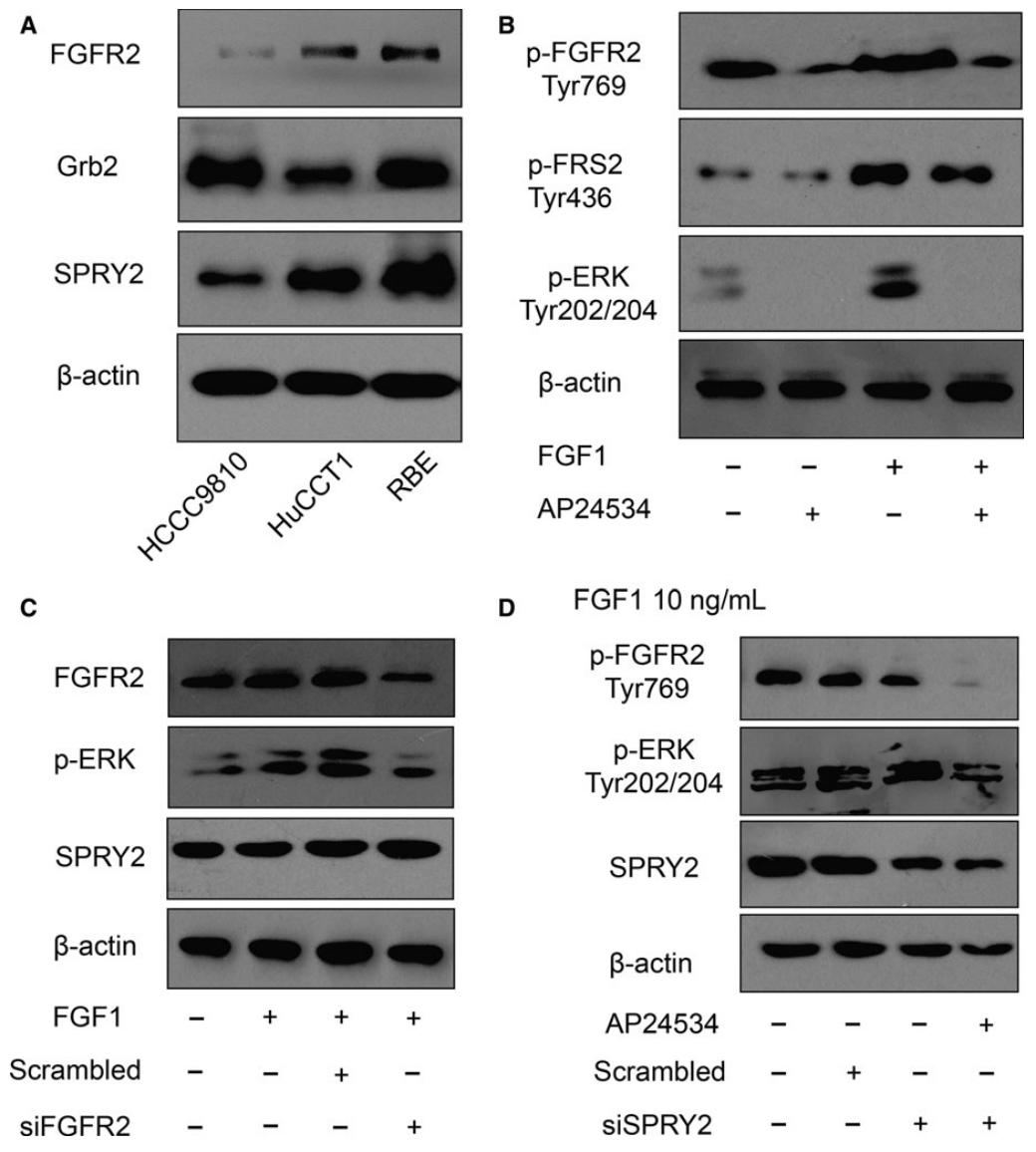
图4:SPRY2 抑制 FGFR2 诱导的 ERK 磷酸化
该图揭示核心信号调控机制:RBE 细胞中 SPRY2 和 FGFR2 基础表达较高(图 4A);FGF1 刺激可诱导 FGFR2、FRS2 及 ERK 磷酸化,而 FGFR2 抑制剂 AP24534 可阻断该效应(图 4B);siRNA 沉默 FGFR2 可抑制 FGF1 诱导的 ERK 磷酸化(图 4C);沉默 SPRY2 则显著增强 FGFR2 介导的 ERK 磷酸化,且 AP24534 可逆转该效应(图 4D),证实 SPRY2 通过拮抗 FGFR2 信号抑制 ERK 激活。
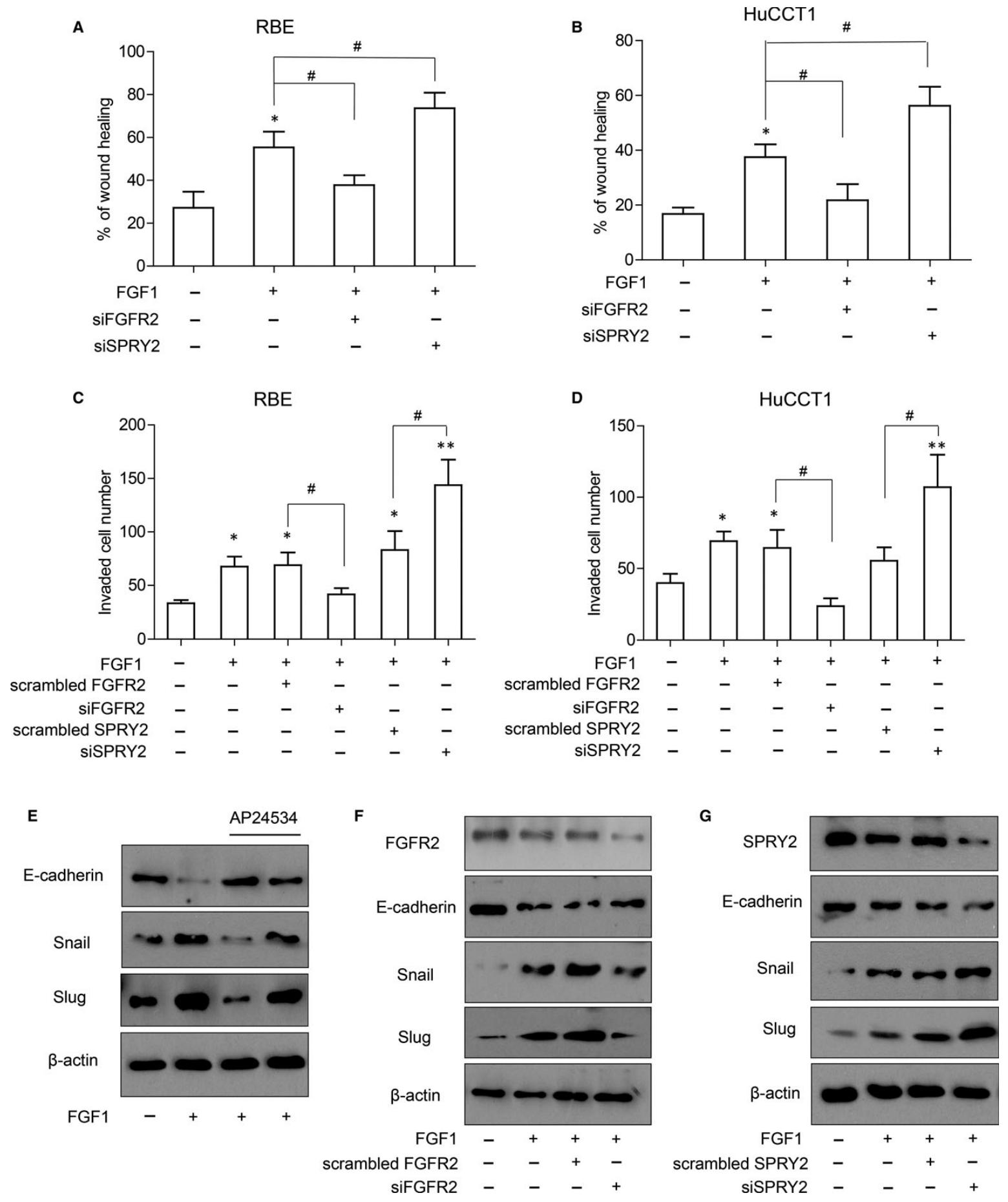
图5:SPRY2 抑制 FGFR2 诱导的 ICC 细胞迁移侵袭及 EMT
该图验证 SPRY2 的功能作用:划痕愈合实验显示,沉默 SPRY2 可促进 RBE 和 HuCCT1 细胞迁移,沉默 FGFR2 则抑制迁移(图 5A-B);Transwell 实验显示,FGF1 刺激增强细胞侵袭,沉默 FGFR2 可减弱侵袭,沉默 SPRY2 则促进侵袭(图 5C-D);Western blot 显示,FGF1 诱导 EMT(E-cadherin 下调,Snail/Slug 上调),沉默 FGFR2 可阻断 EMT,沉默 SPRY2 则增强 EMT(图 5E-G),表明 SPRY2 通过抑制 FGFR2 信号抑制 ICC 细胞侵袭和 EMT 进程。
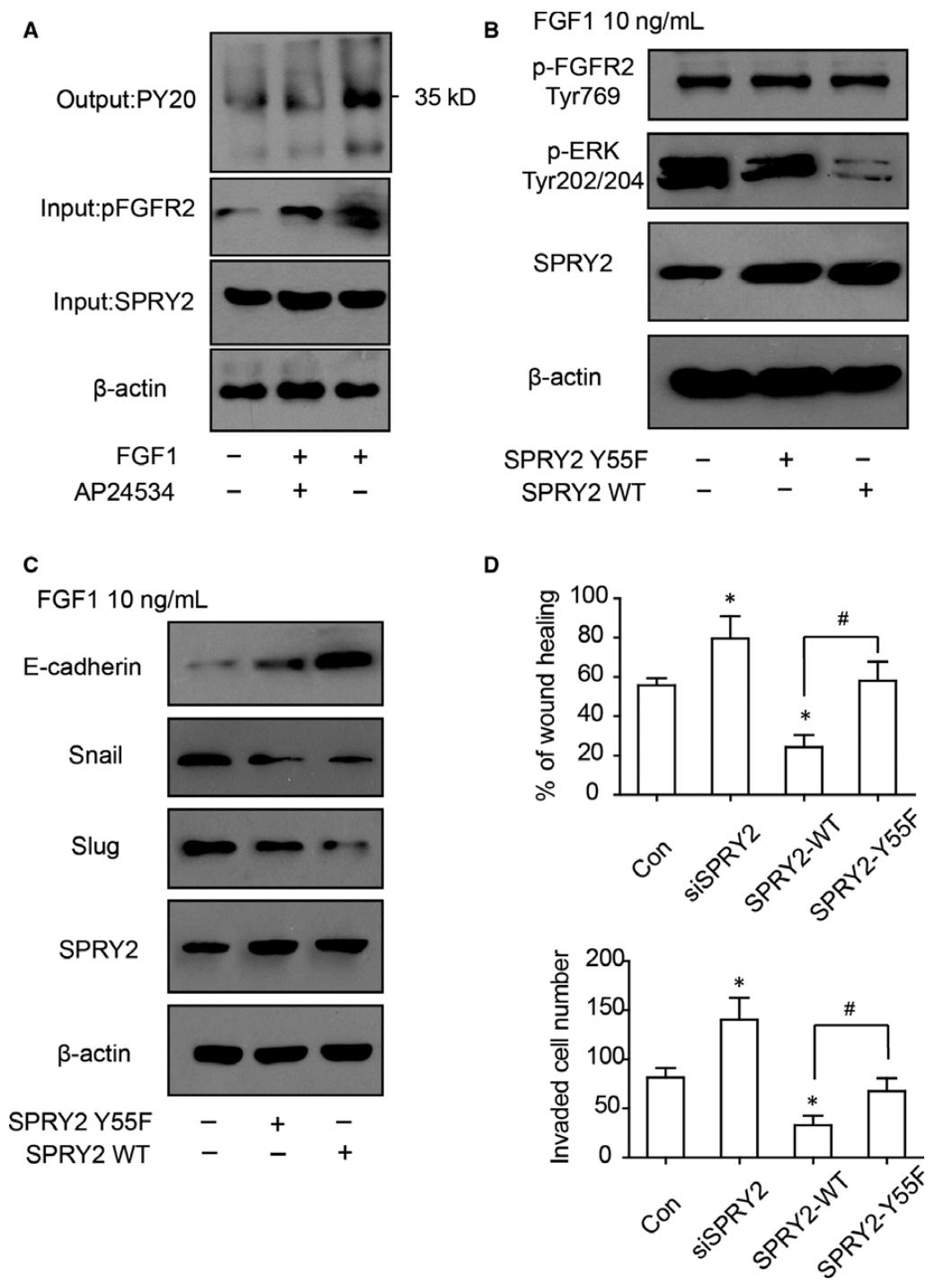
图6:SPRY2-Y55 磷酸化对其抑癌功能至关重要
该图明确关键磷酸化位点:免疫沉淀实验显示,FGF1 刺激可增强 SPRY2 磷酸化,AP24534 可抑制该效应(图 6A);过表达 SPRY2-Y55F(酪氨酸 55 突变体)的 RBE 细胞,ERK 磷酸化水平显著高于过表达 SPRY2-WT 的细胞(图 6B);SPRY2-Y55F 突变体无法有效抑制 EMT(图 6C),且对细胞迁移和侵袭的抑制作用显著弱于 SPRY2-WT(图 6D-E),证实 Y55 磷酸化是 SPRY2 发挥抑癌功能的必需位点。
本研究首次明确 SPRY2 在 ICC 中的抑癌作用及分子机制:SPRY2 是 ICC 独立良好预后标志物,其高表达与肿瘤高分化、低淋巴结转移及更长生存期显著相关;SPRY2 通过拮抗 FGFR2 信号通路,抑制 ERK 磷酸化、细胞迁移侵袭及 EMT 进程,且该功能依赖其 Y55 位点的磷酸化;SPRY1、SPRY3、SPRY4 在 ICC 中无显著预后价值,提示 SPRY 家族成员在 ICC 中存在功能特异性。研究结果拓展了 FGFR2 信号通路在 ICC 中的调控网络,为 ICC 靶向治疗提供新方向 —— 通过激活 SPRY2 或靶向其下游信号分子,可能成为 FGFR2 抑制剂之外的备选策略。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:星形胶质细胞通过 Cx47/Chi3l1 轴促进少突胶质前体细胞增殖的机制研究
下一篇:胃部类器官模型揭示幽门螺杆菌感染中的细胞类型特异性宿主-病原互作