常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-12-04 09:12:50 细胞资源库平台 访问量:230
传统肝脏体外模型因缺乏细胞互作、细胞密度不足或与临床检测脱节,难以精准模拟体内生理功能,导致毒理学评估准确性受限。来自斯洛文尼亚马里博尔大学医学部的 Eneko Madorran 团队(通讯作者:eneko.madorran@um.si)在《Current Protocols》(2025, 5:e70172)发表研究,构建了一种新型肝脏细胞培养系统:以 96 孔板为载体,共培养肝细胞(Hepatocytes)与肝脏非实质细胞(NPCs,含肝血窦内皮细胞、肝星状细胞、库普弗细胞),并整合临床生化分析仪(Cobas C111)和膜电位细胞活力检测(MPCVA)技术。该系统可复现体内葡萄糖 - 甘油三酯动态平衡,精准响应布洛芬(IBU)、利福平(RIF)等肝毒性药物的生理效应,显著提升肝脏模型的生理相关性与转化潜力,为肝脏(病理)生理研究及毒理学评估提供了可靠工具。
本研究旨在解决传统肝脏体外模型与体内微环境差异大、基础研究与临床应用脱节的问题,建立一种能精准模拟体内肝脏功能的新型培养系统。
1. 配制含脂肪酸、维生素和氨基酸的专用 Hep 培养基,支持多细胞共培养;
2. 采用 96 孔板共培养肝细胞与 NPCs,构建多细胞互作微环境;
3. 利用 Cobas C111 临床生化分析仪检测葡萄糖、甘油三酯、白蛋白等临床相关 biomarkers;
4. 通过 MPCVA 方法结合 ImageStream 成像流式细胞仪(ISX)评估细胞活力与周期。
结果显示,该系统可形成类肝脏小叶结构,复现体内代谢动态,且能特异性响应肝毒性药物,biomarkers 水平与临床诊断标准一致,为肝脏转化研究搭建了 “基础 - 临床” 桥梁。
肝脏作为代谢与毒理学评估的核心器官,其体外模型需精准复现细胞互作、代谢通路及生理响应。然而,现有模型存在显著局限:2D 肝细胞模型虽用原代细胞(“金标准”),但寿命短且缺乏非实质细胞,无法模拟细胞间调控;肝脏器官芯片(OOC)虽能模拟微环境,但细胞数量少、密度低,与体内状态差距大; spheroid 模型细胞量多于 OOC,但核心细胞易因营养不足失活,且整体密度仍低于天然肝脏。
更关键的是,基础研究聚焦分子机制(如葡萄糖代谢通路),而临床研究关注生理指标(如血糖水平),这种目标与方法的脱节导致预临床数据难以转化。本研究通过整合多细胞共培养与临床仪器,首次实现 “体外模型 biomarkers 与临床诊断标准对齐”,填补了传统模型的转化空白。
图 1:新型肝脏细胞培养系统实验流程
该图展示从细胞准备到功能分析的完整流程:1. 分别培养原代肝细胞与 NPCs(非实质细胞);2. 消化后按比例(肝细胞:NPCs=4:1)接种于 96 孔板共培养;3. 倒置显微镜观察细胞形态与自组装结构;4. 收集上清用 Cobas C111 检测生化指标;5. 采用 MPCVA 方法结合 ISX 评估细胞活力。流程设计核心是通过 “单独培养 - 共培养 - 双维度检测(形态 + 生化)”,确保模型的结构与功能一致性。
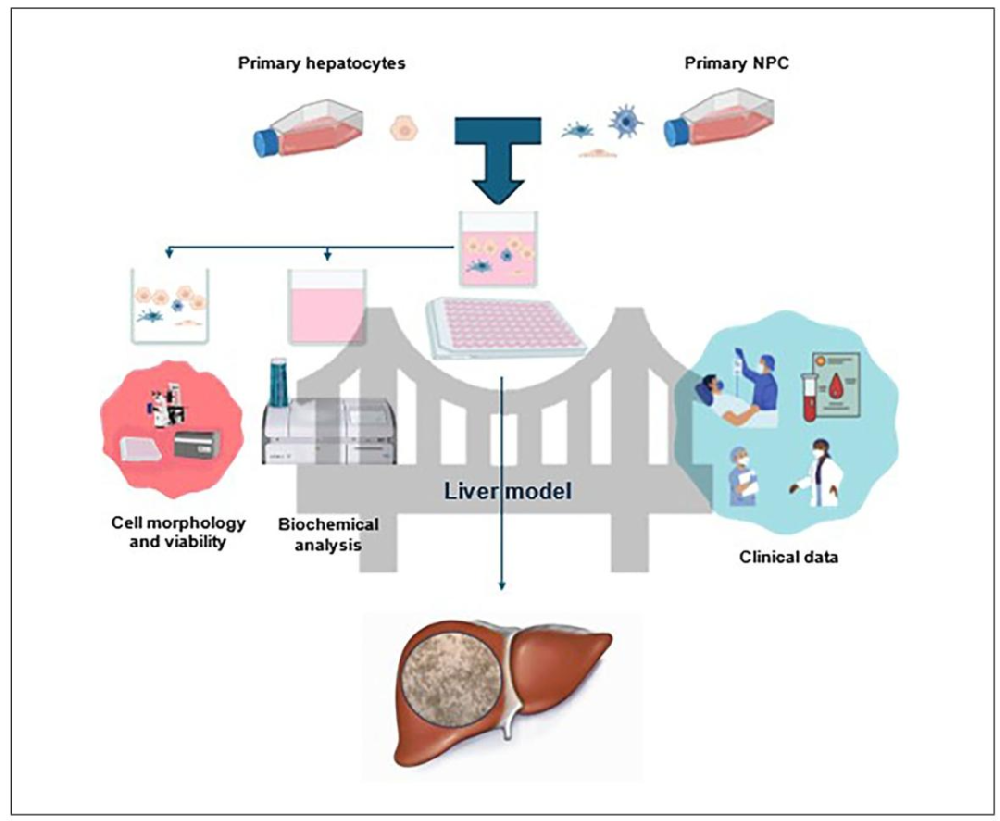
图 2:NPCs 在 Hep 培养基中形成小叶样结构
该图显示 NPCs 的培养特征:NPCs 在 Hep 培养基中培养 7 天后,可自发形成类似体内肝脏的小叶样结构(lobule-like structures),倒置显微镜下可见细胞有序排列,无明显团聚或凋亡。这一结构是肝脏微环境的关键特征,为后续与肝细胞共培养奠定了 “结构基础”,且无需额外添加细胞外基质(ECM)—— 研究证实肝星状细胞可自主合成足量 ECM,外源性 ECM 反而可能干扰细胞天然生化过程。
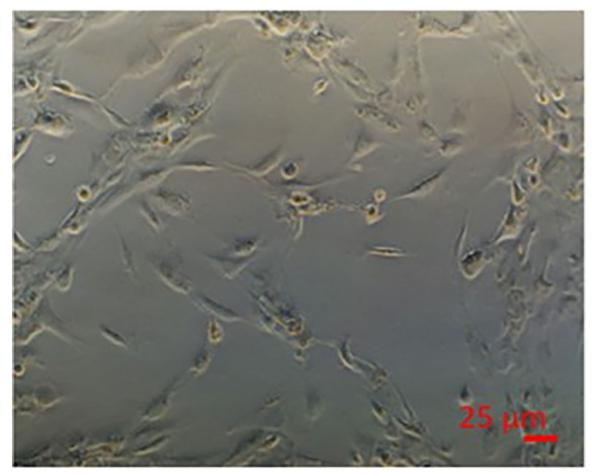
图 3:肝细胞与 NPCs 共培养的自组装结构
该图展示共培养体系的细胞排列:肝细胞与 NPCs 接种后,可自主组装为类似体内肝脏的结构化布局(structured arrangements),而非随机分布。这种自组装依赖细胞间信号互作(如 NPCs 分泌的细胞因子调控肝细胞极性),是模型能复现体内代谢功能的核心前提。研究指出,若细胞未形成该结构,可能导致葡萄糖 - 甘油三酯动态平衡异常,需调整培养基中脂肪酸浓度或细胞接种比例。
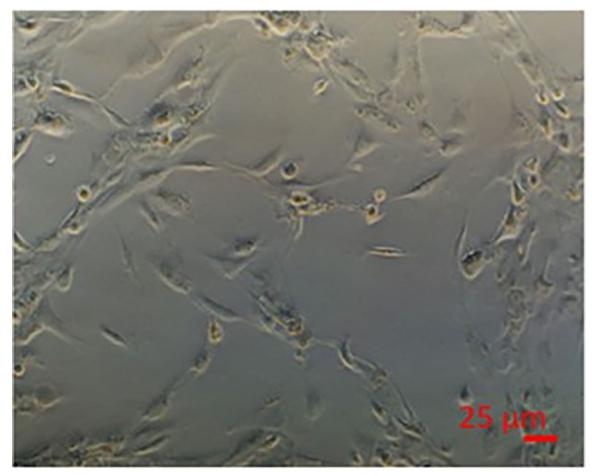
图 4-6:Cobas C111 生化分析仪的样本处理与结果
这组图展示临床生化检测的关键步骤与数据:
Fig.4:Cobas C111 的样本识别界面,需手动录入样本信息(如 “未处理组”“RIF 处理组”),确保检测结果与实验组对应;
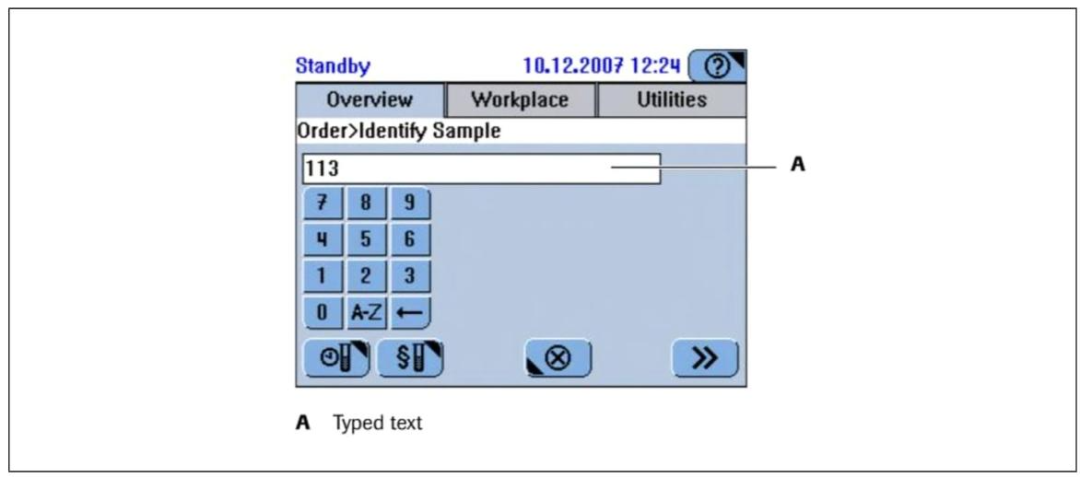
Fig.5:检测项目选择界面,需勾选 ALT(谷丙转氨酶)、AST(谷草转氨酶)、GLU(葡萄糖)、TRIGL(甘油三酯)等肝脏特异性指标,这些指标与临床肝功能诊断完全一致;

Fig.6:典型检测结果,健康模型中葡萄糖与甘油三酯呈负相关(符合体内肝脏代谢规律),而 RIF 处理组甘油三酯显著升高、葡萄糖降低,IBU 处理组则出现 GLU 代谢异常,与体内肝毒性反应一致。
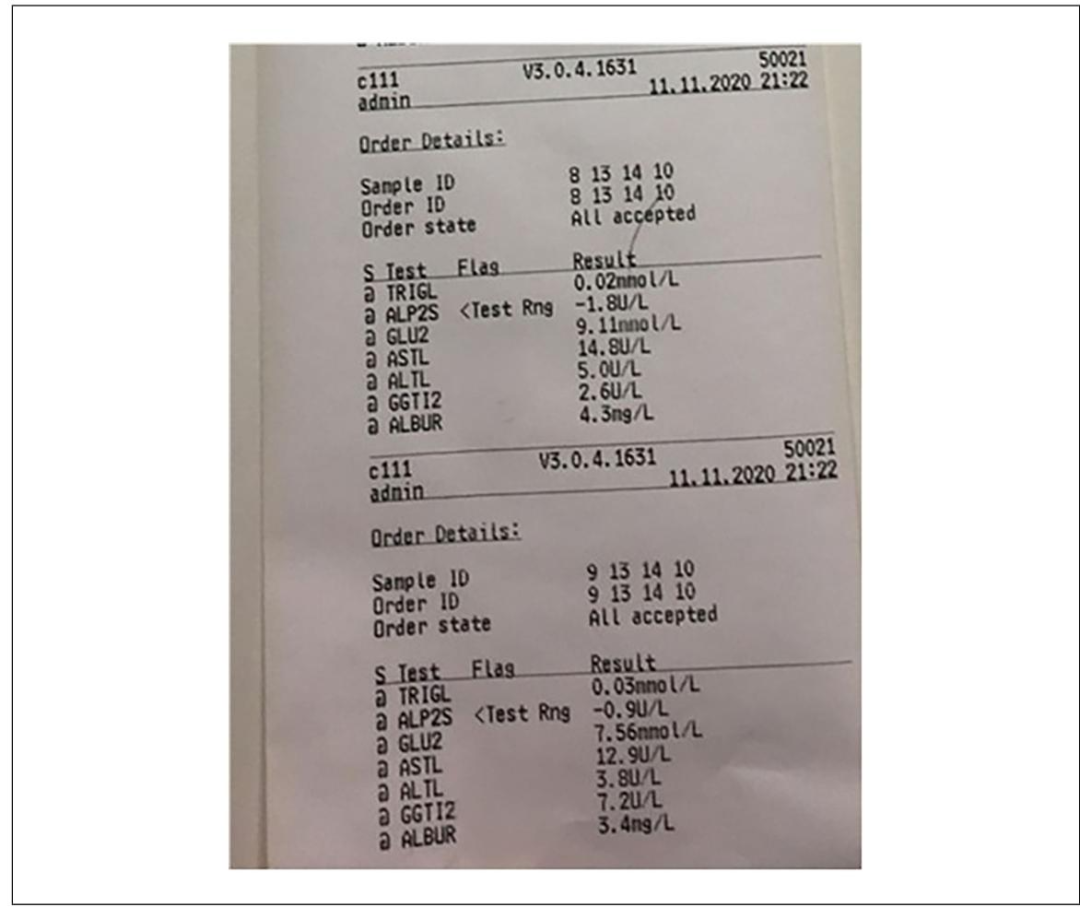
图 7:MPCVA 方法的细胞活力评估结果
该图展示细胞活力检测的判定标准:通过 FluoVolt(膜电位染料,FITC 通道)与 Vybrant(DNA 染料,Texas Red 通道)双染色,结合 ISX 分析:
活细胞判定:FITC 强度 / 细胞大小处于 2.5%-97.5% 分位数之间,且 Texas Red 强度低于 G2/M 期阈值;
死细胞判定:FITC 强度 / 细胞大小低于 2.5% 分位数(低膜电位),或高于 97.5% 分位数且低于 G2/M 期阈值(异常膜电位)。
该方法较传统 MTT 法假阳性率更低,能更精准反映肝毒性药物对细胞活力的影响 —— 如 5 - 氟尿嘧啶(5-FU)处理组死细胞比例达 40% 以上,而未处理组仅 5% 左右。
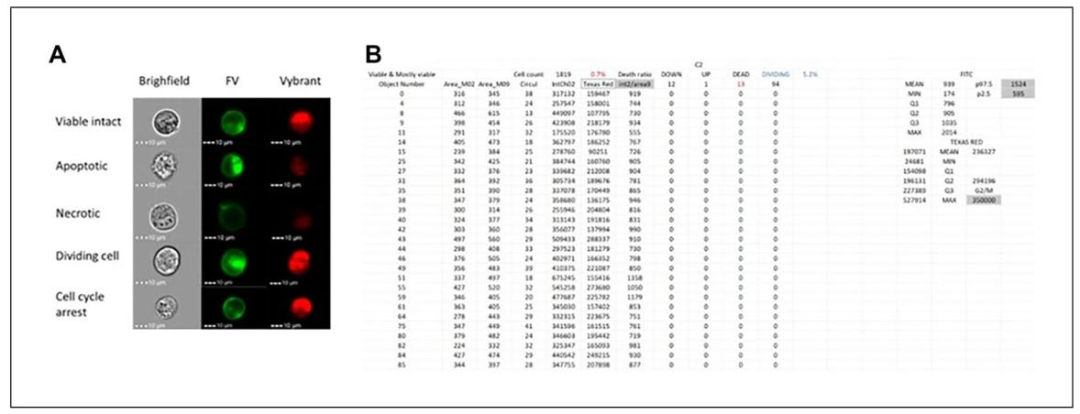
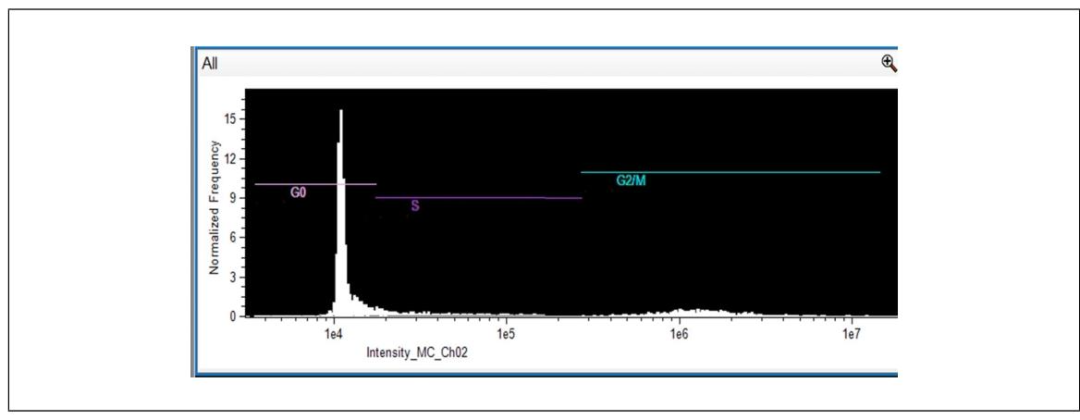
图 8:基于 DNA 染色的细胞周期分析
该图展示细胞周期的流式检测结果:采用膜渗透性 DNA 染料染色后,ISX 可识别 G0/G1 期(低荧光强度,DNA 含量 2n)、S 期(中荧光强度,DNA 复制中)、G2/M 期(高荧光强度,DNA 含量 4n)三个峰。研究指出,肝毒性药物(如 RIF)会导致 G2/M 期细胞比例升高(约 18% vs 未处理组 10%),提示药物干扰细胞分裂,这一结果需结合 MPCVA 活力数据综合解读 —— 避免将 “周期阻滞细胞” 误判为活细胞。
本研究构建的新型肝脏细胞培养系统具有三大核心优势:1. 结构生理化:通过肝细胞与 NPCs 共培养,自发形成类体内小叶结构,无需外源性 ECM;2. 功能临床化:整合 Cobas C111 分析仪,biomarkers(如 GLU、TRIGL)与临床诊断标准一致,解决基础 - 临床脱节问题;3. 应用广泛化:可用于健康肝脏模拟、肝毒性药物筛选(如 IBU、RIF)及 NAFLD/NASH 等病理模型构建(未来拓展方向)。
该系统操作标准化(全程约 1 周),成本可控,可在 96 孔板中实现高通量检测,为肝脏(病理)生理机制研究、药物毒理学评估及转化医学研究提供了可靠且实用的体外模型。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:核糖体显神通!诱导鸡肌细胞 “变身” 又产生长因子,为低成本培养肉铺路
下一篇:星形胶质细胞通过 Cx47/Chi3l1 轴促进少突胶质前体细胞增殖的机制研究