常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-11-23 09:05:55 细胞资源库平台 访问量:271
小胶质细胞过度激活引发的神经炎症是阿尔茨海默病、帕金森病等神经退行性疾病的关键病理机制。来自美国乔治敦大学医学中心的 David J. Loane 团队(Alan I. Faden 为通讯作者)在《The Journal of Biological Chemistry》(2009, 284:15629-15639)发表研究,首次证实激活代谢型谷氨酸受体 5(mGluR5)可通过抑制 NADPH 氧化酶活性,显著降低小胶质细胞的炎症反应及神经毒性 —— 减少诱导型一氧化氮合酶(iNOS)表达、一氧化氮(NO)和肿瘤坏死因子 -α(TNF-α)释放,同时降低活性氧(ROS)生成,最终减轻神经元损伤。该发现为靶向调控小胶质细胞活性、治疗神经炎症相关疾病提供了全新靶点。
本研究旨在阐明 mGluR5 在小胶质细胞激活和神经毒性中的调控作用及分子机制。方法包括:以 BV2 小胶质细胞系和原代皮质小胶质细胞为模型,使用 mGluR5 选择性激动剂 CHPG 预处理,结合 LPS 或 IFN-γ 诱导激活;通过免疫荧光、Western blot 验证 mGluR5 表达及功能;利用 siRNA 敲低 mGluR5、NADPH 氧化酶亚基(p22phox、gp91phox),结合 NO 检测、TNF-α ELISA、ROS 测定及神经毒性实验,解析其作用途径。结果显示,mGluR5 激活可通过抑制 NADPH 氧化酶,减少炎症介质释放和 ROS 生成,显著降低小胶质细胞介导的神经毒性,证实 mGluR5 是调控神经炎症的关键靶点。
小胶质细胞作为中枢神经系统的 resident 免疫细胞,在病原体刺激或组织损伤时过度激活,释放 NO、TNF-α、ROS 等炎症介质,加剧神经元损伤,参与阿尔茨海默病、创伤性脑损伤等疾病的进展。NADPH 氧化酶是小胶质细胞产生 ROS 的核心酶,其活性异常升高是炎症放大的关键驱动因素。
代谢型谷氨酸受体(mGluRs)虽在神经元中研究较多,但在小胶质细胞中的功能尚不明确。已知 Ⅰ 组 mGluRs(mGluR1/5)中,仅 mGluR5 在小胶质细胞中检测到 mRNA 表达,但其对小胶质细胞激活的调控作用及机制尚未明确。本研究聚焦 mGluR5,探究其是否通过调控 NADPH 氧化酶抑制小胶质细胞过度激活,为神经炎症相关疾病的治疗提供实验依据。
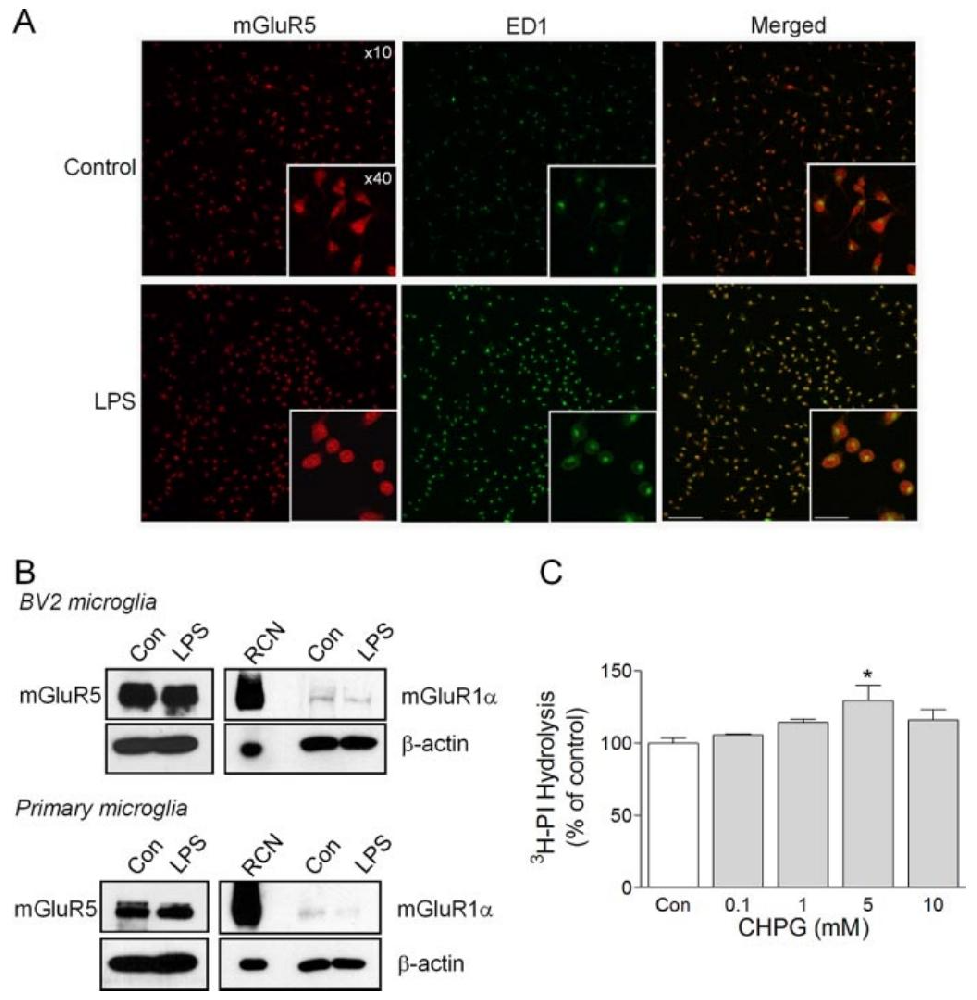
图 1:小胶质细胞表达功能性 mGluR5 受体
该图通过多种方法证实 mGluR5 在小胶质细胞中的表达及功能:(A)免疫细胞化学显示,BV2 和原代皮质小胶质细胞中 mGluR5(红色)呈强阳性表达,LPS 刺激后细胞形态从静息的分支状变为激活的阿米巴状,且与激活标志物 ED1 共定位;(B)Western blot 证实,BV2 和原代小胶质细胞中 mGluR5 蛋白高表达,而同为 Ⅰ 组的 mGluR1 几乎不表达;(C)PI 水解实验显示,mGluR5 选择性激动剂 CHPG 可剂量依赖性促进 BV2 细胞的磷酸肌醇水解(5mM 时显著升高),证实 mGluR5 具有功能性信号传导能力。
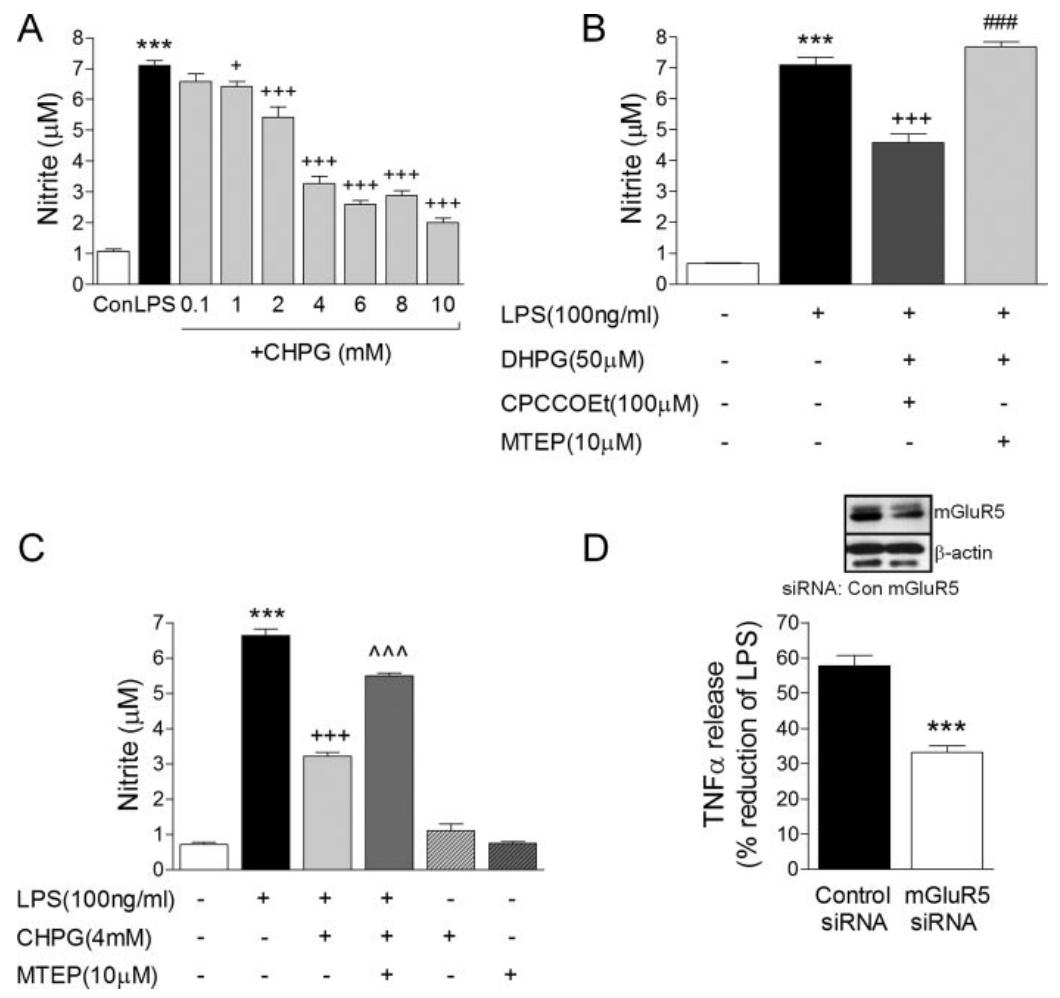
图 2:mGluR5 激活选择性抑制小胶质细胞激活
该图验证 mGluR5 激活对 LPS 诱导的小胶质细胞激活的影响:(A)CHPG 剂量依赖性降低 LPS 刺激的 BV2 细胞 NO 生成(1mM 起显著,4mM 时抑制约 50%);(B)非选择性 Ⅰ 组 mGluR 激动剂 DHPG 联合 mGluR1 拮抗剂 CPCCOEt,可显著减少 NO 释放,而 DHPG 联合 mGluR5 拮抗剂 MTEP 则无此效果,提示作用依赖 mGluR5;(C)MTEP 可逆转 CHPG 对 NO 生成的抑制,证实特异性;(D)mGluR5 siRNA 敲低后,CHPG 对 TNF-α 释放的抑制作用减弱(抑制率从 57.7% 降至 33.2%),进一步验证 mGluR5 的介导作用。
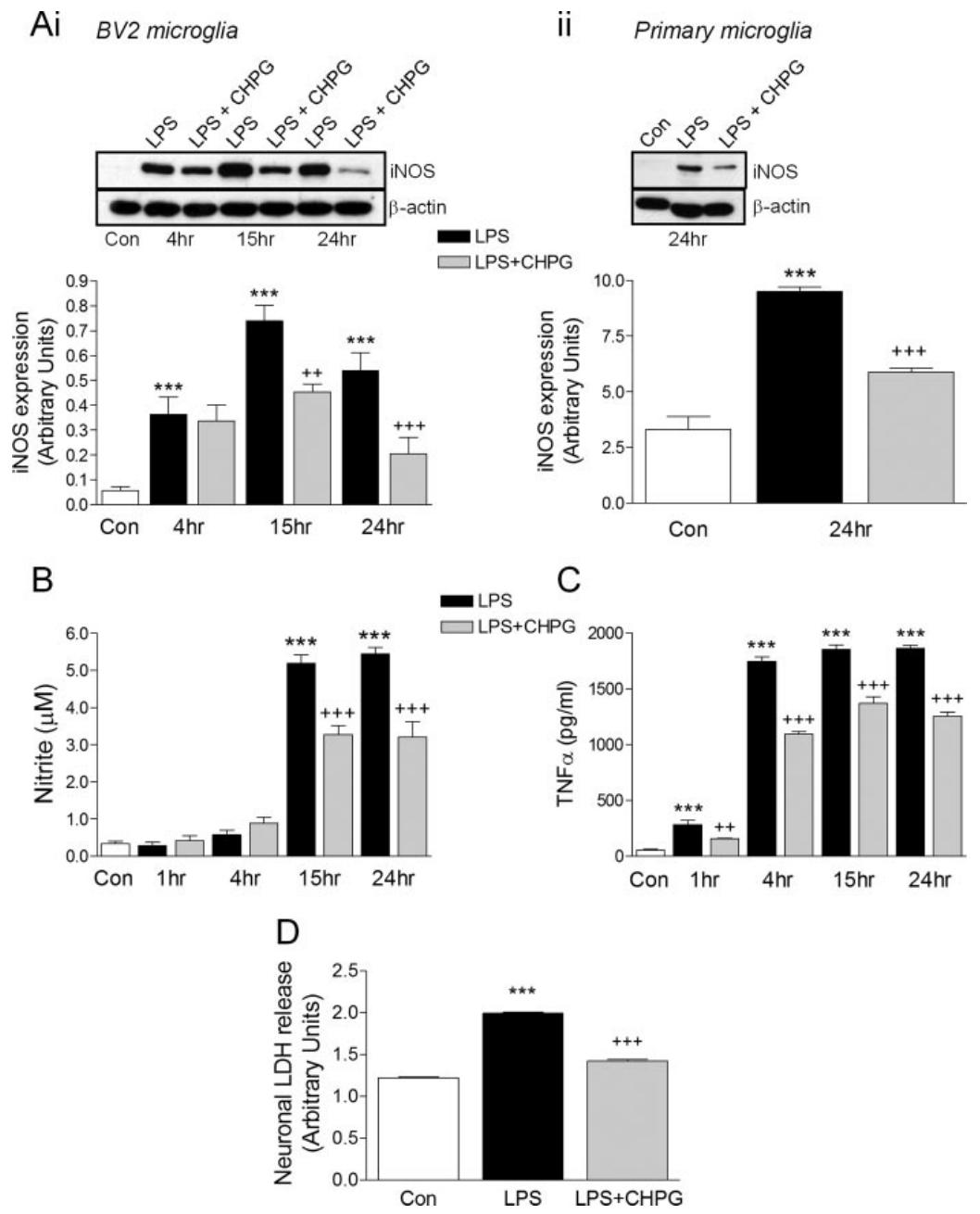
图 3:mGluR5 激活减少炎症介质释放及神经毒性
该图显示 mGluR5 激活对炎症反应和神经损伤的缓解作用:(A)LPS 刺激后,BV2 和原代小胶质细胞的 iNOS 蛋白表达显著升高(4-24h),CHPG 预处理可显著下调(15-24h 尤为明显);(B、C)LPS 诱导的 NO 生成(15-24h)和 TNF-α 释放(1-24h)均被 CHPG 显著抑制;(D)LPS 刺激的小胶质细胞条件培养基可诱导 B35 神经母细胞瘤细胞死亡(LDH 释放增加),而 CHPG 预处理的条件培养基能显著减少神经元死亡,证实神经保护作用。
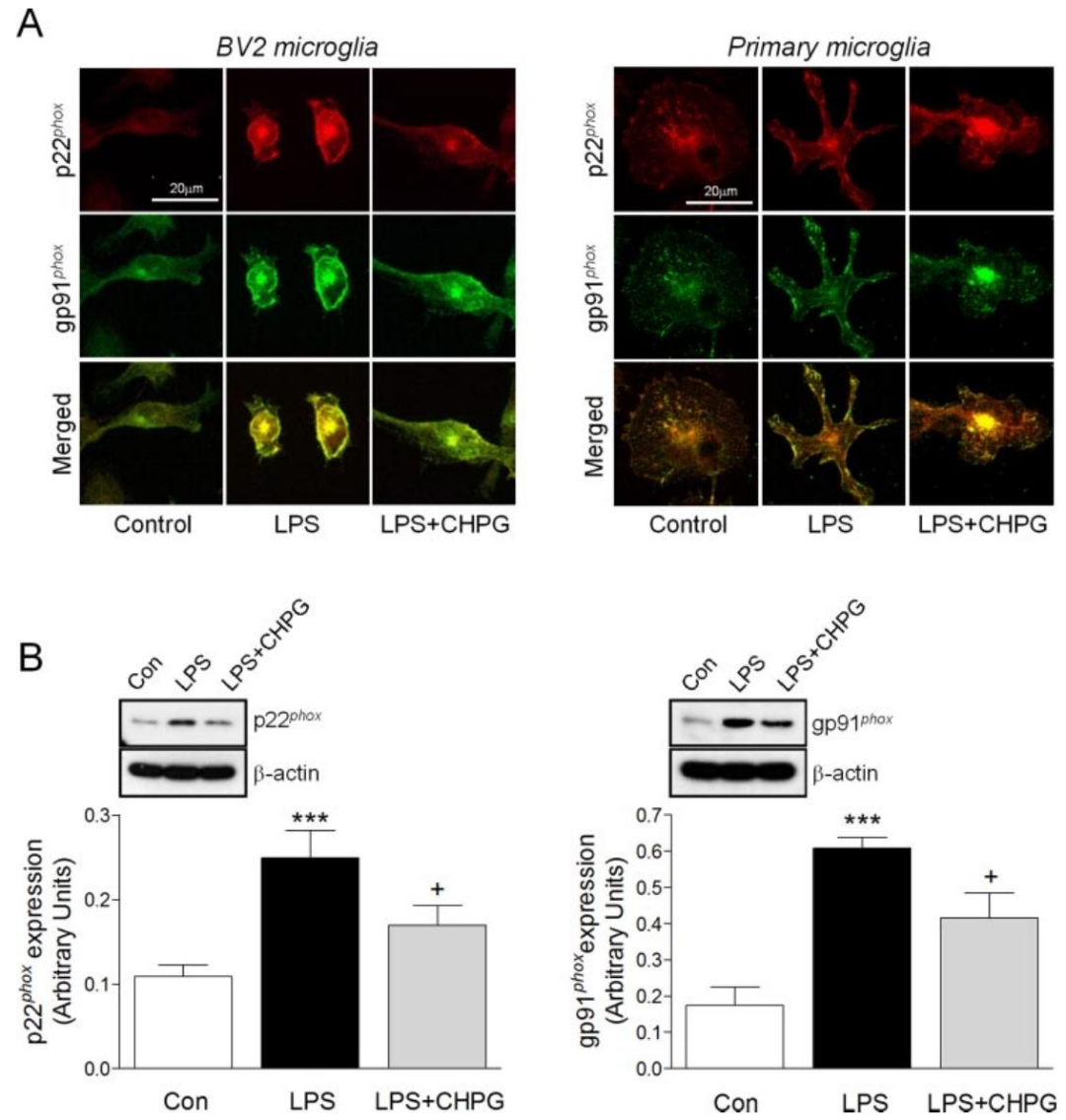
图 4:mGluR5 激活降低 NADPH 氧化酶亚基表达
该图探讨 mGluR5 对 NADPH 氧化酶的调控:(A)免疫细胞化学显示,LPS 刺激后,BV2 和原代小胶质细胞中 NADPH 氧化酶膜亚基 p22phox(红色)和 gp91phox(绿色)表达升高且在膜上共定位,CHPG 预处理可显著降低其表达及共定位;(B)Western blot 证实,CHPG 可显著下调 LPS 诱导的 p22phox 和 gp91phox 蛋白表达,提示 mGluR5 可能通过抑制该酶复合体组装发挥作用。
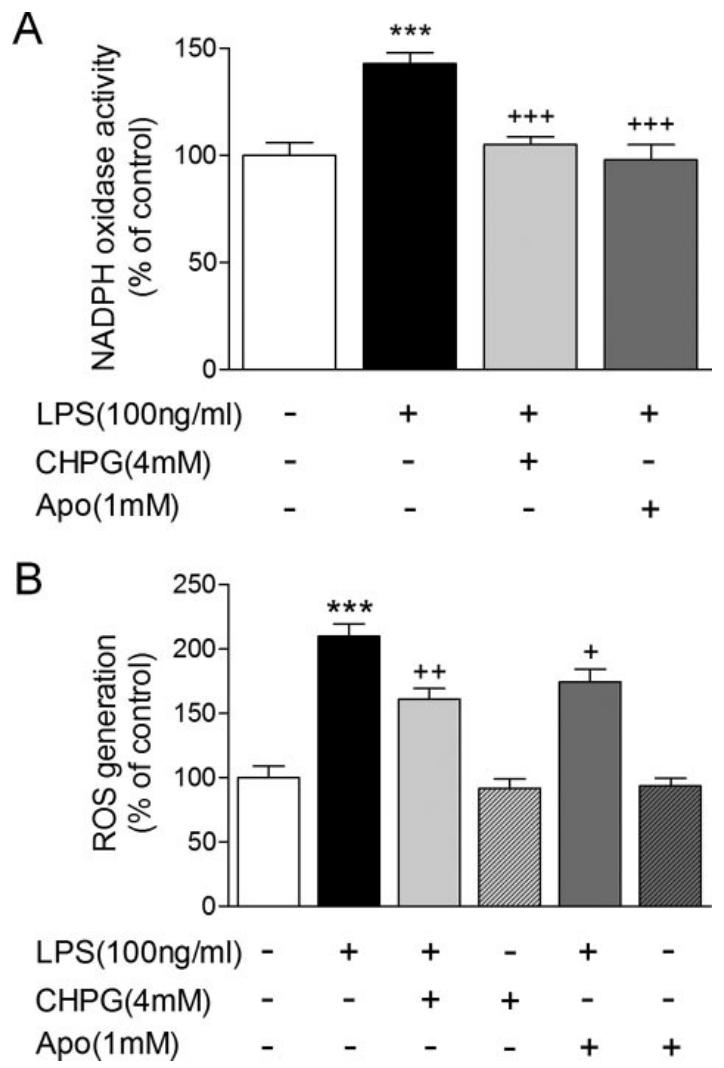
图 5:mGluR5 激活抑制 NADPH 氧化酶活性及 ROS 生成
该图验证 NADPH 氧化酶功能受抑:(A)LPS 刺激 4h 后,BV2 细胞 NADPH 氧化酶活性显著升高,CHPG 预处理可使其降至对照组水平,效果与 NADPH 氧化酶抑制剂 apocynin 相当;(B)LPS 刺激 24h 诱导的细胞内 ROS 生成(H₂DCFDA 检测),可被 CHPG 或 apocynin 显著抑制,且二者单独处理无影响,证实 mGluR5 通过抑制 NADPH 氧化酶减少 ROS。
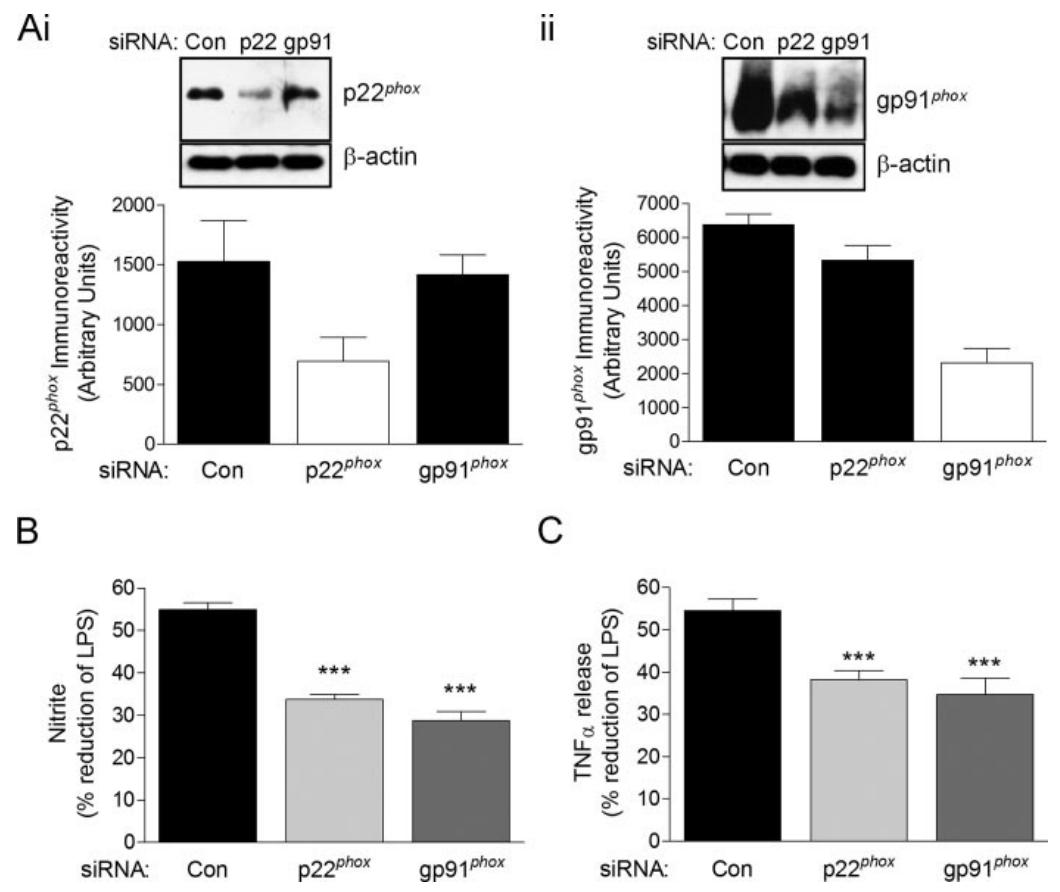
图 6:NADPH 氧化酶亚基敲低减弱 mGluR5 的保护作用
该图通过 siRNA 验证 NADPH 氧化酶的必要性:(A)p22phox 或 gp91phox siRNA 可分别降低其蛋白表达 52% 和 60%;(B、C)与对照 siRNA 相比,p22phox 或 gp91phox 敲低后,CHPG 对 LPS 诱导的 NO 生成和 TNF-α 释放的抑制作用显著减弱(抑制率下降约 38%),表明 NADPH 氧化酶是 mGluR5 发挥保护作用的关键介质。
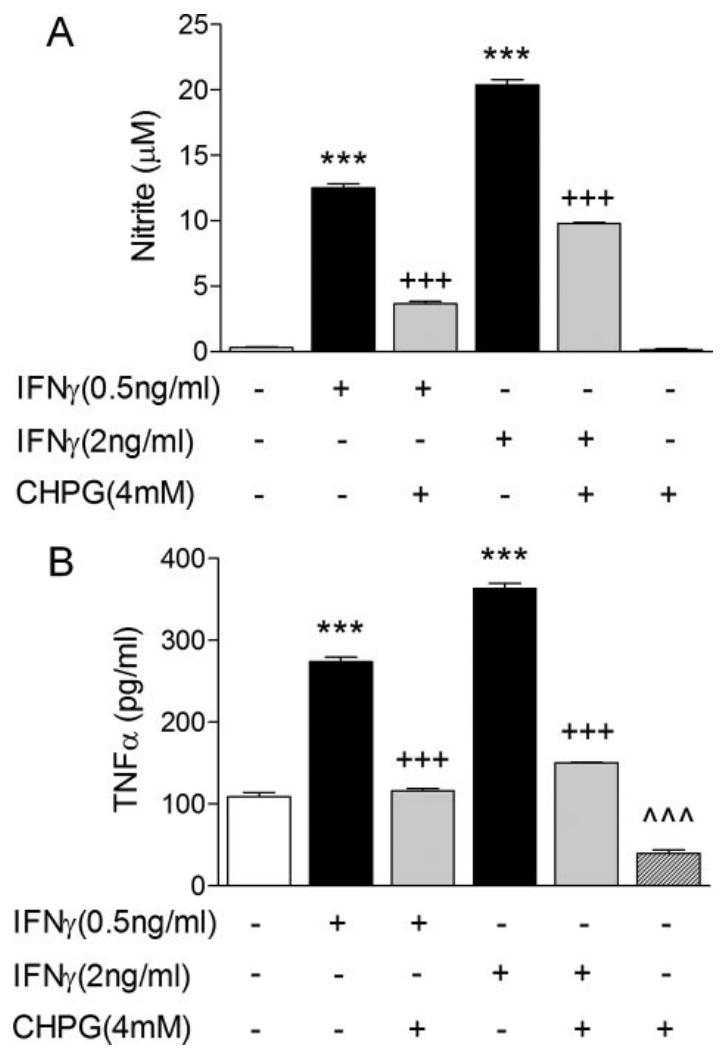
图 7:mGluR5 激活抑制 IFN-γ 诱导的小胶质细胞激活
该图扩展了 mGluR5 作用的普遍性:(A、B)IFN-γ(0.5-2ng/ml)可剂量依赖性诱导 BV2 细胞 NO 生成和 TNF-α 释放,CHPG 预处理可使二者减少 50% 以上,证实 mGluR5 激活对不同刺激诱导的小胶质细胞激活均有抑制作用。
代谢型谷氨酸受体 5(mGluR5)在小胶质细胞中高表达且具有功能活性,其激活(如通过选择性激动剂 CHPG)可通过抑制 NADPH 氧化酶(下调 p22phox、gp91phox 亚基表达及酶活性),减少 LPS 或 IFN-γ 诱导的炎症介质(iNOS、NO、TNF-α)释放和活性氧(ROS)生成,从而显著降低小胶质细胞介导的神经毒性。该研究证实 mGluR5 是调控神经炎症的关键靶点,为阿尔茨海默病、创伤性脑损伤等神经退行性疾病和中枢神经系统损伤的治疗提供了新策略。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:天然抗菌剂显威力!AuraAqua 破解虾透明幼体病难题,死亡率从 91% 降至 6%
下一篇:告别瞬时信号!稳定表达 FLuc 的肝癌细胞系,让体内成像更靠谱