常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-10-30 09:10:24 细胞资源库平台 访问量:295
Reporter THP1 Cell Line 细胞系是以 THP1 为工具细胞,采用慢病毒感染的方式,构建稳定表达报告基因的细胞系,可用于检测信号通路转导。在被PMA、INF-α等刺激后,目标信号通路被激活,会启动下游特定基因的表达,这个表达过程会同时带动“报告基因”的表达。通过检测报告基因的信号强度,可以间接、定量、灵敏地衡量该信号通路的激活程度。
THP-1细胞本身来源于人单核细胞,可以分化为巨噬细胞样细胞,是研究先天免疫的经典模型。报告基因株的建立使其功能更强大。THP-1报告基因株是免疫学、炎症性疾病、药物研发等领域不可或缺的强大工具。它可以将一个复杂的、内在的生物学过程(信号通路激活/基因表达)转变为一个易于检测、可定量的物理信号(光或荧光)。这使得研究人员能够高通量地筛选药物,精确地量化免疫反应强度,直观地研究信号通路机制。
英文标题:Screening Bioactive Nanoparticles in Phagocytic Immune Cells for Inhibitors of Toll-like Receptor Signaling
中文标题:在吞噬性免疫细胞中筛选具有 Toll 样受体信号抑制作用的生物活性纳米颗粒
发表期刊:《Journal of Visualized Experiments》
影响因子:1.0
作者单位:
1. Department of Respiratory Medicine, Shanghai First People's Hospital, Shanghai Jiaotong University School of Medicine2. Department of Pediatrics, BC Children's Hospital and University of British Columbia
作者信息:
Hong Yang, Shan Yu Fung, Aihua Bao, Qiang Li, Stuart E. Turvey
Toll 样受体(TLR)是先天免疫系统的关键组成部分,通过识别病原体相关分子模式(PAMPs)启动免疫防御,但过度激活会诱发败血症、系统性红斑狼疮、类风湿关节炎等多种炎症及自身免疫疾病。目前临床可用的 TLR 抑制剂极为有限,仅抗疟药羟氯喹可抑制 TLR7/9,而单一 TLR 靶点抑制剂(如 TLR4 拮抗剂 eritoran)因炎症常涉及多 TLR 通路,III 期临床试验未能降低重症败血症患者死亡率。纳米技术的发展为 TLR 调控提供新方向 —— 纳米颗粒凭借纳米尺寸优势及可功能化表面,能优化生物分布并赋予特定免疫活性。本研究建立基于人 THP-1 单核细胞衍生报告细胞的高通量筛选体系,通过分泌型碱性磷酸酶(SEAP,受 NF-κB/AP-1 调控)和荧光素酶(受 IRF 调控)双报告基因,筛选可抑制 TLR 信号的肽 - 金纳米颗粒(peptide-GNP),为多靶点 TLR 抑制剂开发提供实验工具。
培养基与试剂制备:配制完全培养基 R10(RPMI-1640+10% 胎牛血清 + 2mM L - 谷氨酰胺 + 1mM 丙酮酸钠),选择培养基 R10-Z(加 200μg/mL Zeocin)和 R10-ZB(加 100μg/mL Zeocin+10μg/mL 杀稻瘟素);制备 SEAP / 荧光素酶底物(避光储存,有效期 2 周 / 1 个月),PMA、LPS 分装 - 20℃保存,避免反复冻融。
THP-1 报告细胞培养与分化:用 THP-1-XBlue(SEAP 单报告)和 THP-1-Dual(双报告)细胞,解冻后 300×g 离心重悬,接种 T75 瓶传代(维持密度 2-5×10⁵细胞 /mL);选择培养基培养 1 代后,96 孔板接种(1×10⁶细胞 /mL+50ng/mL PMA),37℃孵育 24h 分化为巨噬细胞,PBS 洗涤后静置 2 天降低背景。
TLR4 纳米抑制剂筛选:LPS 剂量响应实验确定最佳浓度(10ng/mL);肽 - GNP 浓缩至 200nM(18000×g 离心),与 LPS 混合(终浓度 100nM GNP、10ng/mL LPS);每孔加 100μL 混合液,孵育 24h 后离心去未内化 GNP,测上清 SEAP(655nm 吸光度)和荧光素酶活性。
候选物验证与 TLR 特异性评估:固定 GNP 浓度,用不同 LPS 浓度验证;免疫印迹检测 NF-κB/IRF 通路蛋白;测试 TLR2(Pam3CSK4)、TLR3(poly I:C)、TLR5(鞭毛蛋白)的抑制效果,评估广谱性。
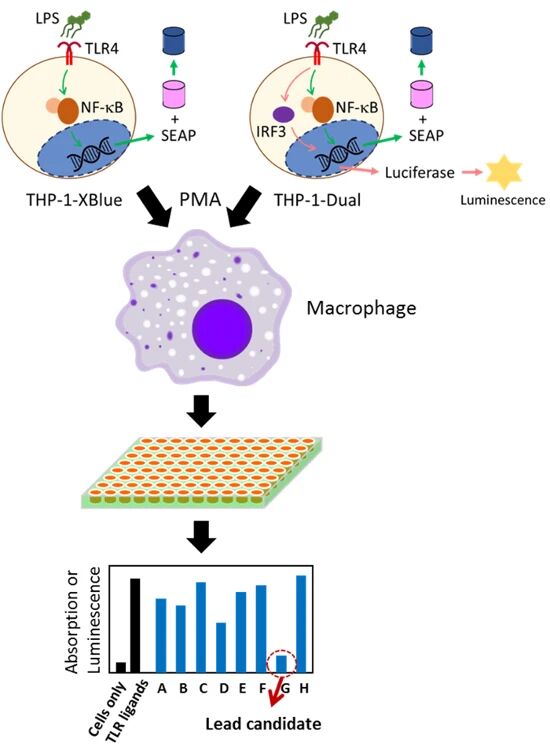
图1:TLR 抑制剂高通量筛选总体实验流程
图 1 展示筛选体系的核心设计:THP-1-XBlue 细胞通过 SEAP 报告 NF-κB/AP-1 激活,THP-1-Dual 细胞额外通过荧光素酶报告 IRF 激活;两种细胞经 PMA 分化为巨噬细胞后,受 TLR4 激动剂 LPS 刺激激活信号通路,最终通过底物检测报告基因活性,实现对 TLR 信号抑制性纳米颗粒的筛选,清晰呈现 “细胞制备 - 信号刺激 - 活性检测 - 候选物筛选” 的完整流程。
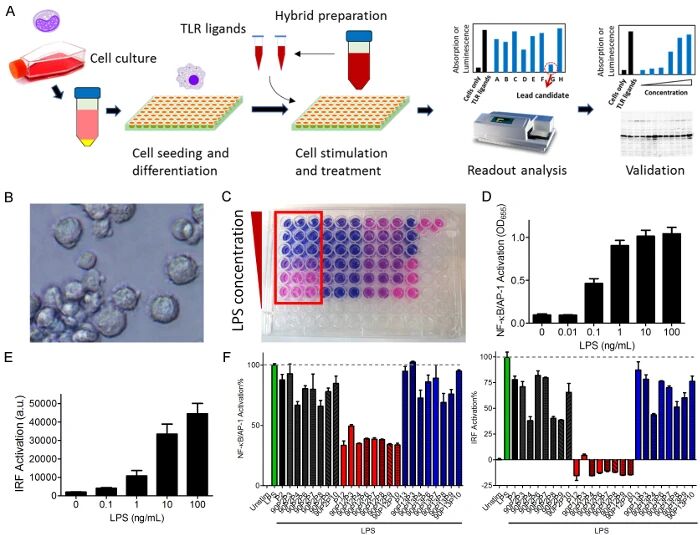
图2:TLR4 纳米抑制剂筛选过程与结果
图 2A 为筛选实验的步骤示意图;
图 2B 为分化后巨噬细胞的光学显微镜图像(200× 放大),可见细胞贴壁生长并呈现伪足形态;
图 2C 为 SEAP 底物的颜色变化结果,随 SEAP 表达量增加,底物从粉色逐渐变为紫色或深蓝色;
图 2D 通过 655nm 吸光度定量显示,LPS 浓度与 NF-κB/AP-1 激活呈剂量依赖性;
图 2E 通过荧光素酶活性定量显示,LPS 浓度与 IRF 激活呈剂量依赖性;
图 2F 为筛选结果,肽 - GNP P12 及其衍生物可显著抑制 LPS 诱导的 NF-κB/AP-1 和 IRF 激活,而结构相近的 P13-GNP 无抑制活性,可作为阴性对照。
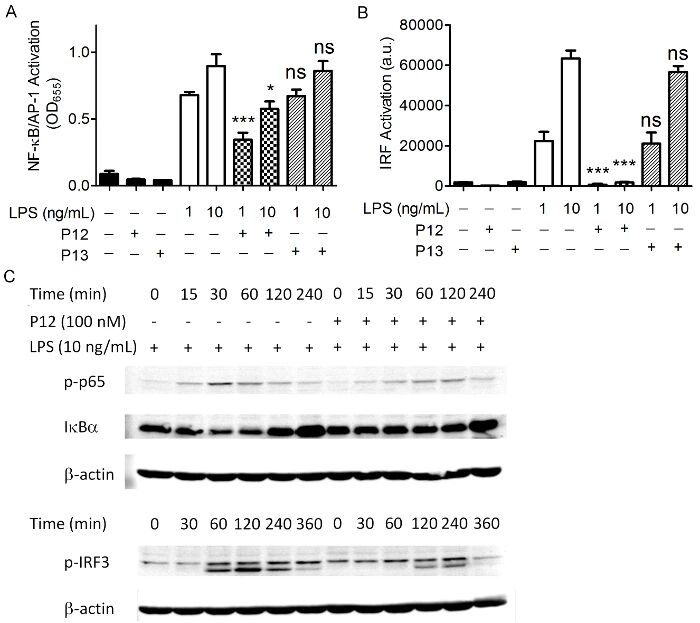
图3:候选物抑制活性验证
图 3A、B 显示,固定 100nM P12-GNP 浓度时,随 LPS 浓度升高(1→10ng/mL),P12 对 SEAP(A)和荧光素酶(B)活性的抑制效果逐渐减弱,符合剂量依赖规律;图 3C 免疫印迹结果显示,P12-GNP 可减少 p65 磷酸化、抑制 IκBα 降解(NF-κB 通路),并延迟 IRF3 磷酸化(IRF 通路),而 P13-GNP 无此作用,直接证实 P12 对 TLR4 信号通路的特异性抑制。
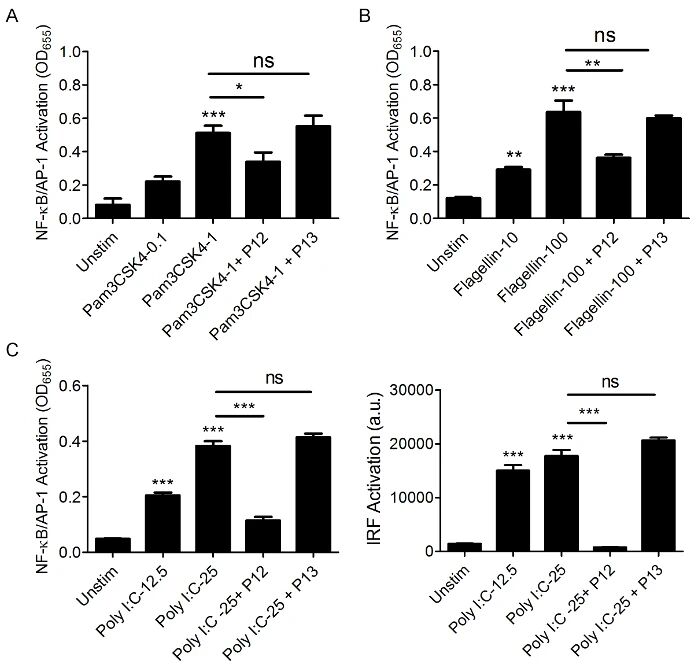
图4:候选物对其他 TLR 通路的抑制效果
图 4A 显示,P12-GNP 可显著抑制 TLR2 激动剂 Pam3CSK4(1ng/mL)诱导的 NF-κB/AP-1 激活;
图 4B 显示,P12-GNP 可显著抑制 TLR5 激动剂鞭毛蛋白(100ng/mL)诱导的 NF-κB/AP-1 激活;
图 4C 显示,P12-GNP 可同时抑制 TLR3 激动剂 poly I:C(25μg/mL)诱导的 NF-κB/AP-1 和 IRF 激活;P13-GNP 在所有 TLR 通路中均无抑制活性,证实 P12-GNP 具有广谱 TLR 抑制作用。
本研究建立的基于 THP-1 报告细胞的高通量筛选体系,可快速、定量地筛选抑制 TLR 信号的生物活性纳米颗粒 —— 通过 SEAP 和荧光素酶双报告基因,同步覆盖 NF-κB/AP-1 和 IRF 两条核心 TLR 信号通路,且细胞分化为巨噬细胞后更贴合体内炎症相关细胞模型。筛选出的肽 - GNP P12 可通过下调 NF-κB 和 IRF3 激活,广谱抑制 TLR2、3、4、5 信号通路,无明显细胞毒性。该筛选方法不仅为 TLR 信号研究提供高效工具,更能加速多靶点 TLR 抑制剂(尤其是纳米类药物)的开发,为炎症及自身免疫疾病治疗提供新方向。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
下一篇:浮游微泡对卡介苗−Guerin的长期释放,以增强膀胱癌的膀胱内免疫治疗