常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-09-20 17:30:09 细胞资源库平台 访问量:273
蝙蝠具有独特的能力,能够携带并耐受对人类和非人灵长类动物高度致病的病原体。比较基因组学研究表明,蝙蝠具有增强先天免疫反应和限制过度炎症的遗传基础,但功能性遗传研究由于蝙蝠独特的生活方式、保护地位以及缺乏针对这些非模式生物优化的分子工具而面临挑战。
目前对蝙蝠抗病毒免疫的研究主要集中在感染蝙蝠的外周免疫反应或永生化细胞系上,这些研究为了解其免疫防御机制提供了重要见解。然而,作为病毒进入的主要部位和对抗局部和全身感染的第一道防线的粘膜表面,在蝙蝠中尚未得到充分研究。
埃及果蝠(Rousettus aegyptiacus)是多种人类病原体的天然宿主,包括高致病性马尔堡病毒(MARV)。为了深入理解蝙蝠异常的病毒耐受能力的分子机制,迫切需要开发生理相关且遗传可操作的研究模型。类器官技术为体外重现组织特异性细胞多样性和功能提供了独特的平台,但迄今为止尚未应用于蝙蝠免疫学研究。
近期,发表在Nature immunology期刊,题为Bat organoids reveal antiviral responses at epithelial surfaces的研究中,研究者利用类器官平台揭示了蝙蝠上皮抗病毒免疫的关键特征,可能为病毒疾病恢复力的治疗策略提供信息。
1,蝙蝠呼吸道类器官的建立与细胞多样性分析:研究团队成功建立了来自埃及果蝠鼻腔、气管、支气管和肺泡的多种呼吸道类器官模型。通过单细胞RNA测序分析发现,这些类器官能够重现体内上皮细胞的细胞多样性,包括基底细胞、纤毛细胞、分泌细胞、刷状细胞以及稀有的微皱褶细胞(M细胞)和离子细胞等。特别是在支气管类器官中发现了表达GP2的微皱褶细胞,这些细胞是罕见的抗原采样细胞,在先天淋巴组织中发挥重要作用。肺泡类器官主要由SFTPC+SFTPB+的II型肺泡上皮细胞组成,能够维持长期培养。
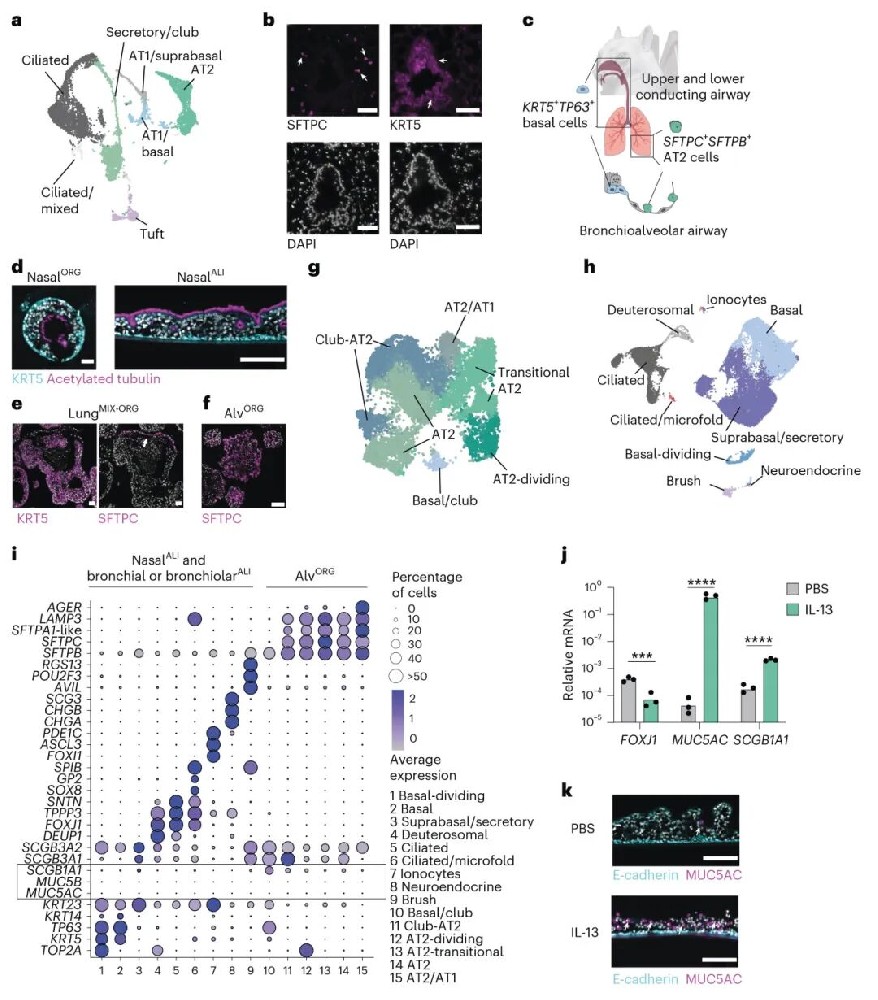
图1 埃及伊蚊鼻腔、支气管和肺泡气道类器官含有多种细胞类型
2,蝙蝠小肠类器官的特征分析:小肠类器官(SIORG)展现出典型的出芽形态,包含多种肠道上皮细胞类型,如干细胞、过渡扩增细胞、肠道祖细胞、杯状细胞、肠细胞和肠内分泌细胞等。通过与体内小肠组织的比较分析,发现类器官能够高度重现原始组织的细胞类型比例和基因表达特征。在分化培养条件下,类器官中肠细胞的比例显著增加,表明其具有良好的分化潜能。
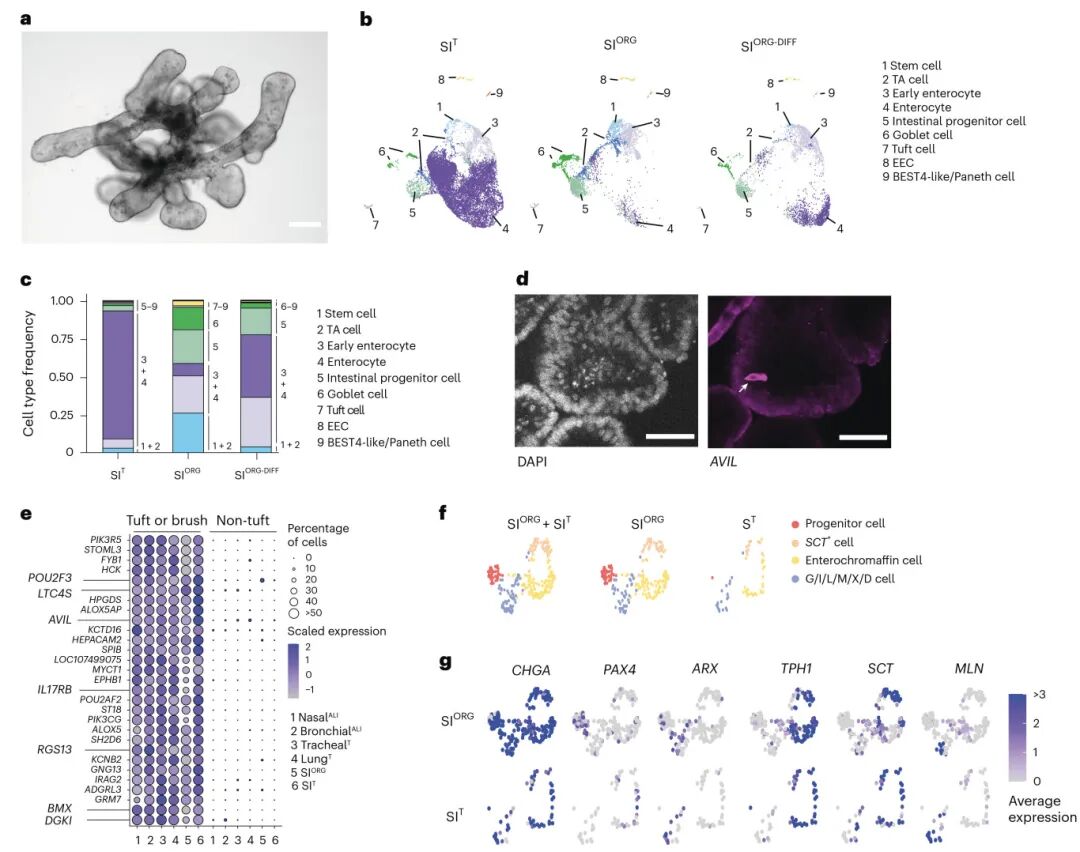
图2 R. aegyptiacus SI类器官重现了本地蝙蝠肠上皮细胞多样性
3,蝙蝠类器官中先天免疫效应分子的本底高表达:与人类类器官相比,蝙蝠类器官显示出先天免疫效应基因的显著高表达,特别是补体系统基因(如C2、C3、C6、C7、C9等)和干扰素刺激基因(ISGs)。最引人注目的是,蝙蝠类器官中IFNε(IFNE)基因的高水平表达,这是一种非典型的I型干扰素,通常仅限于雌性生殖道表达。免疫荧光染色证实了IFNε蛋白在蝙蝠小肠绒毛中的强烈表达。通过CRISPR-Cas9敲除IFNE基因的功能研究表明,IFNε的缺失导致ISGs表达降低和对病毒感染敏感性增加。
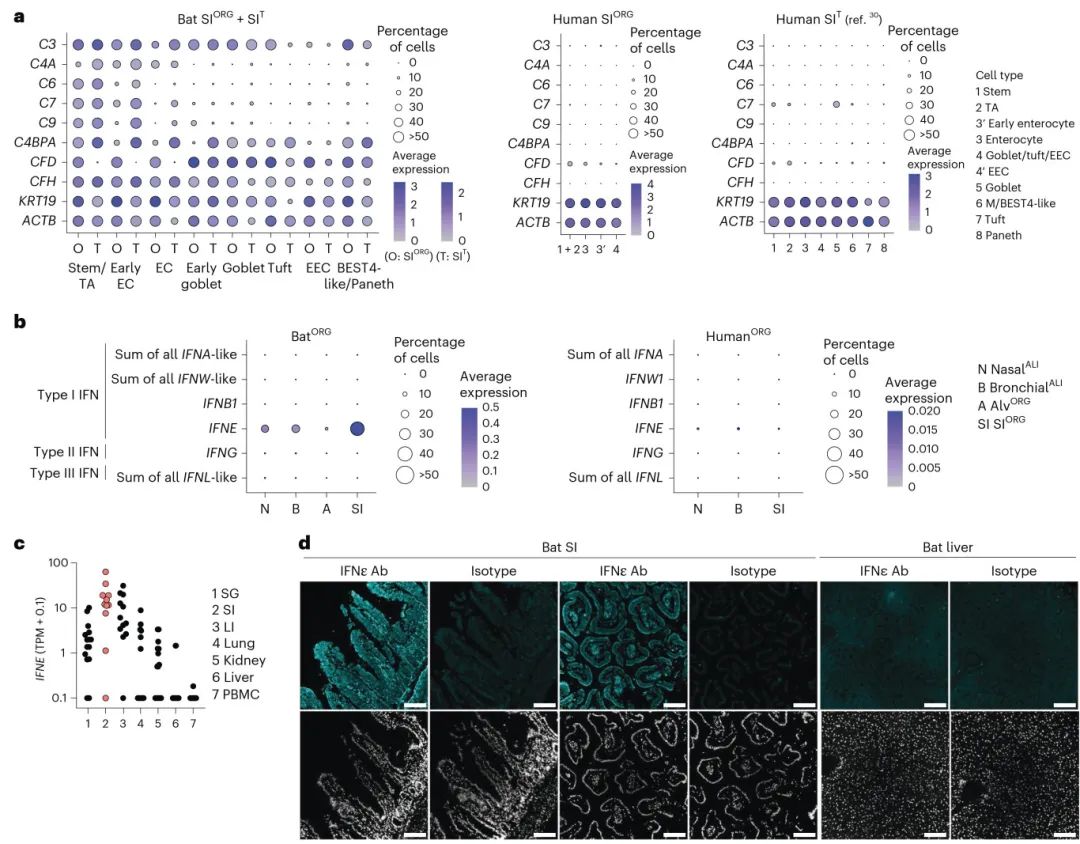
图3 与人类类器官相比,蝙蝠类器官表现出先天免疫基因的高表达,包括补体系统基因、IFNε和ISG
4,蝙蝠类器官对病毒感染的强烈干扰素应答:使用马尔堡病毒、MERS-CoV、仙台病毒等多种人畜共患病毒感染蝙蝠类器官,发现其能够强烈诱导I型和III型干扰素反应。bulk RNA测序分析显示,感染后蝙蝠类器官中大量ISGs被激活,包括MX1、IRF7、USP18、TRANK1等。特别是III型干扰素IFNλ1-like和IFNλ3-like的表达最为显著,而相比之下,感染相同病毒的人类类器官则表现出微弱的干扰素反应。基因本体论分析显示,上调基因主要富集在病毒防御和干扰素信号通路相关的生物过程中。
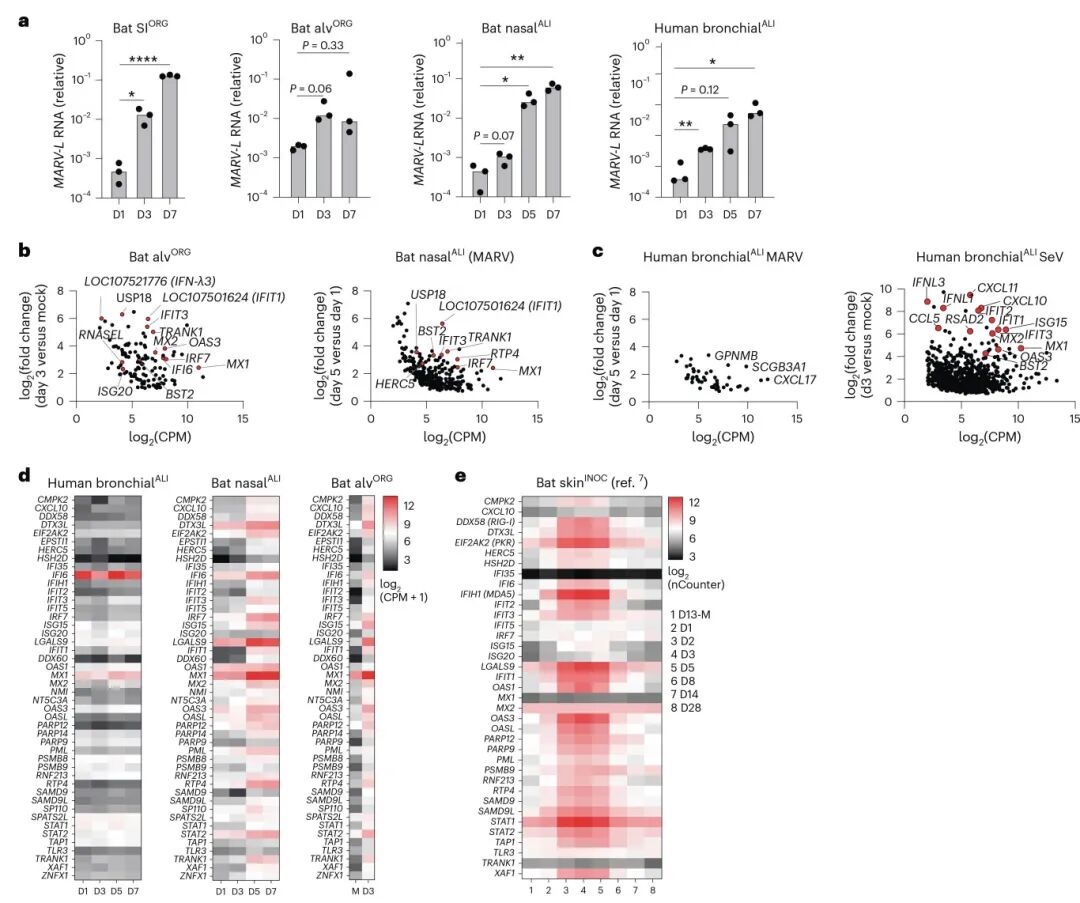
图4 蝙蝠类器官中的MARV感染触发了IFN反应
5,III型干扰素的自我放大机制:研究发现蝙蝠特有的现象,即IFNλ3-like不仅作为干扰素发挥抗病毒作用,同时也作为干扰素刺激基因(ISG)被诱导表达,形成病毒非依赖性的自我放大环路。通过IRF9基因敲除实验证实,这种自我调节依赖于干扰素信号通路。重组IFNλ3-like蛋白处理实验进一步证实了其自我诱导能力,这种独特的正反馈机制可能是蝙蝠抗病毒免疫的重要特征。
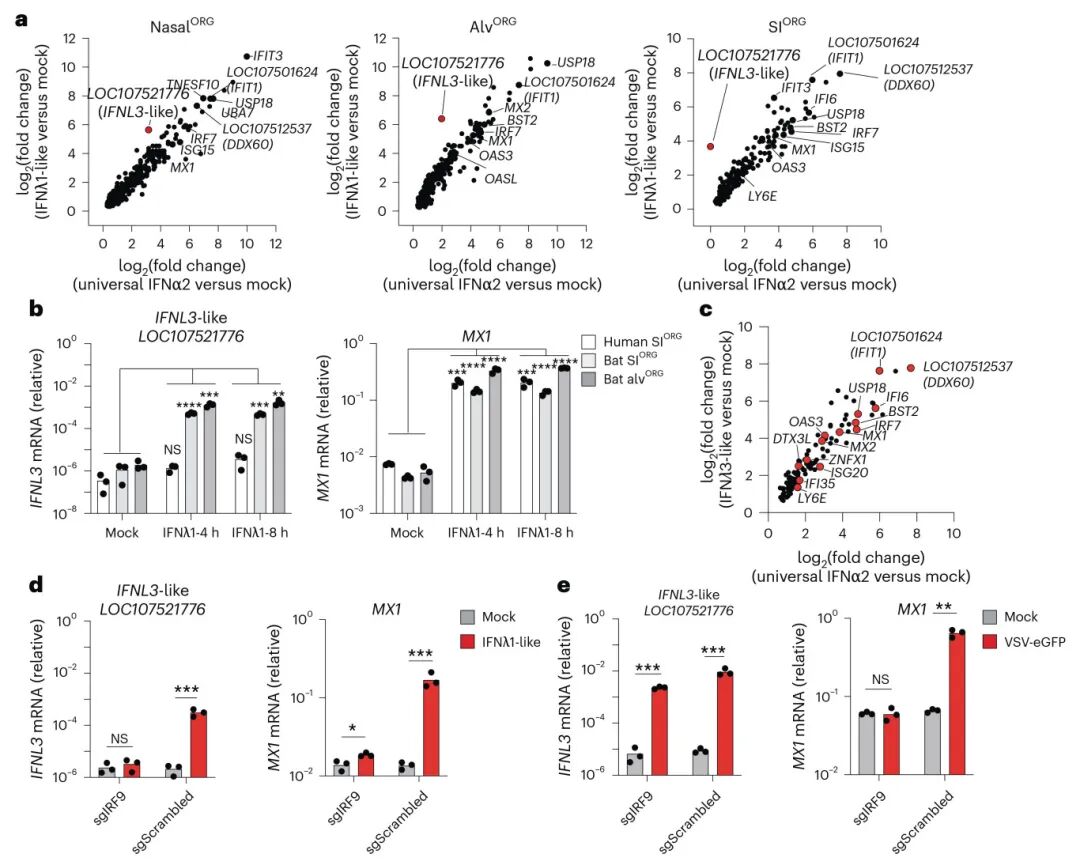
图 5 蝙蝠III型IFNλ驱动蝙蝠类器官的自我放大抗病毒反应
6,干扰素的抗病毒保护效应及动力学差异:功能实验显示,蝙蝠I型和III型干扰素均能有效保护类器官免受病毒感染,包括VSV、MARV等。预处理、同时处理或感染后处理均显示出显著的保护效果,病毒RNA水平降低至对照组的1-30%。时程分析揭示了I型和III型干扰素在动力学上的差异:III型干扰素诱导的ISGs表达更为持久,在干扰素移除24小时后仍维持较高水平,而I型干扰素的效应则较快消退。这种持续性保护可能是蝙蝠抵御病毒感染的重要机制。
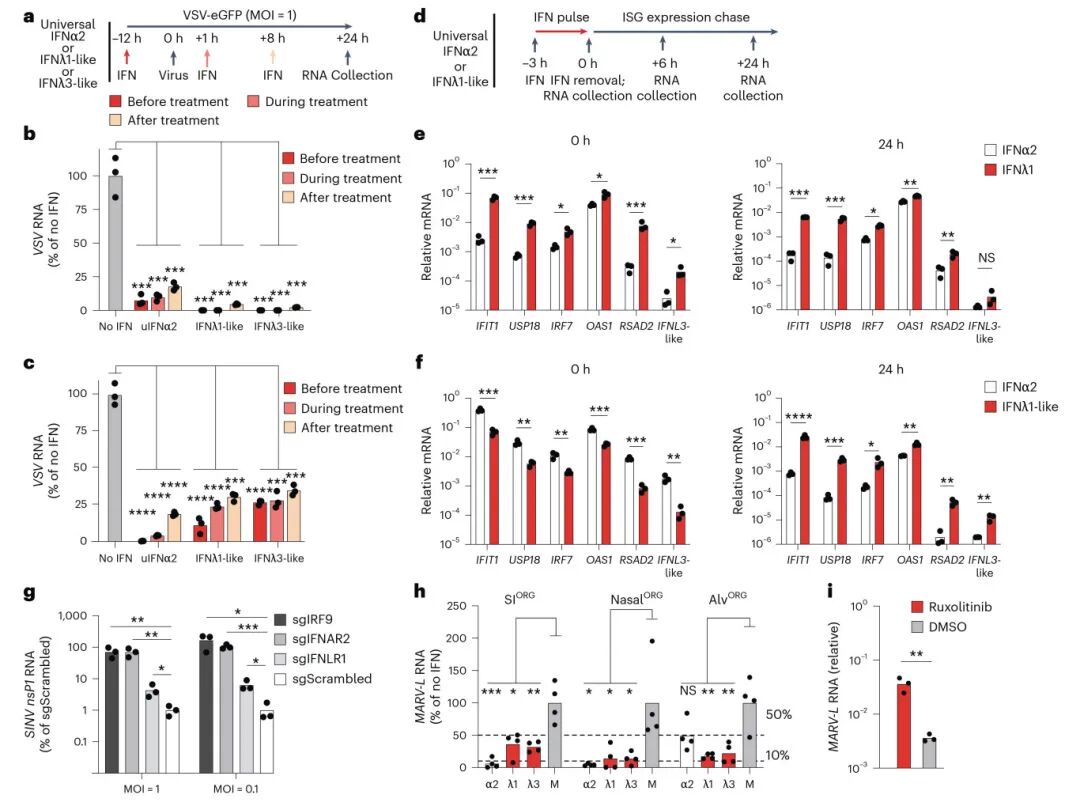
图 6 I型和III型IFN保护蝙蝠类器官免受人畜共患病病毒感染
本研究建立了首个蝙蝠上皮类器官平台,为研究蝙蝠独特的抗病毒免疫机制提供了重要工具。研究揭示了蝙蝠上皮细胞中先天免疫基因的本底高表达、强烈的干扰素反应以及III型干扰素的独特自我放大机制,这些发现有助于理解蝙蝠作为病毒宿主却不发病的分子基础。该研究不仅推进了比较免疫学的发展,也为开发新型抗病毒治疗策略提供了重要启示。特别是III型干扰素在蝙蝠中的独特作用机制,可能为预防和治疗人类病毒感染提供新的思路。此外,该类器官模型还可用于研究其他人畜共患病病原体的感染机制,为公共卫生防控提供科学支撑。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:功能性青蒿素衍生物工程纳米杂化物促进铁死亡应激驱动的癌症治疗