常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-09-14 09:18:28 细胞资源库平台 访问量:275
癌细胞侵袭周围组织时经常发生部分上皮-间充质转化(pEMT)并采用集体侵袭模式,但这些表型特征的调控机制及其相互关联仍不清楚。上皮-间充质转化(EMT)是癌细胞获得侵袭和转移能力的关键过程,在此过程中癌细胞协调性地失去上皮细胞的顶-基极性和细胞粘附系统,同时获得前-后极性和其他间充质特征。然而,EMT往往是不完全和可逆的,导致高度动态的杂交状态或部分EMT(pEMT),癌细胞在不同程度上保留上皮特征的同时获得间充质特征。
从病理生理学角度来看,pEMT具有高度疾病相关性。首先,在转移实验模型中,处于pEMT状态的癌细胞在播种继发性肿瘤方面比完全上皮或间充质状态的细胞更有效。其次,pEMT与集体癌细胞侵袭模式相关,这是人类癌症中最常观察到的基质浸润类型。在原型EMT中,多种细胞外信号和环境条件可触发Snail、Zeb和Twist转录因子家族成员的表达,这些核心EMT转录因子协调广泛的基因表达变化。然而,越来越多的研究表明EMT过程可能不一定作为统一、基本不变的转录程序的结果展开,而是表现为高度依赖背景和分子不同的基因表达程序。
近期,发布在Oncogenesis期刊,题为TGF-β signaling redirects Sox11 gene regulatory activity to promote partial EMT and collective invasion of oncogenically transformed intestinal organoids的文章以携带结直肠癌(CRC)驱动突变的肠道类器官为模型,探讨了TGF-β1诱导的pEMT及集体侵袭的机制基础。
1) scRNA-seq揭示TGF-β1诱导的广谱转换状态和pEMT终点:研究者使用携带结直肠癌驱动突变(Apc、Kras、Trp53)的小鼠肠道类器官(TKA-类器官)进行单细胞RNA测序分析。TGF-β1处理后,类器官形成内聚性细胞片并扩散到周围细胞外基质中。scRNA-seq分析识别出9个具有相似基因表达谱的细胞簇,细胞通过一系列过渡状态最终到达pEMT终点。RNA速度分析和PAGA轨迹推断确定未处理的cluster 3细胞是所有其他细胞状态的起源。重要的是,研究未能识别出显示上皮标记物丢失和间充质标记物获得互补性变化的细胞簇,而是发现了上皮和间充质标记物在单细胞水平的共表达。
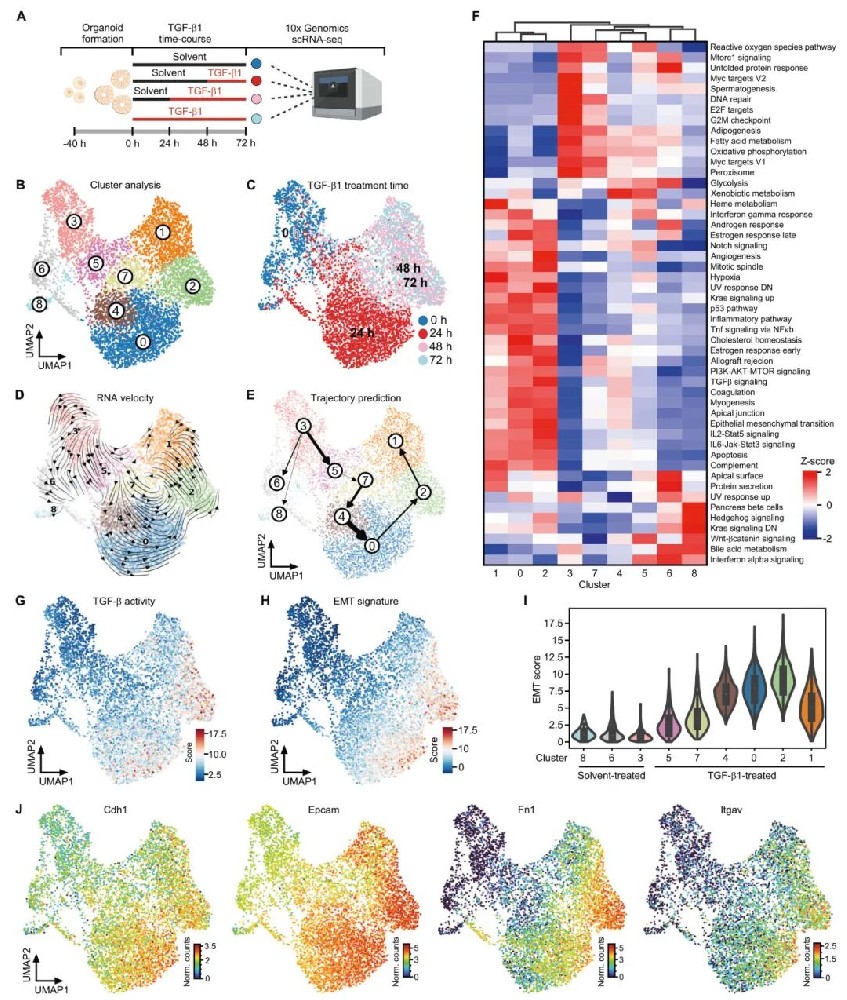
图1 检测TGF-β1处理的TKA类器官中广泛的瞬态状态和pEMT终点
2) leader细胞基因表达谱与最高级pEMT状态的关联:为了解不同pEMT状态如何与集体侵袭细胞群体的表型不同亚群对应,研究者创建了leader细胞特征性基因签名并在scRNA-seq数据集中评分其表达。leader细胞基因表达谱的获得逐渐发生,并反映了TGF-β通路活性和EMT签名表达的动态,在cluster 2中达到最大代表性。纤维连接蛋白作为间充质标记物和leader细胞签名的组成部分,在TGF-β1处理的TKA类器官最外围细胞中表达峰值,这些细胞可能代表leader细胞群体。这表明EMT和leader细胞签名的一致表达动态不仅仅是时间上的巧合,支持间充质特征的逐渐获得与leader-follower细胞命运决定平行的观点。
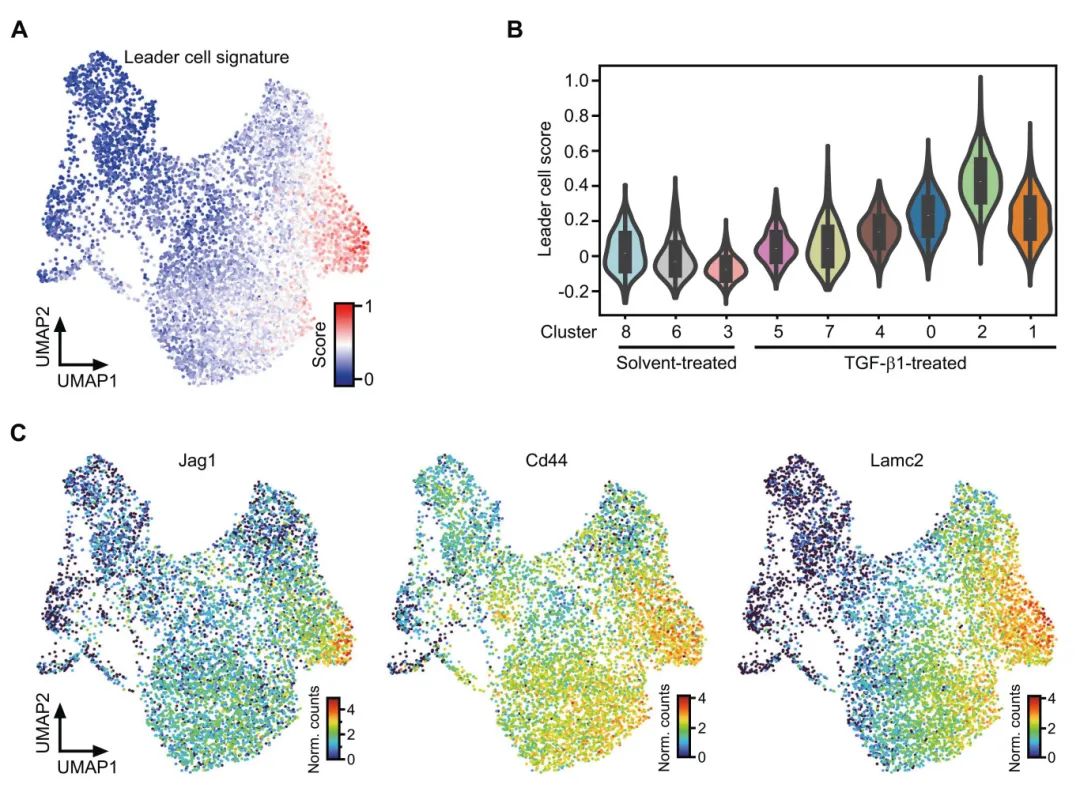
图2 处于最先进pEMT状态的细胞表现出leader细胞的特征
3) Sox11在pEMT高表达细胞中的关键作用:通过分析先前收集的bulk RNA-seq数据集,研究者寻找差异表达的转录因子。在上调的转录因子基因中,Sox11因在bulk RNA-seq数据中显示最高的fold change而突出,并且在scRNA-seq cluster 2细胞中特别丰富。SCENIC工作流程评估显示Sox11调节子在cluster 2中具有最高的活性评分。为验证转录组学分析结果,研究者在Sox11基因中插入FKBP12F36V盒与双血凝素(HA)表位标签,创建Sox11-HA融合蛋白。免疫荧光染色显示,溶剂处理的对照组均为阴性,而在TGF-β1处理的TKA类器官最外层三到四行细胞的细胞核中检测到Sox11-HA,确认了pEMT高表达细胞位于类器官侵袭前沿。
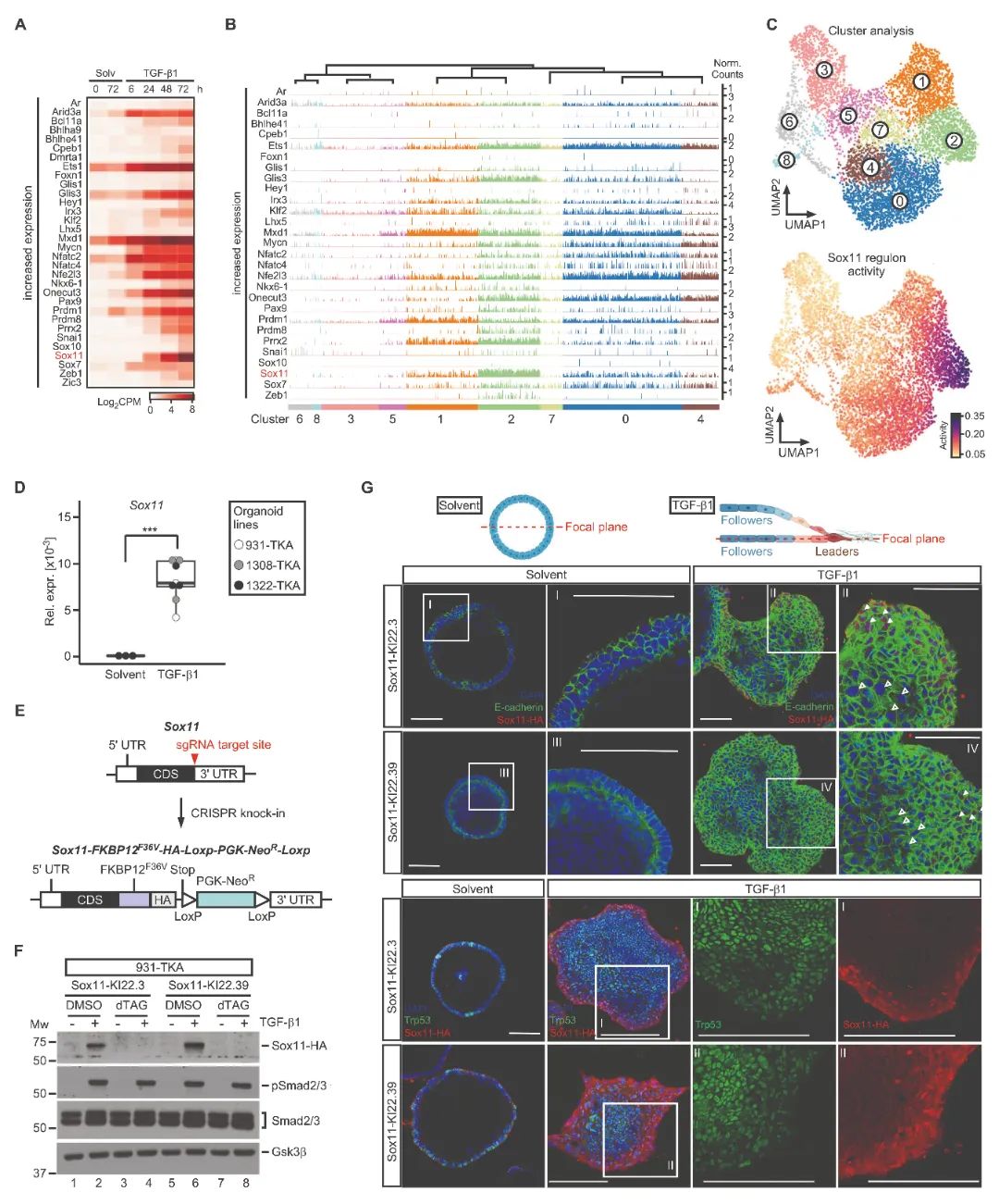
图3 Sox11是簇2细胞中表达最高的tgf-β1诱导转录因子,定位于TKA类器官侵袭前沿的一层细胞
4) Sox11对TGF-β1诱导的集体侵袭和pEMT的必要性:研究者通过删除大部分翻译区域(包括编码HMG-box的部分)在三个不同的TKA类器官系中敲除Sox11。功能丧失实验显示,Sox11 KO类器官不能像对照类器官那样扁平化和扩散,在某些情况下显示解体迹象。Sox11失活也损害了侵袭能力,并减少了TGF-β1介导的上皮和间充质标记物的上调。然而,Sox11过表达实验显示,仅Sox11过表达不足以引发pEMT和集体侵袭,Sox11HA过表达的TKA类器官保持与对照类器官相同的囊性形状,也不能增强类器官侵袭性或改变TGF-β1诱导的侵袭。这些结果表明,虽然Sox11不能作为自主EMT诱导因子,但它是TGF-β信号传导促进pEMT和TKA类器官集体侵袭的必要效应因子。
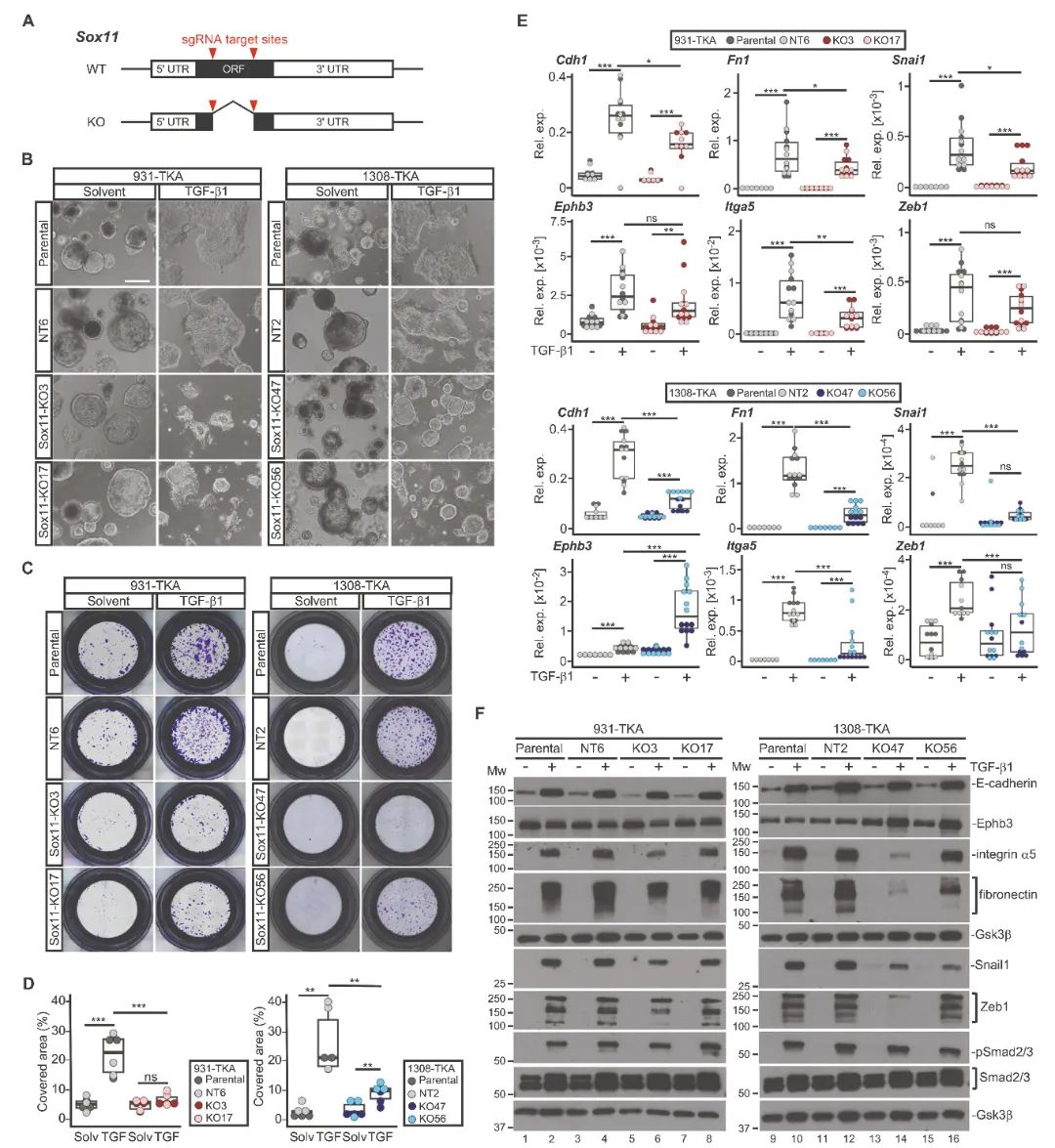
图4 Sox11是TGF-β1诱导的pEMT和集体侵袭所必需的
5) Sox11对基础和TGF-β1刺激基因表达的双重影响:为全面表征TKA类器官中Sox11依赖的转录组,研究者进行了RNA-seq分析。主成分分析显示,样本沿PC1的分离很可能反映TGF-β1反应,而Sox11 WT和KO样本沿PC2的分离暗示Sox11对基因表达的额外、TGF-β1独立影响。总体而言,Sox11 KO导致异常减少和增加的基因表达,表明Sox11在TKA类器官中既作为转录激活因子又作为抑制因子。聚焦于TGF-β1反应,cluster 8和9包含在TGF-β1处理的Sox11突变TKA类器官中表达减少的基因,其中包括与EMT、TGF-β和Pdgf信号传导、肌动蛋白-肌球蛋白纤维动力学和leader细胞签名组成部分相关的几个基因。在检查TGF-β1天真类器官中Sox11依赖的基因表达时,发现Sox11缺陷减少了几个肿瘤抑制因子和参与肠道功能和代谢的基因的表达。
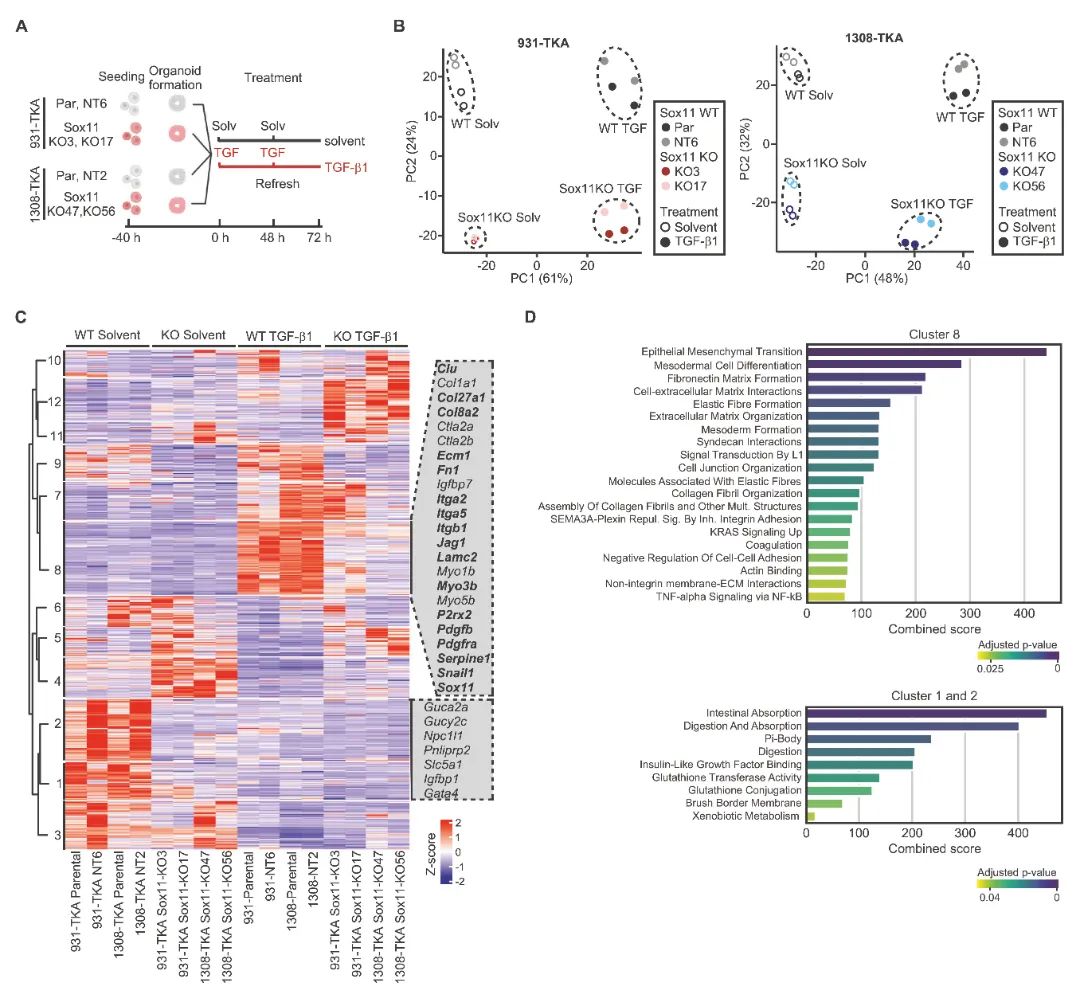
图5 RNA序列显示了Sox11在静息和TGF-β1刺激的类器官细胞中的多种功能
6) 人类CRC中SOX11表达升高与生存率降低的相关性:为确定TKA类器官的发现是否与人类疾病相关,研究者从TCGA队列中检索了健康组织和CRC样本的基因表达数据。尽管未分层肿瘤样本中的SOX11表达并不显著高于正常组织,但SOX11表达在肿瘤进展过程中稳步增加。较高的SOX11表达与总生存期缩短和无病间隔缩短相关。值得注意的是,在TKA类器官中显示Sox11依赖表达的几个与EMT、TGF-β和PDGF信号传导相关基因的人类同源物在TCGA样本中与SOX11表现出高度相关的表达,表明这些基因在人类癌症中也存在某种调控关系。最后,在结肠和直肠腺癌样本的CMS分层中,与CMS2样本相比,SOX11和其他几个基因的表达在CMS4中升高,这与TKA类器官转录谱的TGF-β1诱导的CMS2到CMS4转换一致。
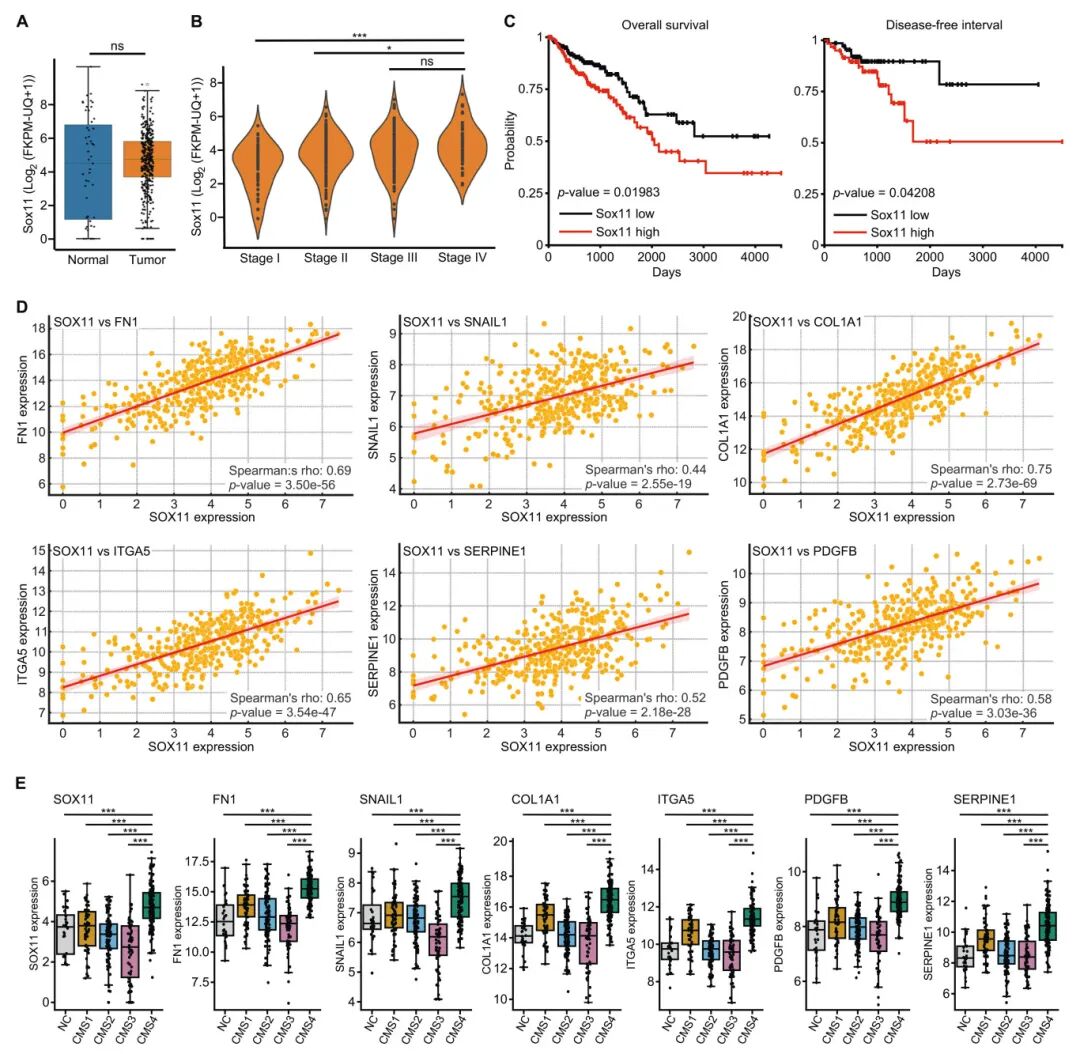
图6 SOX11表达量越高,结肠直肠腺癌的生存时间越短
本研究建立了TKA类器官作为研究非原型pEMT的重要实验模型,该模型精确复制了体内pEMT的几个关键特征,包括上皮标记物的持续表达、对单个核心EMT转录因子的独立性以及EMT的不完全执行。这为理解癌症转移的细胞可塑性机制提供了新的工具。系统性地揭示了Sox11作为TGF-β1诱导的pEMT和集体侵袭的关键调节因子的作用机制。Sox11不仅在TGF-β信号传导中发挥重要作用,还具有维持肠道组织稳态和肿瘤抑制的功能,这表明Sox11可能在TGF-β诱导下从潜在的肿瘤抑制因子转换为肿瘤促进因子。在临床意义上,SOX11在人类结直肠癌中的表达与不良预后相关,且与间充质标记物表达高度相关,提示SOX11可能成为新的治疗靶点。研究为理解癌症细胞pEMT状态与集体侵袭的机制联系提供了重要见解,有助于开发针对癌症转移的新型治疗策略。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:器官芯片体外建模器官间串扰:多器官芯片研究心血管-肾脏-代谢综合征
下一篇:PYY在炎症性肠病中对SATB2缺乏引起的肠道黏膜缺损的保护作用