常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-08-12 17:52:28 细胞资源库平台 访问量:402
人体气道内壁由两个生理功能不同的区域组成:表面气道上皮(SAE)和黏膜下腺(SMG)。表面气道上皮主要包含基底细胞、纤毛细胞、杯状细胞和产生MUC5AC的黏液细胞,作为物理屏障并促进黏液纤毛清除。相比之下,黏膜下腺主要分布在气管和大支气管的软骨性气道中,主要由产生MUC5B的黏液细胞、浆液细胞、基底细胞和肌上皮细胞组成。黏膜下腺负责分泌黏液和各种抗菌肽,对维持气道湿度和抵御病原体至关重要。
近年来研究表明,黏膜下腺在小鼠气道损伤后的修复和再生中发挥重要作用,提示其可能是多能干细胞的储存库,能够分化为多种气道细胞类型。这种再生能力使黏膜下腺在健康和疾病状态下都具有重要意义,特别是在慢性阻塞性肺病(COPD)等疾病中,气道重塑和慢性炎症非常普遍。事实上,黏膜下腺肥大被认为是COPD气道的主要病理生理变化之一,导致黏液分泌过多、气道阻塞和肺损伤加重。
尽管黏膜下腺具有重要作用,但除了来自人类或动物模型的短期外植体培养外,一直缺乏来自成体组织的强健体外黏膜下腺模型。基于类器官的人体气道疾病建模主要集中在更易获得的表面气道上皮上。考虑到黏膜下腺在黏液产生和宿主防御中的重要作用,建立来自原代支气管组织的人体黏膜下腺类器官模型对于研究气道再生、炎症和病毒感染具有重要意义。
近期,发表在Cell Stem Cell期刊上一篇题为Human airway submucosal gland organoids to study respiratory inflammation and infection的研究论文建立的人体气道黏膜下腺类器官模型为研究气道生理病理学提供了新的平台。该模型成功重现了黏膜下腺的关键特征,特别是产黏液细胞和肌上皮细胞,填补了气道疾病建模领域的重要空白。通过与表面气道上皮类器官的比较研究,揭示了两种气道区域对炎症和感染的不同反应模式,为理解COPD、哮喘等呼吸系统疾病的发病机制提供了新的视角。
1,黏膜下腺类器官的建立与表征:研究者优化了现有的气道组织处理方案,采用两步酶消化法首先从支气管组织中分离表面气道上皮,随后从黏膜下肌纤维中释放黏膜下腺。成功从7个独立供体建立了表面气道上皮和黏膜下腺类器官,并在定制培养基中分别培养。培养28天后,黏膜下腺类器官包含PAS阳性和MUC5B阳性的黏液细胞,而表面气道上皮类器官主要由基底细胞、纤毛细胞和较少的产黏液细胞组成。与天然组织一致,黏膜下腺黏液细胞主要表达MUC5B,而表面气道上皮黏液细胞同时表达MUC5AC和MUC5B。
2,单细胞转录组学验证细胞异质性:为了验证类器官模型与其组织对应物的相似性,研究者对培养第28天的类器官进行了单细胞RNA测序,并与已发表的人体气道上皮组织数据集整合分析。结果显示,来源于类器官的细胞与其组织对应物密切聚类,证实了模型的准确性。黏膜下腺类器官主要包含黏膜下腺基底细胞(44.3%)和黏膜下腺分泌细胞(4.1%),而表面气道上皮类器官主要包含表面气道上皮基底细胞、分泌细胞和杯状细胞。研究还鉴定出ANPEP/CD13是黏膜下腺分泌细胞的特异性表面标记物,并通过流式细胞术和免疫荧光染色得到验证。
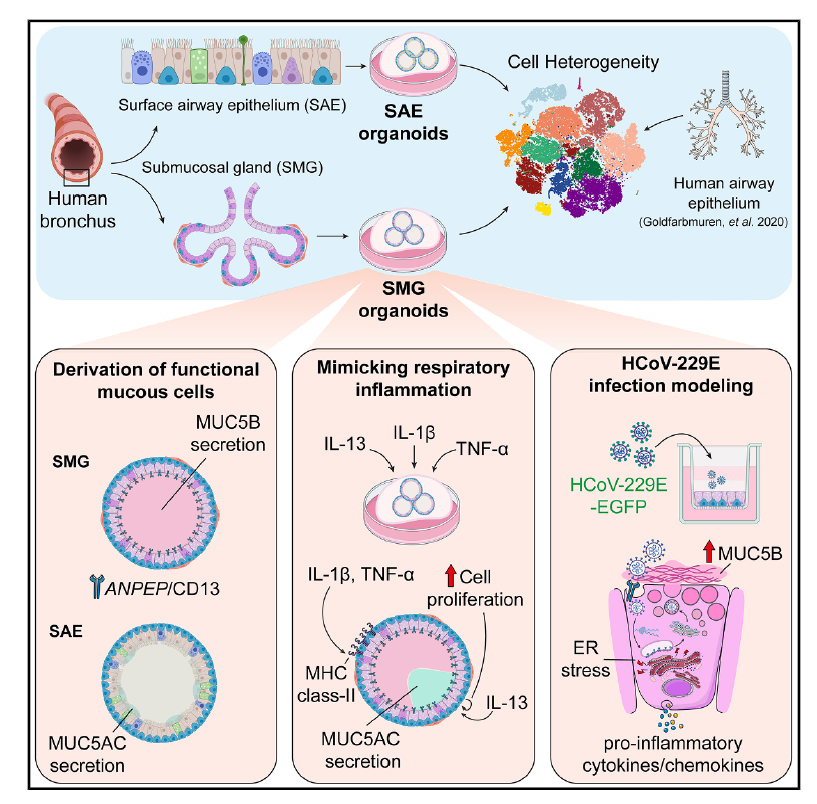
图1 流程示意图
3,肌上皮细胞的存在与功能:黏膜下腺的一个重要特征是肌上皮细胞的存在,这些特化的上皮细胞位于腺体上皮和基底膜之间,表达平滑肌标记物如α-SMA和肌球蛋白。通过基于已报道标记物的肌上皮细胞评分,研究者在黏膜下腺基底细胞群中鉴定出小群肌上皮细胞,占黏膜下腺类器官细胞的2.2%,与组织中的3.1%相近。这些细胞保持平滑肌细胞标记物的表达,并通过α-SMA免疫染色得到进一步确认。研究还发现CD200是肌上皮细胞的富集表面标记物,并验证了其在标记黏膜下腺类器官中肌上皮细胞的特异性。
4,炎症因子的差异性反应:为了阐明黏膜下腺对炎症刺激的独特反应,研究者将黏膜下腺类器官暴露于IL-1β、TNF-α或IL-13中。结果显示,IL-1β和IL-13显著降低了CD13阳性细胞的百分比,而TNF-α没有显著影响。转录组学分析揭示了不同细胞因子特异性的基因程序:IL-1β和TNF-α共同诱导先天免疫和抗原呈递通路,特别是主要组织相容性复合体II类(MHC II类)基因的表达。IL-1β特异性诱导急性期血清淀粉样蛋白A(SAA)基因SAA1和SAA2的表达,这些被用作气道炎症的生物标志物。值得注意的是,IL-13显著抑制了CD13阳性黏膜下腺细胞中MUC5B的表达,同时增强了MUC5AC的表达,这与Th2高表型哮喘患者的临床观察一致。
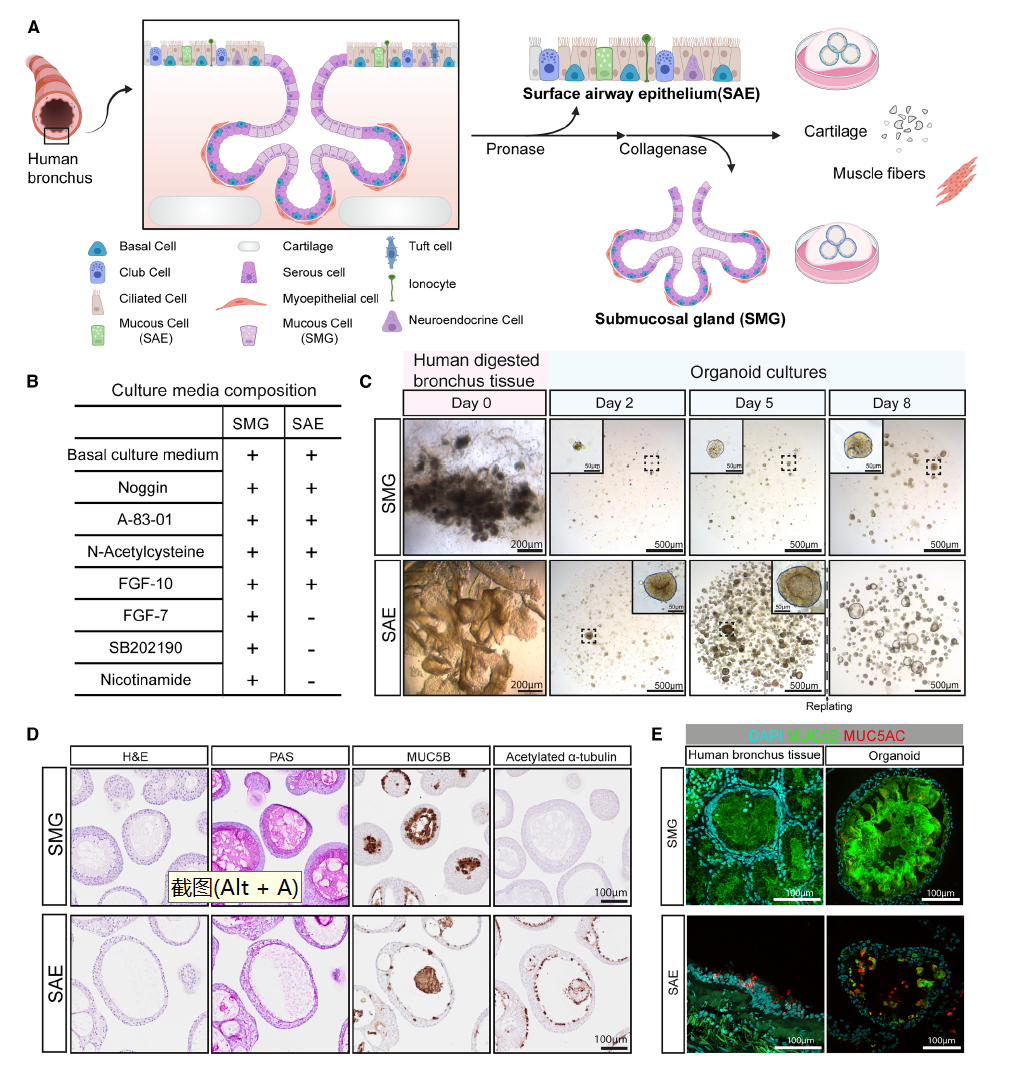
图 2 人类支气管 SMG 类器官的建立与表征
5,病毒感染的靶向性研究:研究者使用表达EGFP的人类α冠状病毒229E(HCoV-229E-EGFP)进行感染实验,发现HCoV-229E主要感染CD13阳性的黏膜下腺分泌细胞。在黏膜下腺转孔培养物中,30-60%的CD13阳性细胞被感染,而CD13阴性细胞的感染率低于1%。使用抗CD13抗体预处理显著降低了HCoV-229E的感染性,证实了CD13作为病毒进入受体的功能作用。感染的CD13阳性细胞主要表现出细胞病变效应,转录组学分析显示这些细胞上调了内质网应激和未折叠蛋白反应相关基因,包括中心调节因子DDIT3/CHOP、EIF2AK3/PERK和HSPA5/BiP。感染还适度增加了黏膜下腺培养物中MUC5B和MUC5AC的分泌,而表面气道上皮培养物保持不受影响。
6,多能性验证与分化潜能:为了评估人体黏膜下腺细胞的谱系可塑性,研究者将黏膜下腺来源的类器官在表面气道上皮培养基中培养。在这些条件下,类器官表现出纤毛细胞标记物FOXJ1表达的增加,乙酰化α-微管蛋白免疫染色确认了顶端表面纤毛细胞的存在,表明从产黏液向纤毛细胞分化的转变。相反,在黏膜下腺培养基中培养的表面气道上皮类器官显示MUC5AC和MUC5B表达上调,但仍保持纤毛细胞分化。这些结果表明,虽然环境信号可以影响分化并促进部分表型转换,但来自每个区域的干细胞的内在身份继续指导其谱系潜能。
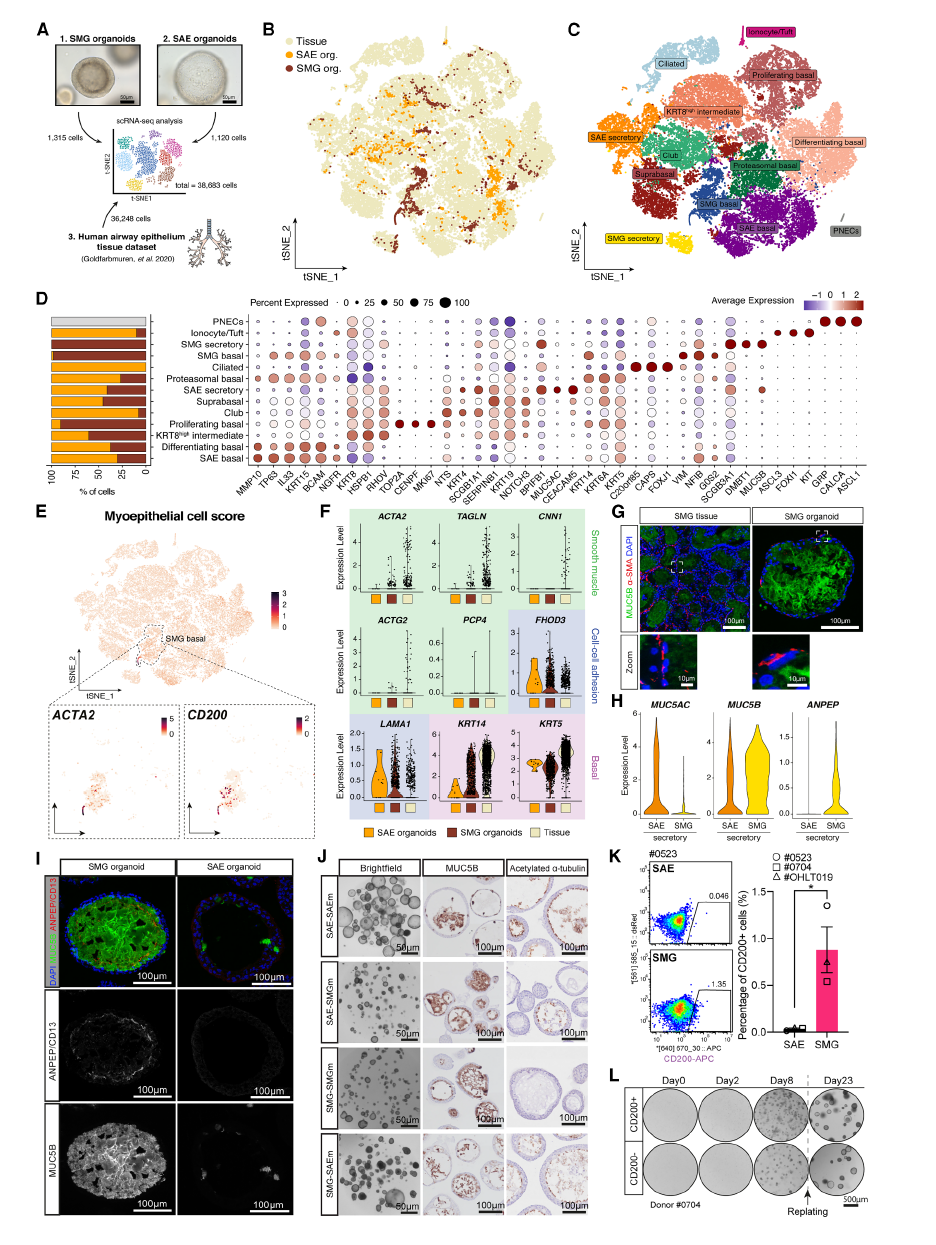
图 3 人类支气管 SMG 类器官、SAE 类器官与原代气道组织的整合单细胞 RNA 测序(scRNA-seq)图谱
该研究发现的ANPEP/CD13作为黏膜下腺分泌细胞特异性标记物,以及HCoV-229E对CD13阳性细胞的选择性感染,为理解冠状病毒感染的细胞靶向性和病毒驱动的气道损伤机制提供了重要见解。这对于开发针对呼吸道病毒感染的治疗策略具有重要指导意义。此外,该模型在药物筛选、个性化医疗和再生医学研究中具有广阔的应用前景,有助于推动呼吸系统疾病的精准治疗和新型疗法的开发。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
下一篇:CD19 CAR-T 细胞治疗大 B 细胞淋巴瘤后的感染问题:来自 CIBMTR 的真实世界分析