常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-07-24 17:33:59 细胞资源库平台 访问量:397
常染色体隐性遗传多囊肾病(ARPKD)是一种严重的发育性囊性肾脏疾病,发病率约为1/20000,具有高发病率和死亡率特征。ARPKD在围产期表现突出,30%的患者在出生后一个月内死亡,存活者平均在26岁时需要透析或肾移植治疗。该疾病被认为是典型的发育性肾囊性疾病原型,由PKHD1基因双等位基因突变引起,该基因编码纤维囊蛋白(FPC)。
在肾脏中,FPC定位于肾小管上皮细胞的初级纤毛,可能参与多囊蛋白复合体的钙离子通道功能。ARPKD和成人型多囊肾病(ADPKD)的共同病理机制是细胞内钙离子紊乱激活腺苷酸环化酶(AC),催化环磷酸腺苷(cAMP)合成,从而激活依赖cAMP的致囊通路。
尽管对PKD分子机制的理解不断深入,但针对疾病进展的靶向治疗仍然匮乏。特别是ARPKD目前尚无FDA批准的治疗药物,这可能与动物模型的局限性影响药物发现相关。现有的多种Pkhd1突变小鼠模型未能很好地重现人类发育表型,往往表现为有限的肾脏病变。因此,建立有效的临床前模型来识别发育性PKD中的致囊刺激因子存在重要科学缺口。
近十年来,人多能干细胞(PSC)衍生的肾脏类器官作为遗传性和非遗传性肾脏疾病的潜在人体外模型备受关注。hPSC衍生的肾脏类器官是类似于早期妊娠中期胎儿肾脏的发育性人类肾脏模型,已被用于ARPKD建模研究。
近期,发布在American journal of physiology. Renal physiology期刊,题为Kidney organoids demonstrate that PTH1R drives a cystogenic cAMP-pPKA-pCREB axis 2 in developmental Polycystic Kidney Disease的文章证明了肾脏类器官作为体外模型的效用,以探索缺乏忠实动物模型的罕见疾病的病理机制。
1,类器官模型建立与表型验证
研究团队利用CRISPR突变的iPSC构建了PKHD1-/-类器官及其同源对照,通过质量控制免疫染色确认第8天SIX2+肾元祖细胞诱导和第21天类器官中足细胞、近端小管和远端小管的存在。与之前ADPKD类器官研究类似,贴壁培养未能在野生型和突变类器官中诱导明显囊肿形成,证明微环境在人类PKD中的关键作用。而ARPKD类器官在高剂量福斯可林(20μM)处理下发生囊性结构形成,可通过明场显微镜观察到,且福斯可林处理的野生型类器官缺乏类似囊肿,建立了基因型-表型相关性。
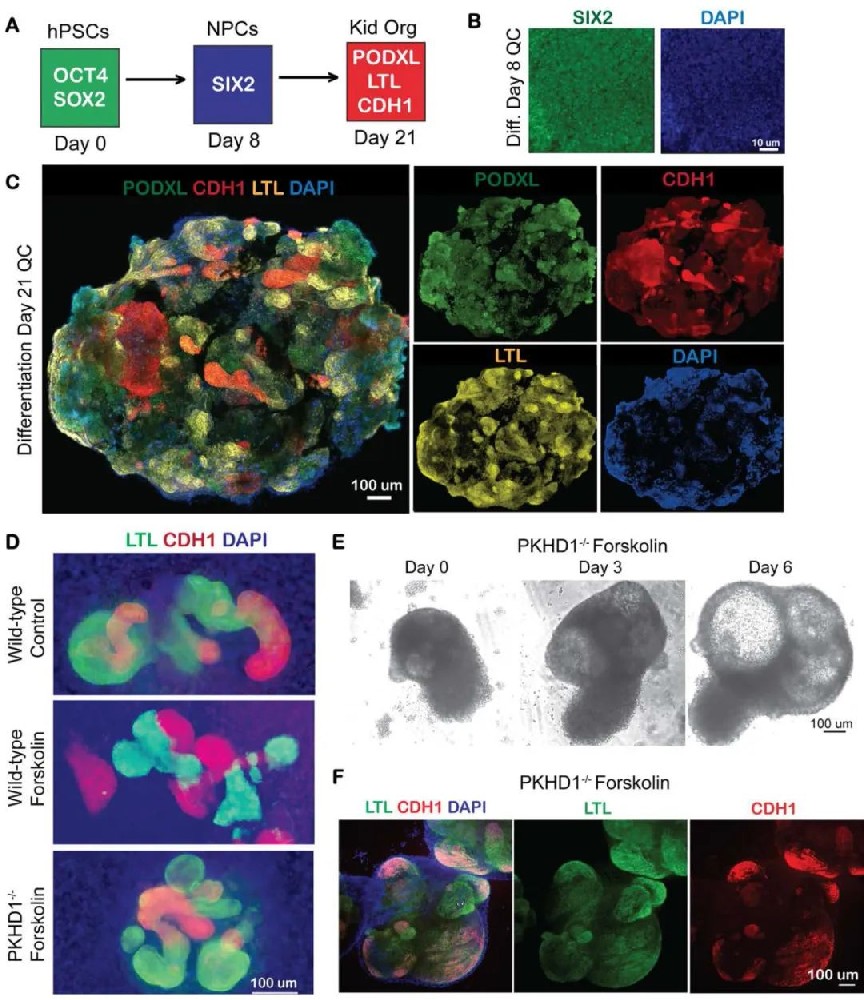
图1 悬液培养介导ARPKD类器官的囊肿形成效应
2,福斯可林的剂量依赖性致囊效应
ARPKD类器官接受连续低剂量福斯可林处理(1和10μM)4天后,显示剂量依赖性的囊肿形成。10μM处理组显示1.503±0.198倍增长(p=0.0022),1μM处理组为1.399±0.301倍增长(p=0.0259),而载体对照组相对无变化(0.999±0.228倍)。全细胞免疫染色的三维重建显示,LTL+近端小管和CDH1+远端小管均发生囊性扩张。最大小管直径测量显示福斯可林处理组达到130.68±17.64μm(p=0.0097 vs对照组),证实了囊肿形成。
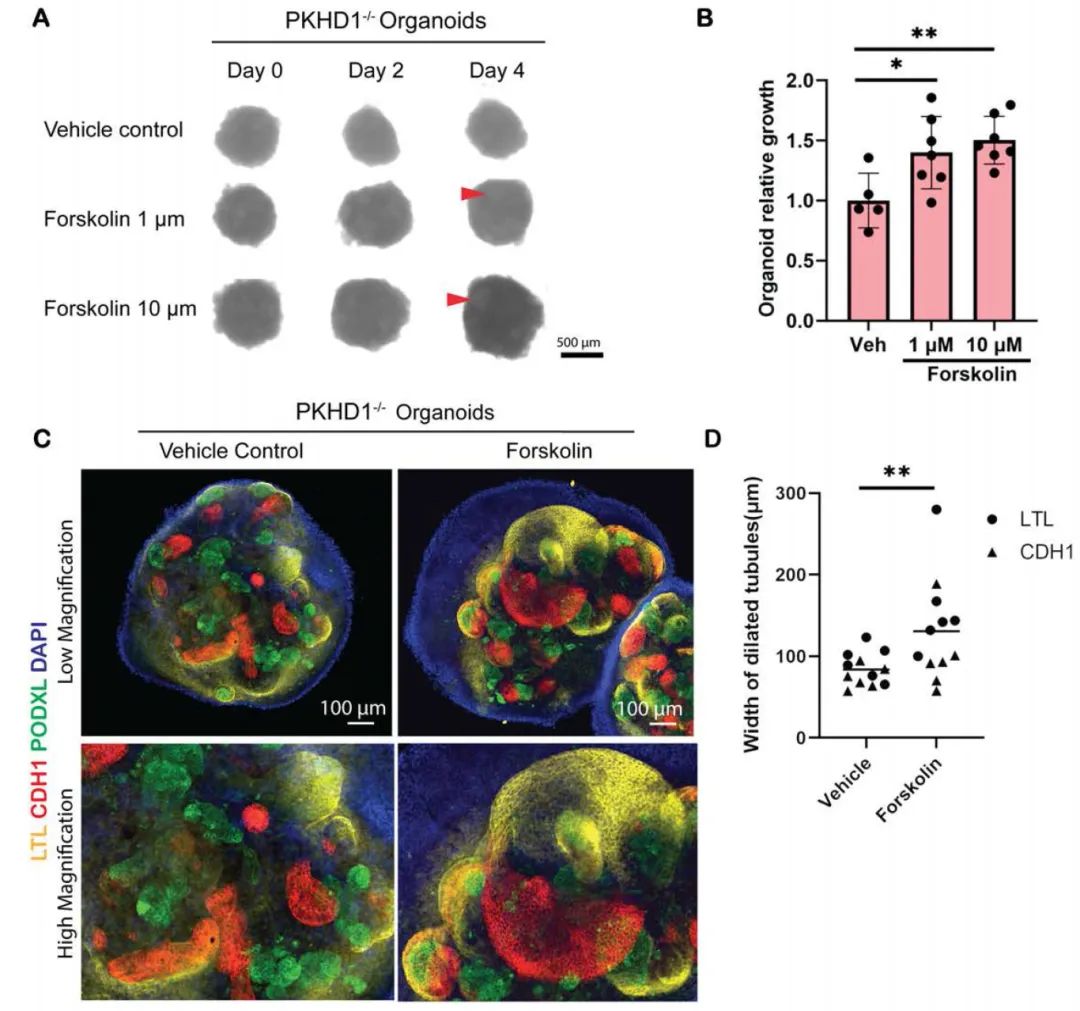
图2 福斯科林介导ARPKD类器官中剂量依赖性的膀胱形成
3,PTH受体在类器官中的表达鉴定
通过单细胞RNA测序筛选野生型肾脏类器官中表达的Gαs-GPCR,研究发现甲状旁腺激素受体PTH1R和PTH2R在肾元上皮细胞簇中具有特异性和可变表达。蛋白质水平检测显示PTH1R在LTL+和CDH1+小管中呈阳性,而PTH2R表达较少。为验证类器官是否忠实复制了PTH1R和PTH2R的细胞类型特异性表达,研究团队进一步检测了原生人类肾脏中的相关表达模式。
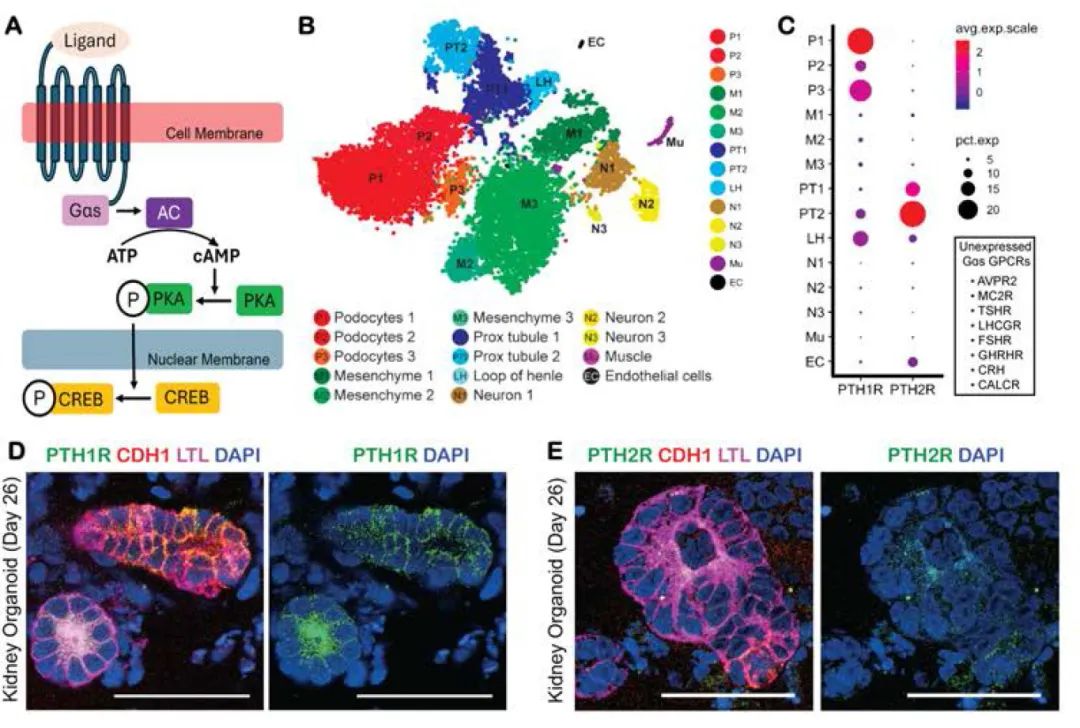
图3 PTH受体是肾脏类器官表达的Gαs-GPCR
4,原生肾脏和ARPKD患者组织中的PTH受体表达
利用肾脏精准医学项目(KPMP)的数据,研究分析了28名健康参照人群的汇总scRNA测序数据,包含225,177个肾脏细胞。结果显示PTH1R和PTH2R沿整个肾元表达,包括足细胞、近端小管、亨利袢和远端小管,表达模式倾向于近端肾元PTH1R和远端PTH2R。更重要的是,在一名4日龄死亡ARPKD患者的肾脏样本中,PTH1R和PTH2R在来源于LTL+近端小管和CDH1+远端小管的囊肿中均呈阳性表达。
5,PTH1R激动的致囊效应
研究使用内源性PTH1R和PTH2R激动剂处理ARPKD类器官:人重组PTH作为广谱激动剂,PTH相关肽(PTHrP)用于选择性PTH1R激动,管状下丘脑蛋白39(TIP39)用于选择性PTH2R激动。第28天ARPKD类器官接受载体、PTH(0.1和1.0μM)或PTHrP(0.1和1.0μM)处理4天后,1.0μM的PTH和PTHrP诱导类器官相对倍数增长分别为1.384±0.246(p=0.0259)和2.104±0.700(p=0.008511)。而PTH2R激动剂TIP39未能诱导类器官增长,提示PTH1R在致囊过程中的特异性作用。
图4 PTH1R和PTH2R在原生肾小管和ARPKD囊肿中表达
6,cAMP-pPKA-pCREB轴的机制验证
为机械性探究PTH诱导的cAMP-pPKA-pCREB轴是否负责囊肿形成,研究进行了靶向顺序抑制研究。使用腺苷酸环化酶抑制剂(ACi, 2',5'-双脱氧腺苷)和PKA抑制剂(PKAi, KT5720)处理显示,10μM ACi将PTH介导的类器官相对倍数增长从1.553±0.261抑制至0.934±0.050(p=0.0218),10μM PKAi抑制至0.934±0.890(p=0.03087)。全细胞免疫染色验证显示,最大LTL+和CDH1+小管直径从PTH处理的118.02±11.33μm显著降低至ACi和PKAi处理的89.61±8.55μm和88.85±11.45μm,证实了PTH1R激动驱动依赖cAMP-pPKA-pCREB的致囊程序。
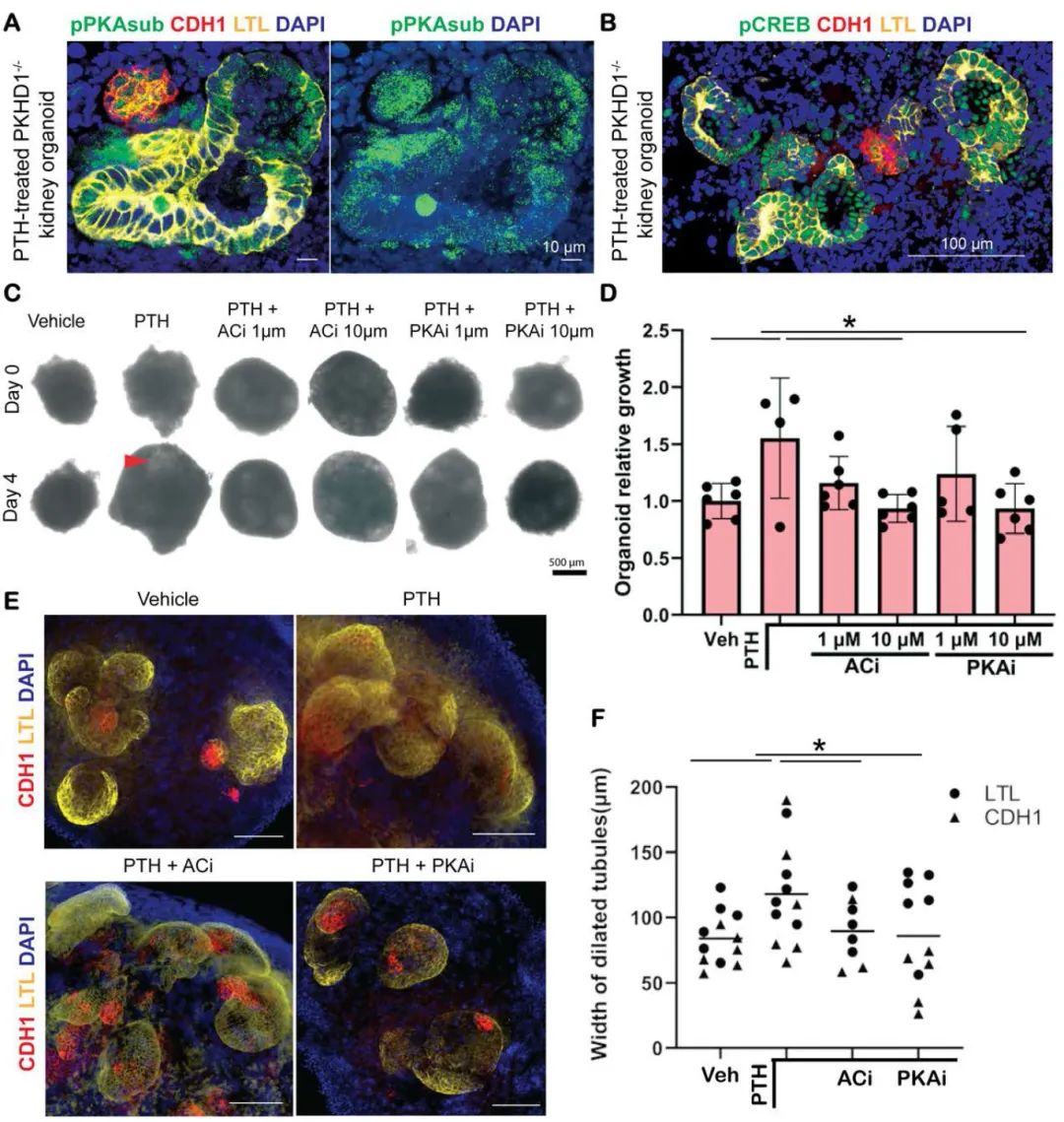
图5 PTH诱导的囊肿形成依赖于AC-pPKA-pCREB轴
本研究在人类干细胞衍生的ARPKD类器官中发现PTH1R作为一个新的致囊刺激因子,揭示了PTH1R激动能够驱动cAMP-pPKA-pCREB依赖性的囊肿形成机制。这一发现不仅扩展了我们对多囊肾病发病机制的理解,更重要的是为缺乏忠实动物模型的罕见疾病提供了有效的体外研究平台。从临床转化角度,该研究具有重要价值。研究发现的PTH1R激动作为福斯可林上游的信号,为沿GPCR-AC-cAMP-pPKA-pCREB轴的治疗候选药物测试提供了可能。
考虑到约35%的FDA批准药物调节GPCR活性,这一新的致囊机制可能支持使用商业化GPCR化合物库或FDA批准药物库进行治疗筛选。临床实践中,肾科医生已有使用拟钙剂和维生素D类似物治疗CKD继发性甲状旁腺功能亢进症的经验,证明PTH抑制在CKD中是安全可行的。本研究表明PTH抑制可能在PKD患者中具有治疗效果,值得进一步临床研究验证。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
下一篇:人参皂苷 Rb2 直击寨卡病毒,体内外实验证实强效抑制力