常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2025-07-22 21:26:59 细胞资源库平台 访问量:292
癌症是全球主要死因,根据世界卫生组织数据,2020年约有1000万人死于癌症,1900万人新确诊癌症。尽管癌症治疗取得显著进展,但目前仅少数患者能从基因检测和精准医学中获益。一方面,大多数已批准的抗癌药物具有重叠的临床适应症;另一方面,许多耐药机制由肿瘤表观遗传谱或微环境的适应性驱动,现有分子检测方法无法准确评估。因此,为每个病例确定最佳治疗方案仍然是医生和患者每天面临的难题。
传统的2D细胞培养无法捕获癌症的复杂性,不足以支持新化合物的合理开发、现有药物组合的测试或预测患者对治疗的反应。此外,新现象如抗体-药物偶联物(ADCs)的旁观者效应只能在复制癌细胞空间分布的3D结构中得到适当研究。基因工程动物模型和患者来源肿瘤异种移植(PDTX)虽然更接近肿瘤复杂性,但微环境会被小鼠细胞替代,且成本高昂、耗时且涉及动物伦理问题。
患者来源类器官(PDOs)作为三维培养模型,能够保持遗传异质性并密切模拟原始肿瘤的形态学特征。这些类器官通过从患者活检或手术样本中分离癌细胞,在特定培养基质中生长而产生。PDOs不仅可用于研究癌症生物学和测试潜在疗法,还可用于个体化患者治疗。然而,目前大多数研究专注于确定类器官的体外特征,而未分析其与原始患者真实结果的相关性。
近期,发布在Journal of experimental & clinical cancer research期刊,题为Multicenter study correlating molecular characteristics and clinical outcomes of cancer cases with patient-derived organoids的文章旨在从癌症患者不同来源和时间点的样本中建立药物敏感性数据集(PDOs)。通过对比这些样本与原发肿瘤在解剖病理特征及遗传背景上的差异,研究者评估了体外药物敏感性是否能真实反映多中心临床环境中病例随病程发展的实际疗效。只有这种将体外实验结果与真实临床结局直接对照的研究,才能为新药研发和精准医疗提供更优质的模型支持。

1, PDOs建立成功率及样本来源分析
本研究从184名患者(17种肿瘤类型)收集了249个样本,包括149个(59.8%)肿瘤组织样本、61个(24.5%)腹膜液样本和39个(15.7%)外周血样本。PDOs建立成功率分别为39.5%、34.4%和25.6%。研究发现,不同肿瘤类型的PDOs建立成功率存在差异,卵巢癌为33%,肾癌达68%。配对样本分析显示,来自同一患者的肿瘤组织和腹膜冲洗液的成功率分别为31.4%和28%,8例(16%)患者的肿瘤和腹膜冲洗液均成功建立PDOs。研究还发现,样本处理时间对某些肿瘤类型(如前列腺癌、卵巢癌)的PDOs建立至关重要,而对其他类型(如黑色素瘤)影响较小。
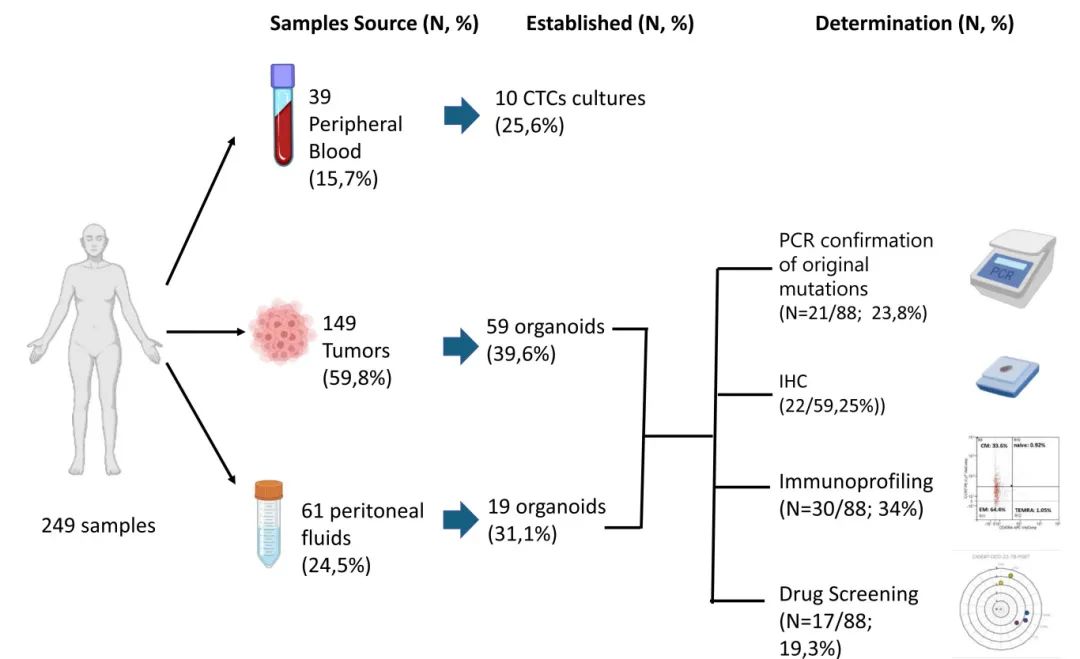
图1 用于建立和表征PDO的样品采集流程图
2, 免疫微环境分析与PDOs建立相关性
研究对31个肿瘤样本进行了流式细胞术分析,检测七种T细胞亚群,发现成功建立PDOs的样本显示肿瘤浸润淋巴细胞(TILs)富集(27.5% vs 10%,p=0.042)和中央记忆T细胞(TCM)富集(51.5% vs 26.5%,p=0.023)。相反,效应记忆T细胞(TEM)和调节性T细胞(Tregs)在建立失败的样本中富集,分别为63.62% vs 36.70%(p=0.009)和9.4% vs 1.65%(p=0.0045)。这些发现为PDOs建立的预测因子提供了重要线索,表明肿瘤免疫微环境的组成可能影响类器官培养的成功率。
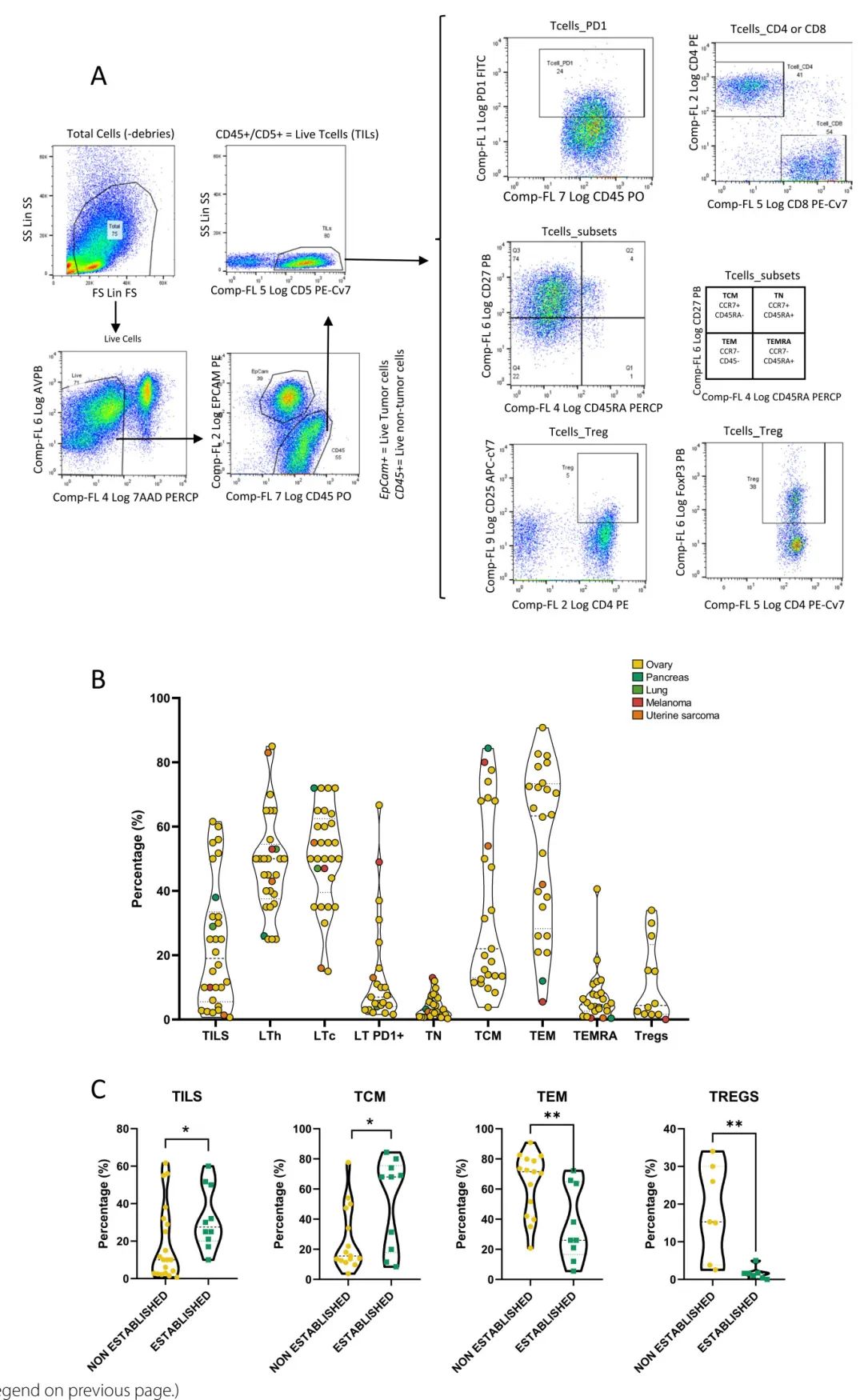
图2 研究源肿瘤的免疫浸润及与PDO建立的相关性的流式细胞术门控策略
3, 组织病理学和遗传特征保持性验证
22个PDOs达到足够的数量和大小进行免疫组织化学(IHC)分析,其中20个(91%)再现了相应肿瘤中观察到的组织学模式,并保持了IHC标记物的相似表达。为确认PDOs保持源肿瘤的遗传背景,研究从27个类器官中提取DNA,这些类器官的相应肿瘤已通过下一代测序(NGS)进行常规医学实践研究。PCR测序针对16个不同基因在25个(92.6%)PDOs中得以完成,21/25(84%)样本确认存在至少一个原始致病性变异。这些结果证实PDOs能够忠实保持原始肿瘤的病理特征和分子遗传学特征。
4, 药物敏感性与临床结果相关性分析
研究比较了13个PDOs(来自9例晚期疾病患者)的体外治疗反应与患者的真实临床结果。所有11个上皮性卵巢癌PDOs均测试了奥拉帕尼,病例#2和#6在样本获取时正在或曾经接受PARPi治疗,两名患者均显示临床反应不佳,相应地,两者均显示该系列中奥拉帕尼敏感性评分最低(0.5)。相反,病例#1、#5和#7为PARP naive,显示出更高的敏感性指数。铂类衍生物卡铂或顺铂在11个上皮性卵巢癌PDOs中的10个进行了测试,所有铂naive PDOs均来自接受卡铂作为新辅助治疗的三名患者的诊断性腹腔镜检查样本,三例病例均表现出临床部分缓解,其相应PDOs显示敏感性评分高于1。
5, 循环肿瘤细胞来源PDOs建立探索
从39名患者的外周血样本中,根据详细协议成功建立了10个PDOs(3个来自子宫内膜癌患者、3个来自卵巢癌患者、2个来自肾癌患者、1个来自膀胱癌患者和1个来自胰腺癌患者)。然而,这些PDOs未达到足够的大小或细胞数量进行进一步表征。研究发现,循环肿瘤细胞(CTCs)在血流中稀少、异质性强,存在不同的上皮-间质转化状态,血流环境对肿瘤细胞具有"敌意",这些因素都影响PDOs的建立成功率。
6, 免疫-类器官共培养系统建立
研究成功建立了患者来源类器官(PDOs)和自体肿瘤浸润淋巴细胞(TILs)的共培养系统来预测免疫治疗敏感性。从一名58岁男性肾癌患者获得1 cm³肿瘤样本,癌细胞按常规处理,同时分离、表征和扩增自体TILs。PDOs与TILs以不同比例(10:1或20:1)共培养,在伊匹单抗(抗CTLA4抗体)存在或不存在的情况下维持5天。结果显示,单独TILs共培养在10:1和20:1比例下导致类器官细胞死亡增加(分别为60.6%和17.2%),在20:1比例下伊匹单抗的存在进一步增强了这种活性(85.4% vs 17.2%细胞死亡,p=0.0134)。
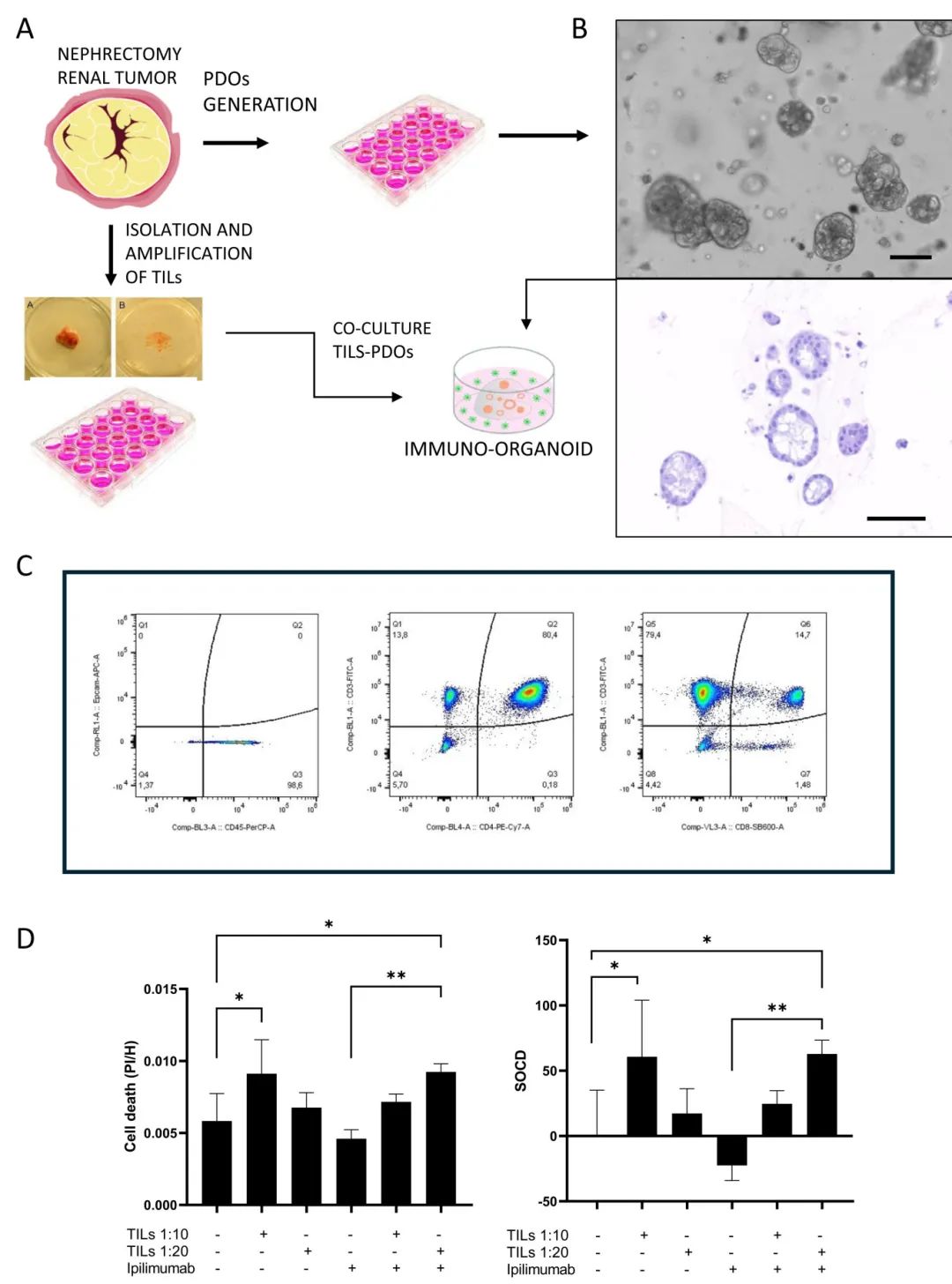
图3 免疫器官建立和检查点抑制剂检测
本研究在多中心环境下系统评估了不同来源PDOs的建立可行性及其与临床结果的相关性,为精准医学提供了重要的实验室工具。研究证实PDOs能够保持原始肿瘤特征、反映疾病进展并预测治疗反应,为分子检测在精准医学中的应用提供了有价值的补充模型。特别重要的是,研究展示了PDOs在罕见肿瘤治疗选择中的巨大潜力。罕见肿瘤占癌症诊断的约20%,通常预后较差,部分原因是缺乏新药物的获取途径。PDOs技术能够为这些患者筛选多种药理学选择,有助于解决这种不平等现象。
此外,免疫-类器官共培养系统的建立为免疫治疗的发展开辟了新的可能性,能够在体外模拟肿瘤-免疫相互作用,为个体化免疫治疗策略的制定提供重要参考。研究结果表明,PDOs技术有望成为连接基础研究与临床应用的重要桥梁,推动精准医学在癌症治疗中的实际应用。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:糖尿病伤口难愈合?研究证实:羊膜胶原水凝胶 + 槲皮素组合可加速修复,促再生还抗炎!
下一篇:子宫导管植入不良可能加重并发症,3D 计划为治疗精准护航