常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-05-04 17:00:00 细胞资源库平台 访问量:18
肾脏类器官作为模拟胎儿肾脏发育的体外模型,在肾病研究、药物毒性筛选中具有重要价值,但现有分化方案(如 Morizane 等 2017 年建立的 2D 分步 protocol)存在效率低、肾祖细胞比例不足、类器官成熟度不均等问题。人诱导多能干细胞(hiPSCs)处于 “始发态(primed)” 多能性,其分化潜能受细胞周期、表观遗传状态调控。此前研究发现低剂量二甲基亚砜(DMSO)可通过调控细胞周期(G1 期停滞)增强 hiPSCs 向三胚层分化,但 DMSO 对肾脏类器官分化的影响及机制尚未明确。
来自荷兰马斯特里赫特大学等机构的团队在《Stem Cell Reviews and Reports》上发表题为Dimethyl Sulfoxide Conditions Induced Pluripotent Stem Cells for more Efficient Nephron Progenitor and Kidney Organoid Differentiation的研究,证实1-2% DMSO 短期(24 小时)处理 hiPSCs可通过调节细胞周期、重塑表观遗传景观、优化集落形态,显著提高后肾间充质肾祖细胞(SIX2+)比例(最高达 92%)及肾脏类器官分化效率(1% DMSO 组类器官形成率 78%,对照 38%),为肾脏类器官的高效构建提供简单可行的优化策略。
1. hiPSC 培养与 DMSO 处理
细胞系与培养:使用 3 株 hiPSCs(LUMC:尿液来源;H101、H107:外周血单核细胞来源),在 1% Geltrex 包被板上用 mTeSRplus 培养基培养,传代时用温和解离试剂处理。
DMSO 处理:hiPSCs 按不同密度接种(LUMC 1×10⁴细胞 /cm²,H101 9×10³,H107 7×10³),培养 3 天后,用含 0%(对照)、1%、2% DMSO 的 mTeSRplus 处理 24 小时,随后启动肾脏类器官分化。
2. 肾脏类器官分化(基于 Morizane 等 2017 protocol 优化)
中胚层诱导(Day 0-4):DMSO 处理后,换用含 CHIR99021(Wnt 激动剂,LUMC 8μM、H101 10μM、H107 12μM)和 5ng/mL Noggin(BMP 抑制剂)的 Advanced RPMI 培养基,2 天换液 1 次;Day 4 换用含 10ng/mL Activin A 的培养基,持续 3 天。
肾祖细胞诱导(Day 7-9):Day 7 换用含 10ng/mL FGF9 的培养基,Day 9 观察到囊泡结构,提示后肾间充质(MM)肾祖细胞形成。
类器官成熟(Day 14-21):Day 14 换用基础 Advanced RPMI 培养基,每 2-3 天换液,Day 21 获得含肾小管结构的肾脏类器官。
3. 细胞特性检测
多能性评估:流式细胞术检测表面标志物(TRA-1-81、TRA-1-60、SSEA3/4)和 intracellular 标志物(SOX2、OCT4);qPCR 检测多能性基因(SOX2、OCT4、NANOG、c-Myc)。
细胞周期分析:PI 染色结合流式,检测 G0/G1、S、G2/M 期细胞比例;scRNA-seq 分析细胞周期相关基因(如 CCND1/2/3、CDKN1B)。
毒性与应激检测:LDH 释放实验评估细胞毒性;CellROX Green 检测活性氧(ROS);qPCR 检测热休克蛋白(HSPA5、HSP90B1)。
4. 肾祖细胞与类器官鉴定
肾祖细胞定量:Day 9 用流式细胞术检测 SIX2 + 细胞比例(肾祖细胞标志物);免疫荧光染色验证 SIX2 与 PAX2(后肾间充质标志物)共表达。
类器官成熟度评估:Day 21 手动计数类器官数量;免疫荧光检测肾小球标志物(Podocalyxin、Nephrin)、近端小管标志物(Megalin、LTL)、远端小管 / 集合管标志物(GATA3、E-cadherin);In-cell Western 定量关键蛋白表达。
5. 转录组与表观遗传分析
单细胞 RNA 测序(scRNA-seq):处理后 hiPSCs 经固定、分选后,用 10x Genomics 平台测序,分析多能性状态(naive/formative/primed)、表观调控基因(DNMT3A/B、TET 家族)及凋亡相关基因。
qPCR 验证:检测中胚层(TBXT、MIXL1)、中间中胚层(OSR1、LHX1、PAX2)标志物表达,验证分化定向性。
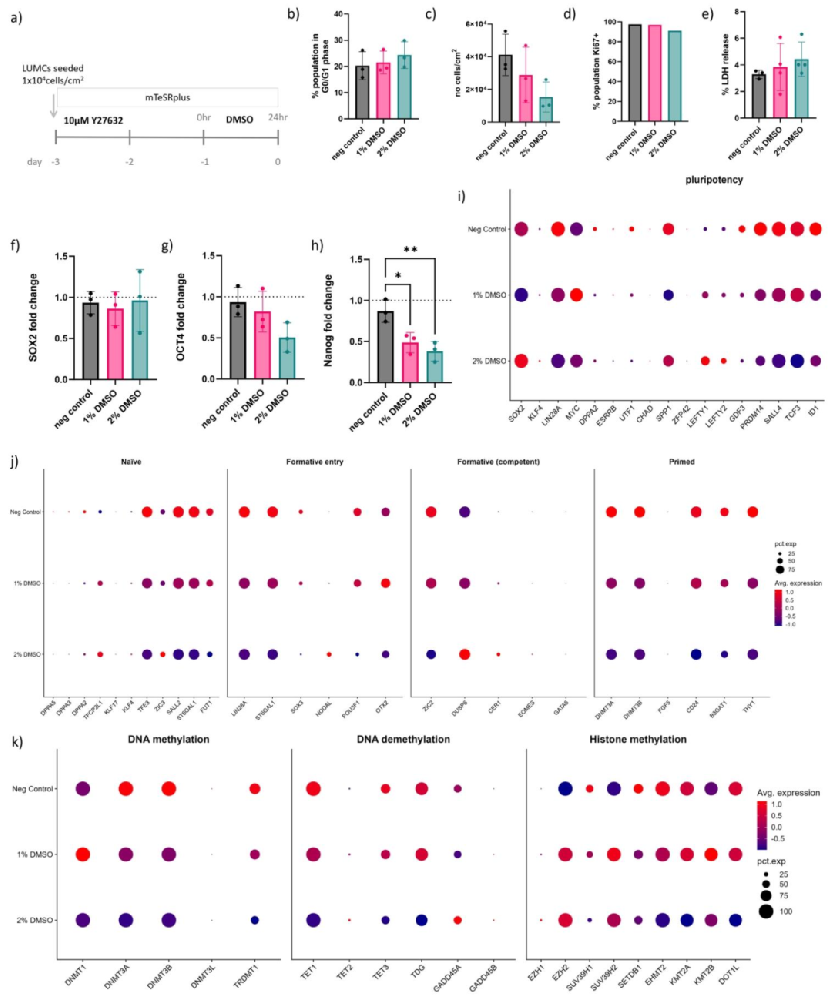
图1:DMSO 对 hiPSCs 多能性与细胞周期的影响
该图解析 DMSO 处理对 hiPSCs 基础特性的调控:A 为处理流程示意图,hiPSCs 接种 3 天后用 DMSO 处理 24 小时,Day 0 启动分化;B-C 显示,1-2% DMSO 处理使 G0/G1 期细胞比例显著增加(剂量依赖性),总细胞数减少,但 Ki67 + 增殖细胞比例无显著下降,提示 DMSO 诱导细胞周期停滞而非抑制增殖;D-E 显示,DMSO 处理后 LDH 释放增加(提示轻度细胞毒性),但 ROS 水平无变化,HSPA5(热休克蛋白)上调,证实存在轻度应激但无氧化损伤;F-I 为 qPCR 结果,SOX2、c-Myc 表达稳定,OCT4 轻度下降,NANOG 显著下调(2% DMSO 组最明显),说明多能性核心状态保留但 “过度增殖相关” 的 NANOG 表达降低;J-K 为 scRNA-seq 结果,DMSO 处理下调细胞周期基因(CCND1/2/3)、上调周期抑制剂 CDKN1B,同时下调表观调控基因(DNMT3A/B、TET 家族),证实 DMSO 通过 “G1 期停滞 + 表观重塑” 为分化做准备,且未诱导提前向三胚层分化(图S3f)。
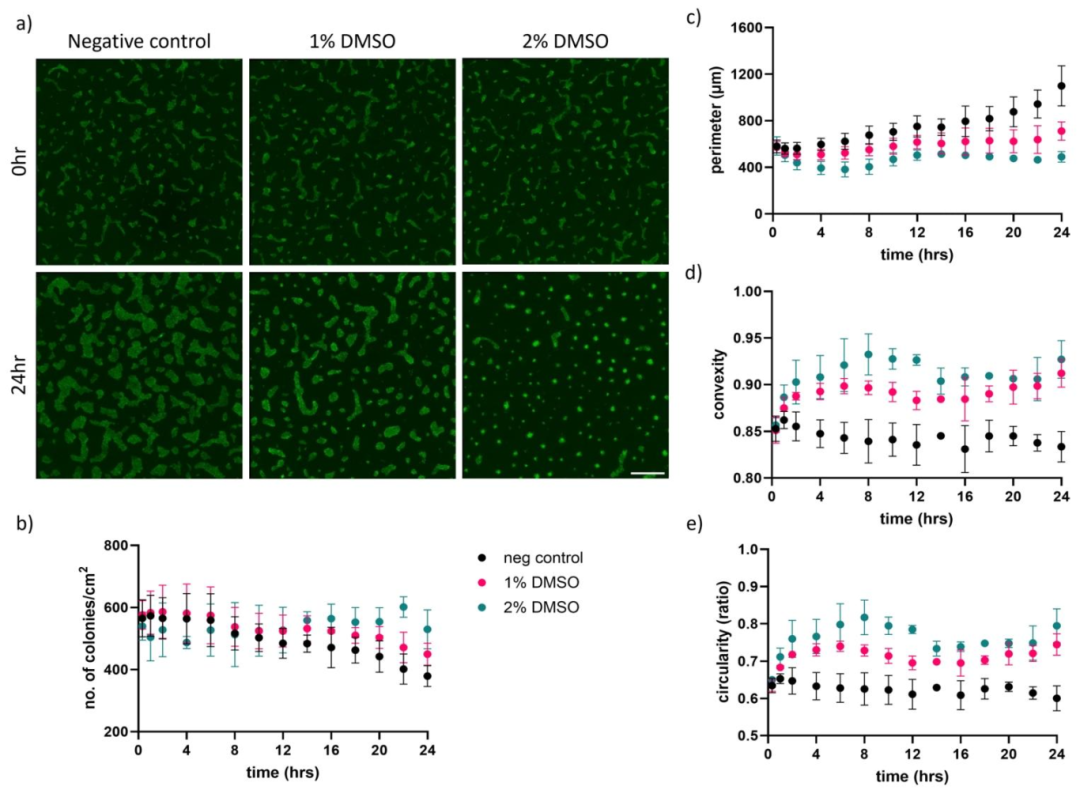
图2:DMSO 对 hiPSC 集落形态的动态影响
该图通过实时成像量化集落形态变化:A 为 LUMC-GFP+ hiPSCs 的荧光图像,0 小时各组集落形态相似,24 小时后 DMSO 组集落更紧凑、圆形度更高;B-E 为定量分析,1-2% DMSO 组集落数量增加( fewer 融合)、周长减少、凸度和圆形度显著升高(p<0.05)。集落的 “小而圆” 形态是 hiPSCs 分化潜能提升的典型特征 —— 边缘细胞比例增加,更易响应分化信号,为后续肾祖细胞分化奠定形态基础。
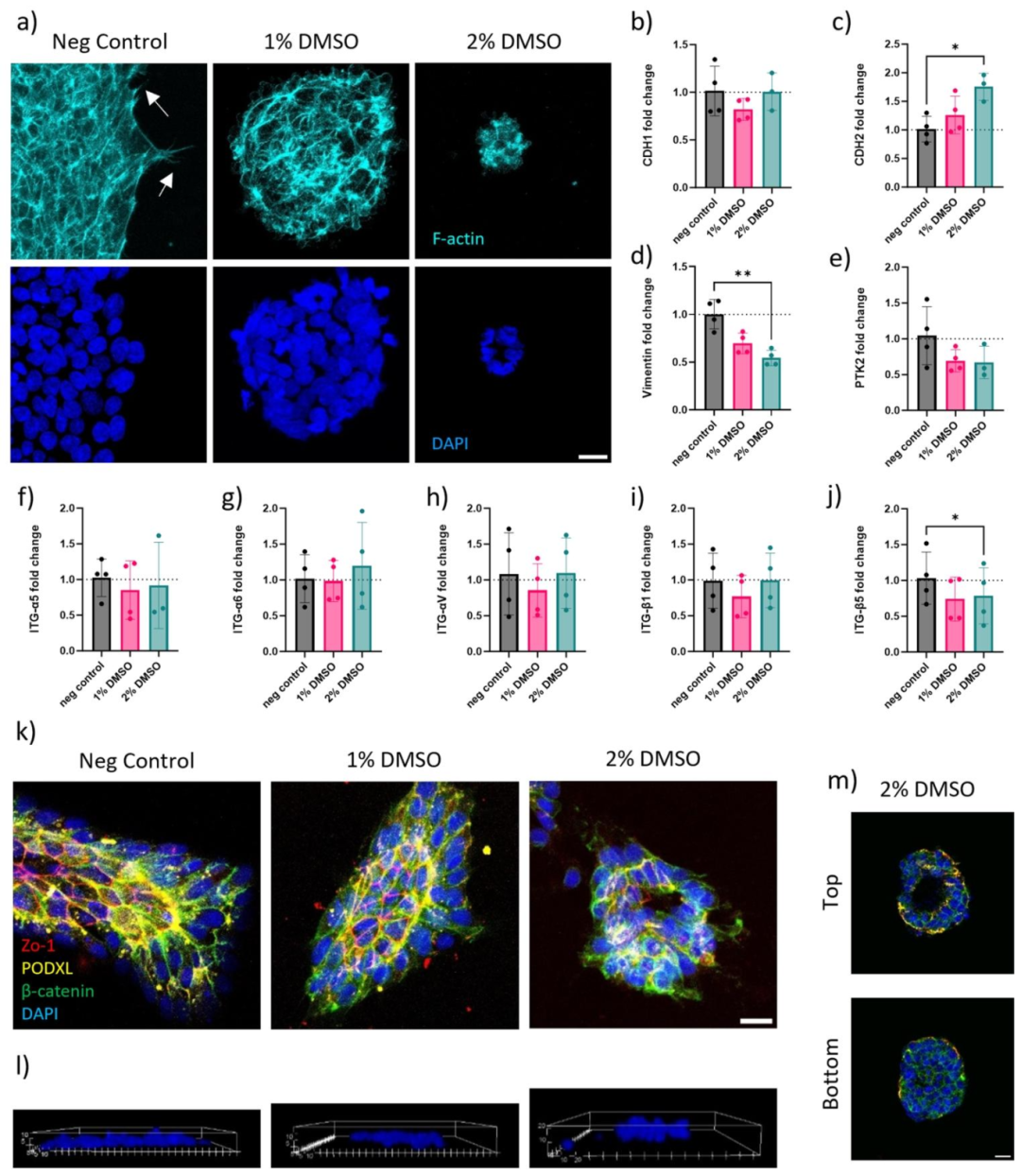
图3:DMSO 对 hiPSC 细胞结构与整合素表达的影响
该图揭示 DMSO 对细胞骨架与基质交互的调控:A 为 Phalloidin 染色(F-actin),DMSO 组集落边缘细胞突起减少( focal adhesion 减少), cytoskeleton 更紧凑;B-J 为 qPCR 结果,E-cadherin(细胞间黏附)稳定,N-cadherin 上调,PTK2( focal adhesion kinase)、Vimentin(间质标志物)及整合素 β1/β5 下调,证实 DMSO 通过调节细胞 - 基质黏附(如整合素下调)和细胞骨架重组,减少不必要的 focal adhesion,使细胞更易接受分化信号,而非维持自我更新所需的基质锚定状态。
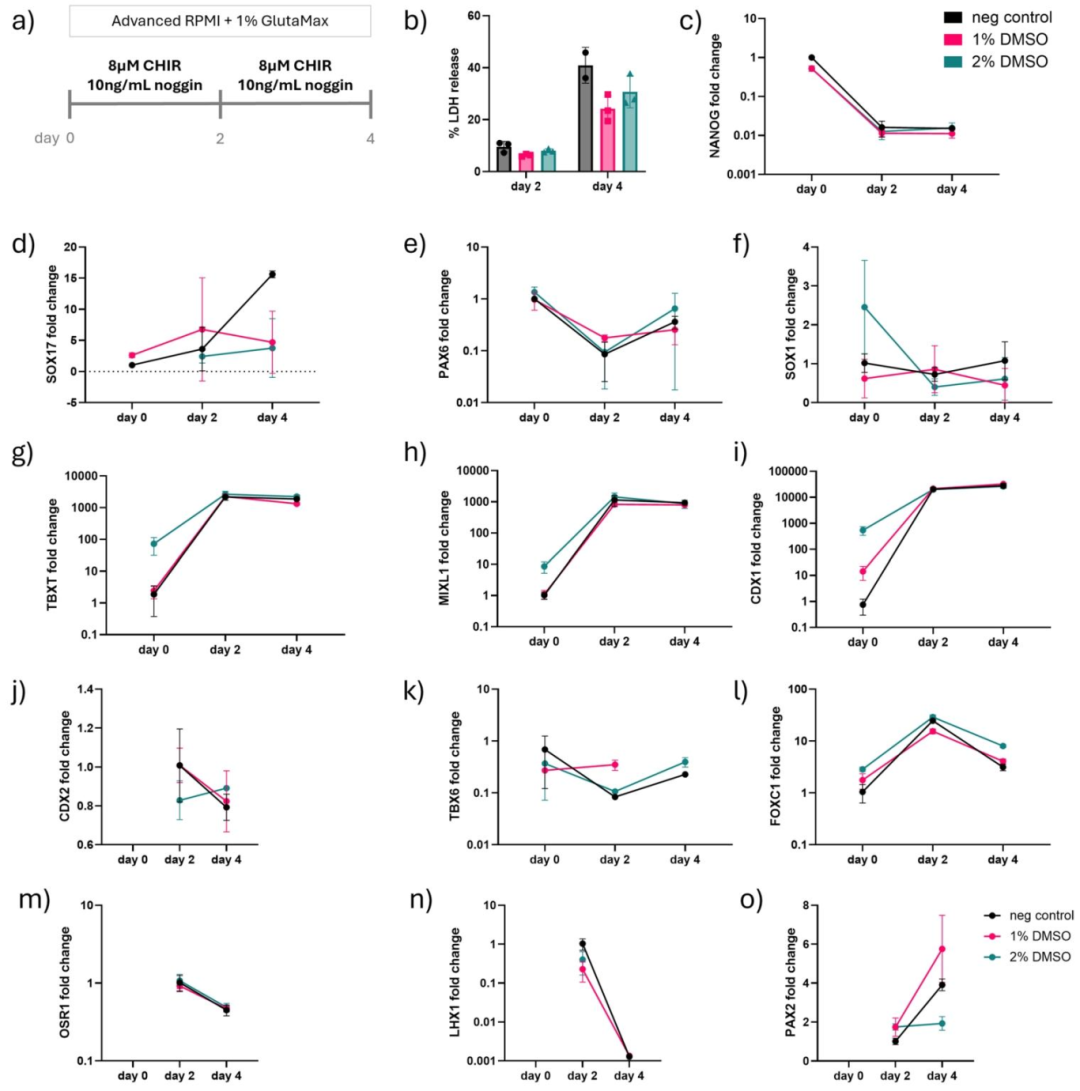
图4:DMSO 对 hiPSCs 向中胚层分化的定向调控
该图验证 DMSO 对分化早期阶段的影响:A 为中胚层诱导流程,DMSO 处理后用 CHIR+Noggin 诱导;B 显示,DMSO 组在分化 Day 2-4 的 LDH 释放减少,提示 DMSO 预处理增强细胞对分化压力的耐受性;C-I 为 qPCR 结果,NANOG 在各组均下调(证实退出多能性),SOX17(内胚层)仅在对照上调(DMSO 抑制内胚层偏移),TBXT/MIXL1(原条标志物)在各组均上调(成功诱导中胚层);J-O 显示,PAX2(中间中胚层)在 1% DMSO 组 Day 4 显著上调,OSR1/LHX1(中间中胚层)表达稳定,证实 DMSO 可定向促进中间中胚层分化(肾脏发育的关键前体),同时抑制内胚层等 off-target lineage。
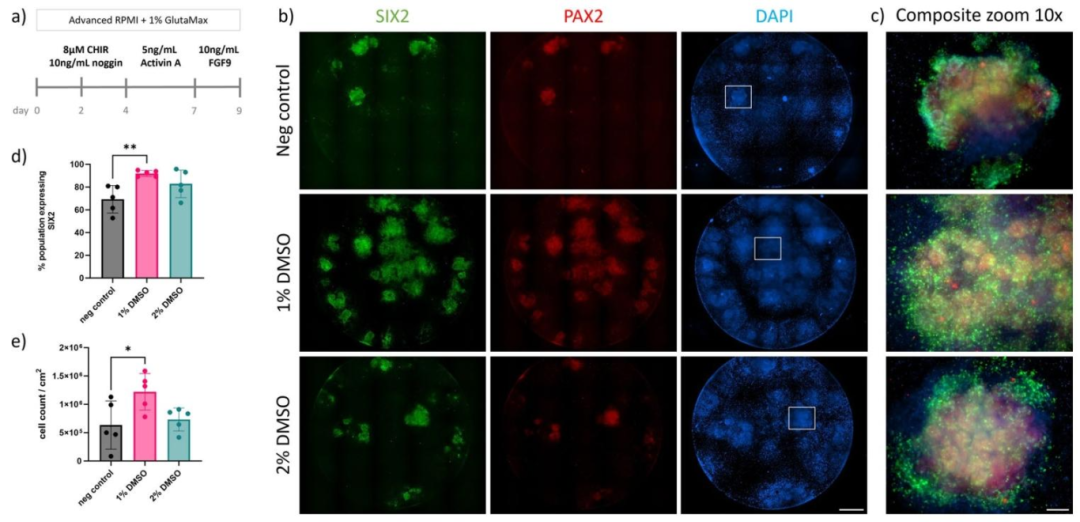
图5:DMSO 促进 hiPSCs 向 SIX2 + 肾祖细胞分化
该图是核心结果,证实 DMSO 对肾祖细胞生成的促进作用:A 为肾祖细胞诱导流程,Day 9 为肾祖细胞成熟时间点;B-C 为免疫荧光,1% DMSO 组 SIX2+(绿色)与 PAX2+(红色)细胞广泛共表达,对照组成熟度低;D-E 为定量,流式检测显示 1% DMSO 组 SIX2 + 细胞比例达 92%,显著高于对照的 69% 和 2% DMSO 的 83%,且细胞密度最高(12×10⁵细胞 /cm²)。SIX2 是后肾间充质肾祖细胞的关键标志物,其比例需达 80-90% 才能高效形成肾脏类器官,该结果直接证实 1% DMSO 是最优浓度,可最大化肾祖细胞产量。
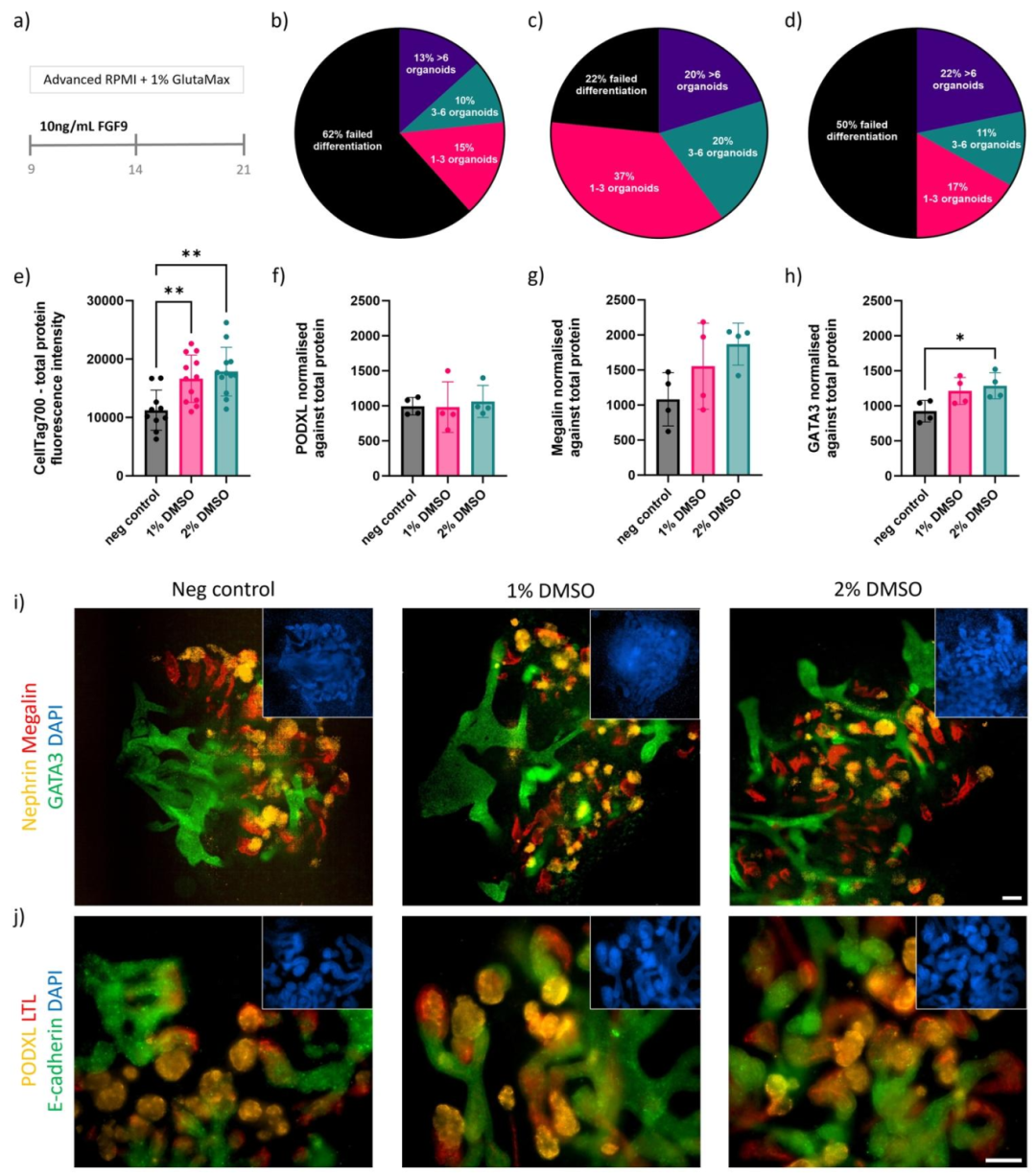
图6:DMSO 提升肾脏类器官分化效率与成熟度
该图评估 DMSO 对类器官终末成熟的影响:A 为类器官成熟流程,Day 9 至 Day 21 为肾单位形成阶段;B-D 为类器官形成率,1% DMSO 组 78% 的孔出现管状结构,显著高于对照的 38% 和 2% DMSO 的 50%;E-H 为 In-cell Western 定量,总蛋白信号与类器官数量正相关,Podocalyxin(肾小球)表达无差异,Megalin(近端小管)轻度上调,GATA3(远端小管 / 集合管)在 2% DMSO 组显著上调;I-J 为免疫荧光,各组类器官均表达肾小球(Podocalyxin/Nephrin)、近端小管(LTL/Megalin)、远端小管(E-cadherin/GATA3)标志物,DMSO 组管状结构更密集。结果证实,DMSO 不仅提高类器官形成率,还促进远端小管 / 集合管成熟,且效果在 1% DMSO 时最优。
本研究证实低剂量 DMSO(1%)短期(24 小时)处理是提升 hiPSCs 向肾脏类器官分化效率的简单策略,核心机制与应用价值体现在三方面:1)细胞周期与表观调控:DMSO 通过上调 CDKN1B 诱导 G1 期停滞,下调 DNMT3A/B 重塑表观景观,使 hiPSCs 从 “自我更新态” 转向 “分化准备态”,且保留多能性核心(SOX2/OCT4 稳定);2)分化定向性优化:抑制内胚层偏移(SOX17 下调)、促进中间中胚层(PAX2 上调),最终使 SIX2 + 肾祖细胞比例达 92%(对照 69%),解决肾祖细胞不足的关键瓶颈;3)类器官效率与成熟度提升:1% DMSO 组类器官形成率达 78%(对照 38%),且远端小管 / 集合管标志物 GATA3 表达增加,类器官功能分区更完整。研究局限性包括:DMSO 的长期表观遗传影响需进一步验证,类器官缺乏血管结构(需后续共培养优化)。总体而言,DMSO 处理作为低成本、易操作的优化步骤,可广泛应用于肾脏类器官构建,为肾病模型、药物筛选提供高效工具。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:卵巢癌类器官模型精准反映铂类敏感性:PDO 与 PDXO 的一致性与临床价值
下一篇:塞内卡病毒 A(SVA)在顶向外猪肠道类器官中的复制与宿主反应