常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-04-24 09:00:00 细胞资源库平台 访问量:32
近年来,单细胞 RNA 测序(scRNA-seq)已成为解析细胞异质性、挖掘稀有细胞群体的核心工具。目前主流技术中,10X Genomics 凭借微流控技术实现高通量分析,但存在小规模细胞群体检测成本高、无法直接关联细胞表型与转录组数据的局限;而 Smart-seq3xpress(SS3X)虽为平板技术,支持全长转录组测序和索引分选,却存在链入侵伪影、操作繁琐等问题。
来自比利时根特大学药物生物技术实验室和诊断科学系的研究团队,在《BMC Genomics》上发表题为Plate-based 10X Genomics-compatible single-cell RNA-sequencing based on Smart-seq3xpress的文章,开发了一种基于平板的 10X 兼容单细胞 RNA 测序技术(PB10X),实现了小规模细胞群体的低成本、高效基因表达分析和免疫受体库测序。
1.细胞分选与裂解:通过荧光激活细胞分选(FACS)将目标单细胞(如 Jurkat T 淋巴母细胞)分选至 384 孔板,每孔预装有含定制 10X 兼容模板切换寡核苷酸(TSO)的裂解液,TSO 带有生物素封闭的 5’端、细胞特异性条形码和 UMI 序列,避免链入侵和串联体形成。
2.逆转录与条形码标记:对分选后的细胞进行变性处理,加入逆转录混合液,通过模板切换机制合成 cDNA,同时将 TSO 上的条形码和 UMI 整合至 cDNA 中,实现单个细胞的唯一标记。
3.cDNA 合并与预扩增:按 24 个不同条形码分组合并 cDNA,经 AMPure XP 磁珠纯化去除短片段杂质后,进行 PCR 预扩增,获得足量高质量 cDNA。
4.10X 文库构建:将 PB10X 生成的 cDNA 与商业化 10X Single Cell 5’文库构建试剂盒(包括基因表达文库和 V (D) J 富集文库)兼容,进行片段化、扩增和索引标记,构建标准化测序文库。
5.测序与数据分析:采用 AVITI 测序仪进行测序,基因表达分析目标为每细胞 50,000 条 reads,V (D) J 测序为每细胞 5,000 条 reads;通过 Cell Ranger(10X 兼容分析)、TRUST4(TCR 重建)等工具处理数据,与 10X Genomics 和 SS3X 技术进行基准对比。
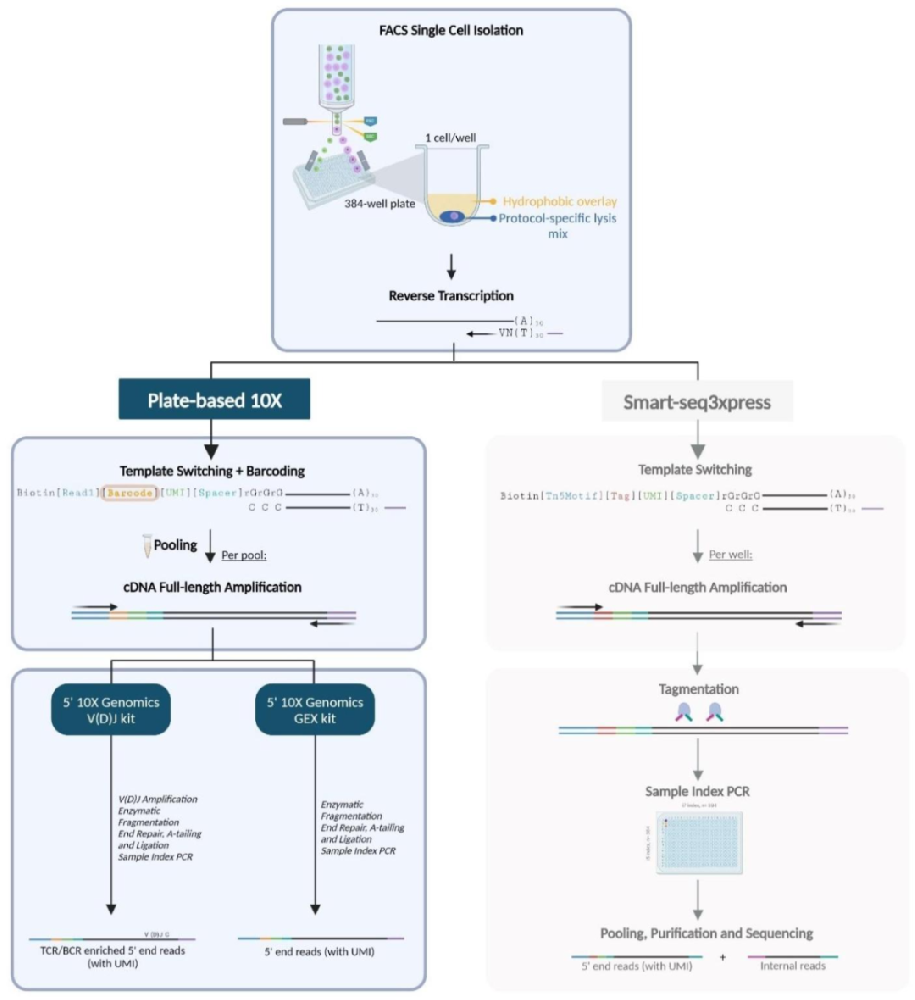
图1:PB10X 与 SS3X 的实验流程对比
左图为 PB10X 流程:FACS 分选后的单细胞经逆转录和条形码标记后,早期合并 cDNA 并通过 10X 试剂盒构建文库,最终获得含 UMI 的 5’端 reads(支持基因表达和 TCR/BCR 分析);右图为 SS3X 流程:单细胞逆转录后需单独进行 PCR 扩增和片段化,最终获得 5’端 UMI 标记片段和全长转录组内部片段。核心差异在于 PB10X 通过定制 TSO 实现早期样本合并,简化操作并兼容 10X 文库,而 SS3X 需单独处理每个样本,且无 10X 兼容性。
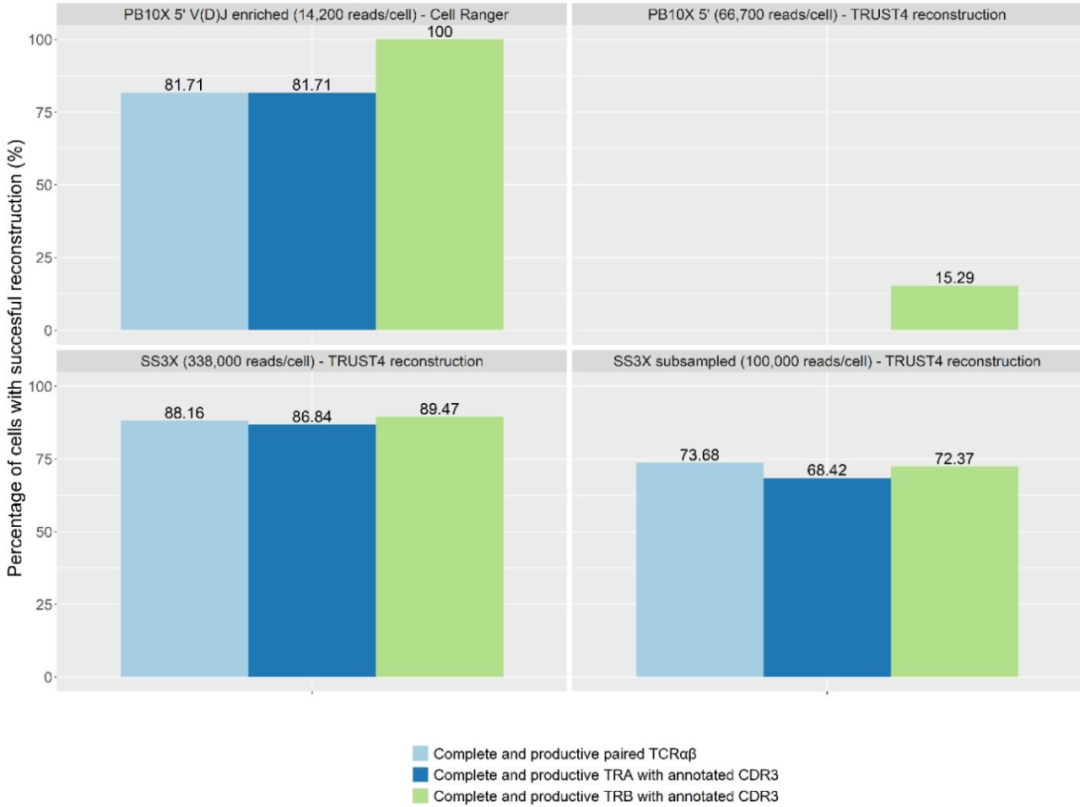
图2:不同策略的 TCR 重建效率对比
PB10X 结合 10X V (D) J 富集文库(每细胞~14,200 条 reads)时,81.71% 的细胞可成功重建完整且有功能的 TCRαβ 配对链;SS3X 在全测序深度(每细胞 338,000 条 reads)下 TCR 配对重建率为 86.84%,但当测序深度降至 PB10X 水平时,重建率骤降至 1.32%;PB10X 仅使用基因表达文库时,15.3% 的细胞可重建 TCRβ 链,但无法检测 TCRα 链。结果表明,PB10X 在低测序深度下即可实现高效 TCR 重建,远优于同等深度的 SS3X。
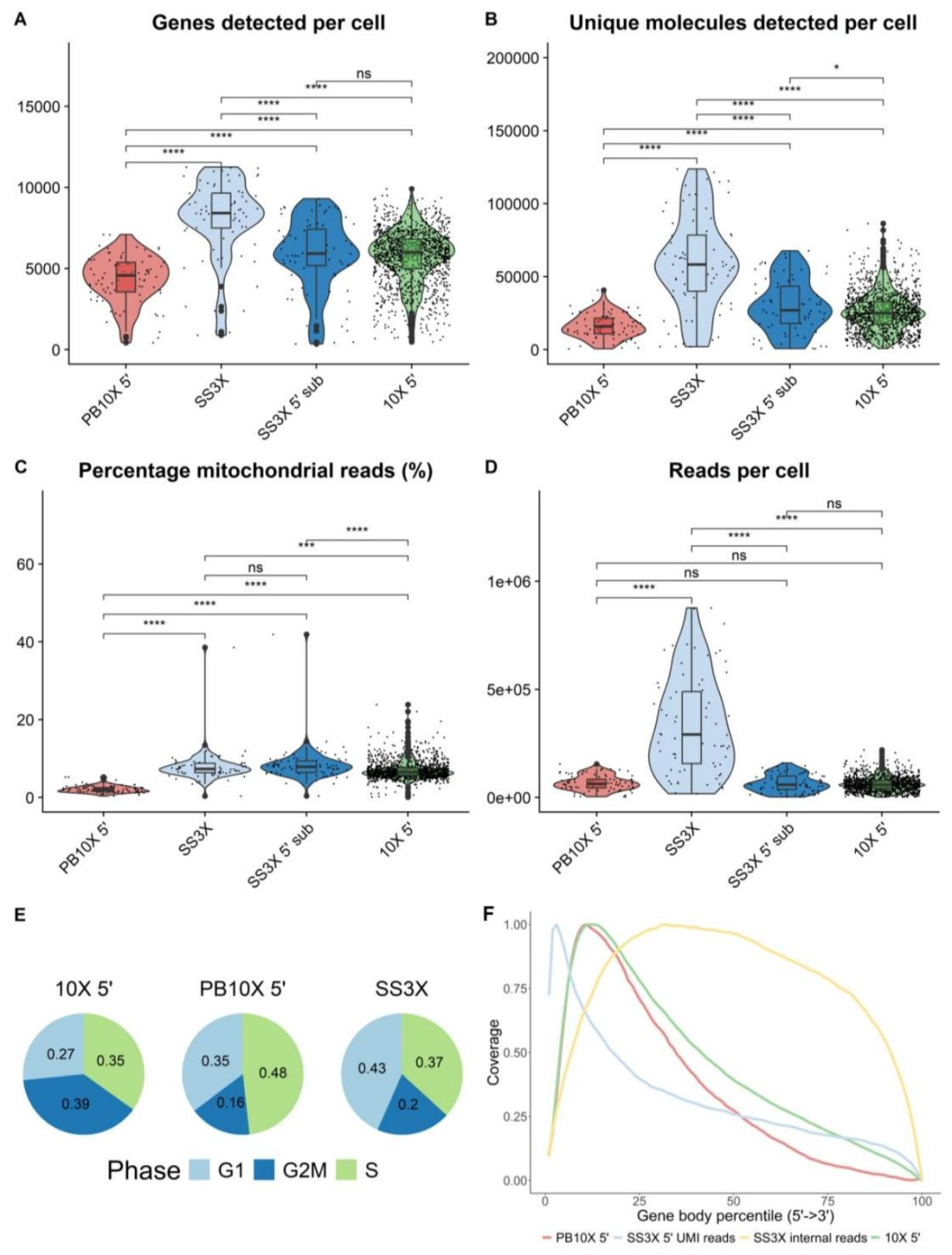
图3:基因检测、UMI 数量及细胞周期等基准指标对比
PB10X 每细胞平均检测 4,343 个基因和 16,137 个 UMI,虽低于 SS3X 但显著高于 10X Genomics;PB10X 的线粒体基因占比最低,说明样本质量更优;细胞周期分布显示 PB10X 与其他两种技术无显著系统性差异;基因体覆盖度上,PB10X 和 10X 均偏向 5’端,而 SS3X 因包含内部片段,覆盖更均匀。此外,SS3X 经 5’端 reads 提取和测序深度标准化后,与 PB10X 的基因检测数量无统计学差异。
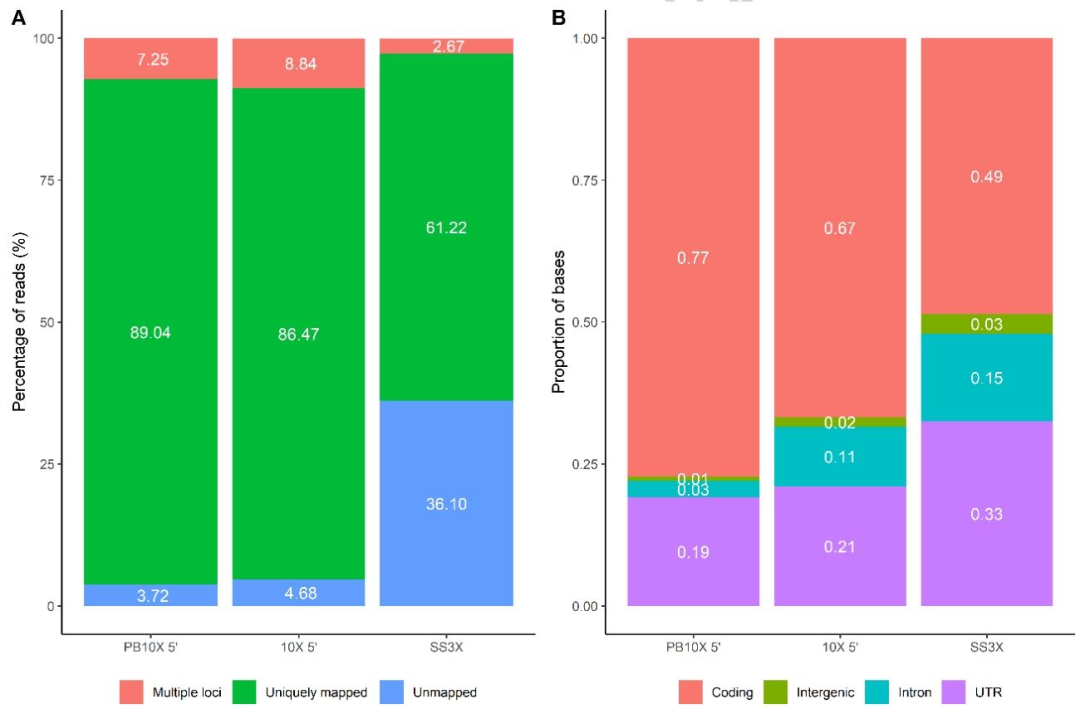
图4:测序 reads 映射效率与基因组区域分布
PB10X 的唯一映射 reads 比例最高(89.04%),未映射 reads 比例最低(2.67%);SS3X 因存在大量短片段内部 reads,未映射比例达 36.10%。在基因组区域分布上,PB10X 映射到编码区的 reads 比例最高(61.22%),而 SS3X 的基因间区 reads 比例更高,提示其链入侵伪影更明显。这表明 PB10X 的测序数据质量更优,有效信息占比更高。
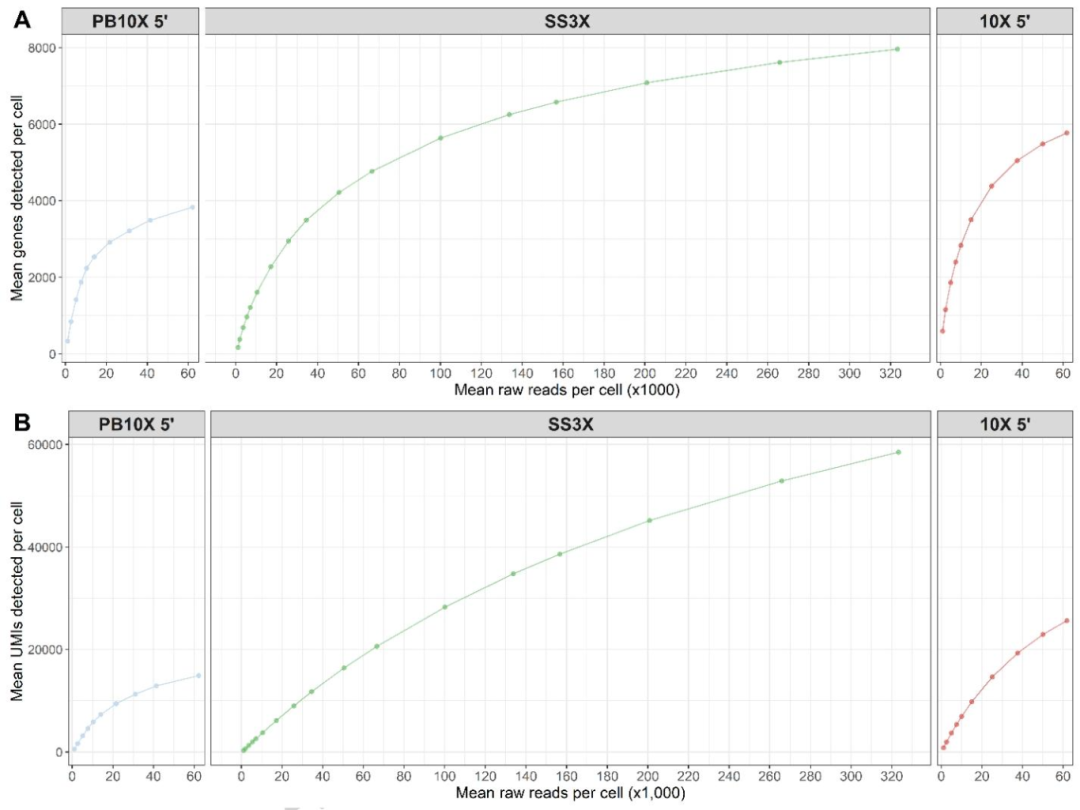
图5:测序饱和度分析
PB10X 最早达到测序饱和(饱和度 0.75),其次是 10X Genomics(0.80),SS3X 因包含非 UMI 标记的内部 reads,饱和曲线最平缓(饱和度 0.58)。这意味着 PB10X 仅需较低测序深度即可捕获足够的基因和 UMI 信息,显著降低测序成本,而 SS3X 需更高测序深度才能达到同等检测效果。
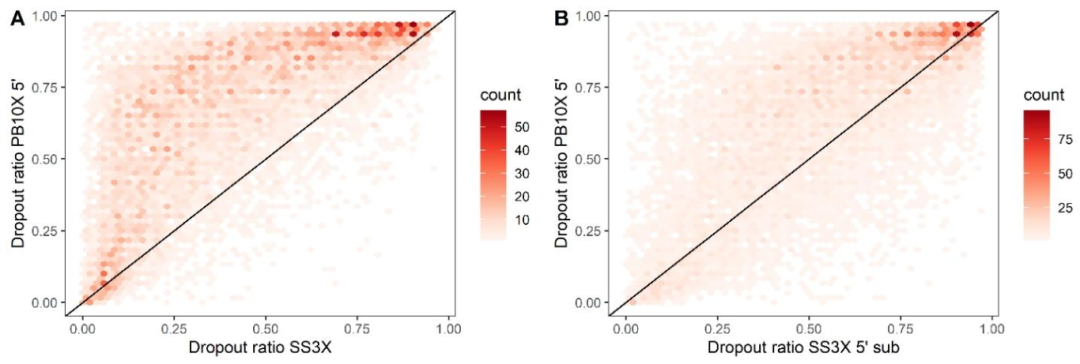
图6:基因 dropout 比例对比
PB10X 的基因 dropout 比例(即特定基因在细胞中未被检测到的比例)高于完整 SS3X,但当 SS3X 仅保留 5’端 reads 并标准化测序深度后,PB10X 与 SS3X 的 dropout 比例无显著差异。这表明 PB10X 的 dropout 主要与测序策略(偏向 5’端)相关,而非技术本身的捕获效率问题,与 10X Genomics 的表现一致。
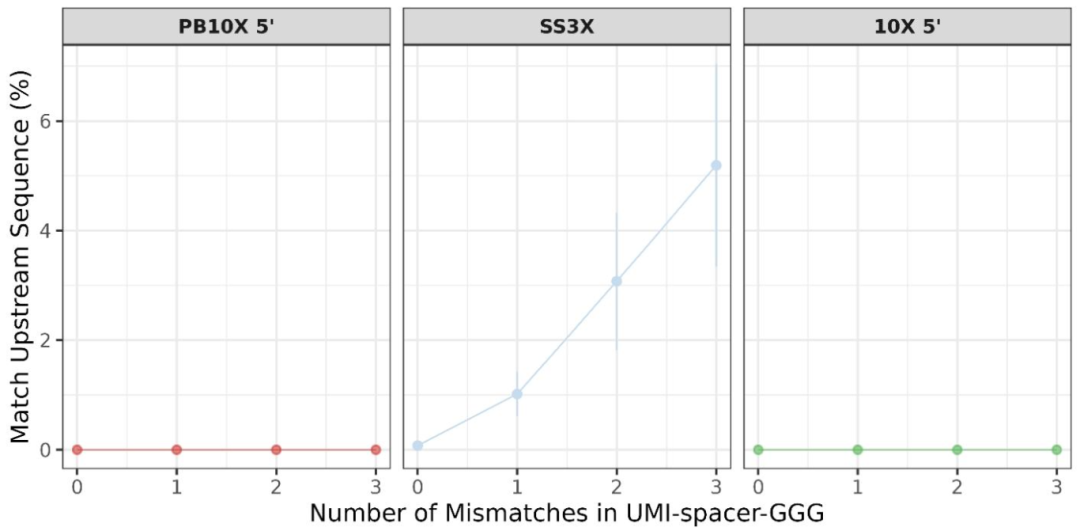
图7:链入侵伪影检测
SS3X 存在明显的链入侵现象(即 TSO 提前与 cDNA 互补区域结合导致逆转录终止),而 PB10X 和 10X Genomics 均有效消除了该伪影。原因在于 PB10X 采用了更优的 TSO 间隔序列(TTTCTTATAT),且早期样本合并后的磁珠纯化步骤去除了过量 TSO,而 SS3X 因无法早期合并,无法进行该纯化步骤。
PB10X 技术创新性地整合了平板测序的灵活性和 10X Genomics 的标准化优势,通过定制生物素封闭 TSO 解决了链入侵和串联体问题,早期样本合并简化了操作流程并降低成本,低测序深度下即可实现高效的基因表达分析和 TCR/BCR 重建。该技术尤其适用于小规模细胞群体(如肿瘤浸润淋巴细胞、少量活检样本),在免疫治疗、罕见病研究等场景中具有广阔应用前景,为科研人员提供了一种低成本、高兼容性、高质量的单细胞测序新工具。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:INHBB 高表达塑造免疫抑制性肿瘤微环境并预测结直肠癌不良预后
下一篇:超高灵敏!NanoLuc斑马鱼平台赋能肾毒性与药物高通量筛选!