常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-26 17:02:06 细胞资源库平台 访问量:81
荧光素酶报告基因系统是一种基于荧光素酶催化底物氧化反应产生生物发光的检测技术,广泛应用于细胞生物学研究。其中,萤火虫荧光素酶(firefly luciferase, Fluc)因其高灵敏度、宽线性检测范围(约7~8个数量级)以及较短的半衰期(在哺乳动物细胞中约为3小时,在植物细胞中约为3.5小时)而成为最常用的报告基因。其发光信号强度在酶浓度为10⁻¹⁶ mol/L至10⁻⁸ mol/L的范围内与酶活性呈线性关系,并且在理想条件下可检测到低至10⁻²⁰ mol/L的荧光素酶活性。此外,荧光素酶报告基因系统具有非放射性、检测快速、灵敏度高(比氯霉素乙酰转移酶CAT高100倍)等优点,特别适用于高通量筛选和活细胞检测。通过将荧光素酶报告基因载体转染至宿主细胞后,可利用荧光素酶检测系统灵敏且便捷地监测基因表达水平,已成为细胞生物学研究中的重要工具。
英文标题:A Spatially Ordered Three-Input Logic Gate for Highly Specific and Sensitive Breast Tumor Imaging
中文标题:用于高特异性和高灵敏度乳腺癌成像的空间有序三输入逻辑门
发表期刊:《Analytical Chemistry》
影响因子:6.7
作者单位:
1.State Key Laboratory of Digital Medical Engineering, School of Biological Science and Medical Engineering, Southeast University, Nanjing 211189, China
2.Key Laboratory of Optic-Electric Sensing and Analytical Chemistry for Life Science, MOE, Shandong Key Laboratory of Biochemical Analysis, Key Laboratory of Analytical Chemistry for Life Science in Universities of Shandong, College of Chemistry and Molecular Engineering, Qingdao University of Science and Technology, Qingdao 266042, China
3.State Key Laboratory of Coordination Chemistry, School of Chemistry and Chemical Engineering, Nanjing University, Nanjing 210093, China
作者信息:
Hongzhe Yan,Xiaoyang Liu,Caifeng Ding and Gaolin Liang(通讯作者)
乳腺癌是全球女性健康的重大威胁,具有高侵袭性和转移性,精准且灵敏的诊断对改善患者预后至关重要。临床常用的有创穿刺活检可能导致肿瘤转移,而无创诊断方法存在诸多局限:血液和尿液检测特异性差,无法单独作为诊断工具;PET 成像组织分辨率低、辐射高且特异性不足,CT 和 MRI 缺乏功能信息;荧光成像存在非特异性背景信号,而生物发光(BL)成像无需外部激发光,信噪比和灵敏度更优,是极具潜力的乳腺癌检测技术,但仍需提升特异性以实现精准体内检测。逻辑门可整合多个输入信号增强检测准确性,单输入和双输入逻辑门易出现非特异性激活和信号串扰,无序三输入逻辑门存在假阳性问题,而空间有序三输入逻辑门具有更复杂的信号处理能力和抗干扰性。乳腺癌细胞中尿激酶型纤溶酶原激活剂(uPA,膜定位)、组织蛋白酶B(CTB,溶酶体定位)和荧光素酶(fLuc,细胞质定位)具有明确的空间分布关系,且均与肿瘤特性相关,以此为输入构建空间有序三输入逻辑门,可实现高特异性和高灵敏度的乳腺癌生物发光成像,而此类逻辑门在乳腺癌精准诊断中的应用尚未见报道。
本研究设计合成了空间有序三输入逻辑门探针 KK (GGR)-Luc,其包含 uPA 响应的 GGR 片段、CTB 切割底物 Cbz-KK 以及生物发光成像部分 D - 氨基荧光素(D-AmLuc),通过电喷雾电离质谱(ESI-MS)和基质辅助激光解吸电离飞行时间质谱(MALDI-TOF-MS)验证合成成功;以 fLuc 转染的小鼠三阴性乳腺癌 4T1 细胞为细胞模型,设置不同抑制剂处理组(uPA 抑制剂 4-CPG、CTB 抑制剂 CA-074-Me 及双抑制剂),采用流式细胞术探究探针的细胞内吞途径,通过激光共聚焦显微镜观察探针与溶酶体的共定位及溶酶体逃逸情况,利用生物发光成像系统检测不同时间点的细胞发光信号,计算发光半衰期;构建 fLuc 转染 4T1 细胞的裸鼠皮下移植瘤模型,将小鼠随机分为四组(仅探针组、探针 + uPA 抑制剂组、探针 + CTB 抑制剂组、探针 + 双抑制剂组),经尾静脉注射探针后,通过小动物成像系统实时监测体内肿瘤区域的生物发光信号,90 分钟后处死小鼠,分离肿瘤组织和主要器官进行离体生物发光成像;通过 MTT 法检测探针的细胞毒性,借助血液学分析和苏木精 - 伊红(H&E)染色评估探针的体内生物安全性;采用高效液相色谱(HPLC)验证探针对 uPA 和 CTB 的串联响应特性,通过生物发光光谱分析探针在细胞裂解液中的特异性激活效果,所有实验数据均进行统计学分析,p<0.05 为差异显著。
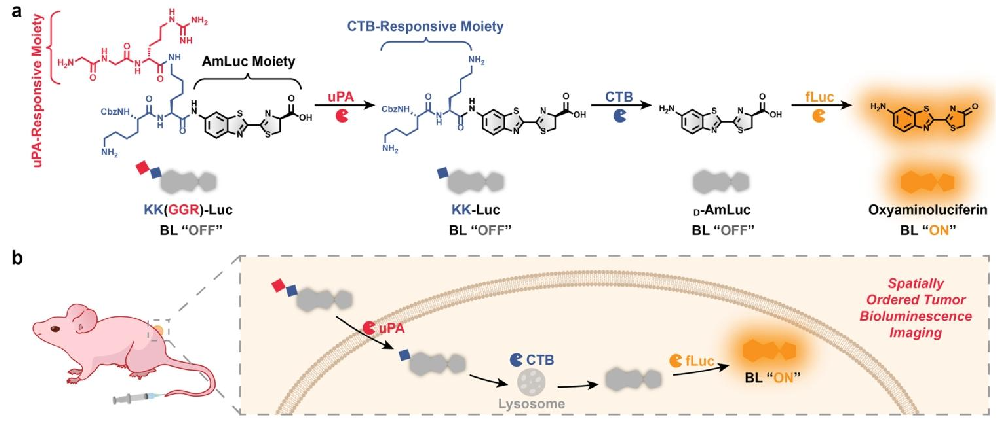
图1:KK (GGR)-Luc 的激活机制及体内成像示意图
图 1a 展示了 KK (GGR)-Luc 作为有序三输入逻辑门对 uPA、CTB 和 fLuc 的串联响应机制:乳腺癌细胞膜上的 uPA 首先特异性切割 GGR 片段,避免 CTB 提前识别 Cbz-KK,随后探针进入溶酶体,溶酶体内的 CTB 切割 Cbz-KK,暴露 D-AmLuc,在细胞质中 fLuc 的作用下启动生物发光信号(BL “ON”),缺少任一输入则无发光信号;图 1b 为体内成像示意图,直观呈现了探针在体内依次响应三种输入、实现肿瘤特异性发光成像的过程,明确了探针的空间有序激活逻辑。
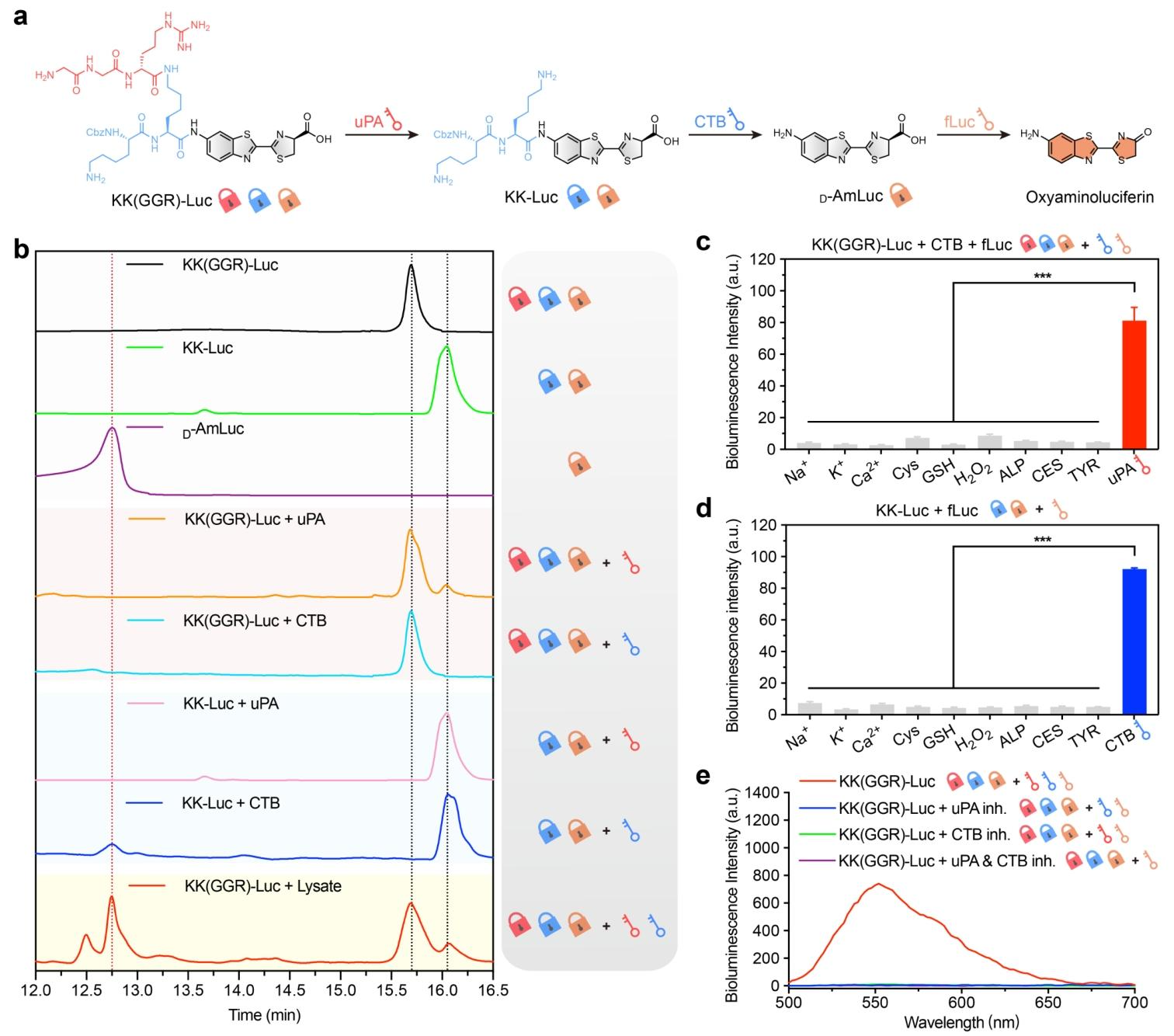
图2:KK (GGR)-Luc 的串联响应特性、选择性及生物发光光谱分析
图 2a 为探针与 uPA、CTB、fLuc 的识别关系图,明确三者的有序作用顺序;图 2b 的 HPLC 结果显示,KK (GGR)-Luc 仅在 uPA 作用下生成 KK-Luc(产率 13%),KK-Luc 仅在 CTB 作用下生成 D-AmLuc(产率 15%),“KK (GGR)-Luc+CTB” 和 “KK-Luc+uPA” 组无新产物生成,4T1 细胞裂解液处理后 45% 的探针转化为 D-AmLuc,证实了前两种输入的逻辑正交性和串联响应关系;图 2c 和 d 的选择性实验表明,KK (GGR)-Luc 仅在 uPA 存在时显著激活生物发光(较其他物质高 9.3 倍),KK-Luc 仅在 CTB 存在时产生强发光信号(较其他物质高 12.5 倍),体现了探针各阶段的高选择性;图 2e 的生物发光光谱显示,fLuc 转染的 4T1 细胞裂解液处理后,探针在 560nm 处的发光强度增强 690 倍,而加入 uPA 抑制剂、CTB 抑制剂或双抑制剂后,发光信号显著抑制,fLuc 阴性的正常 4T1 细胞裂解液无明显发光,证实 fLuc 是激活探针发光的必需输入,三者共同作用才能实现探针的高效激活。
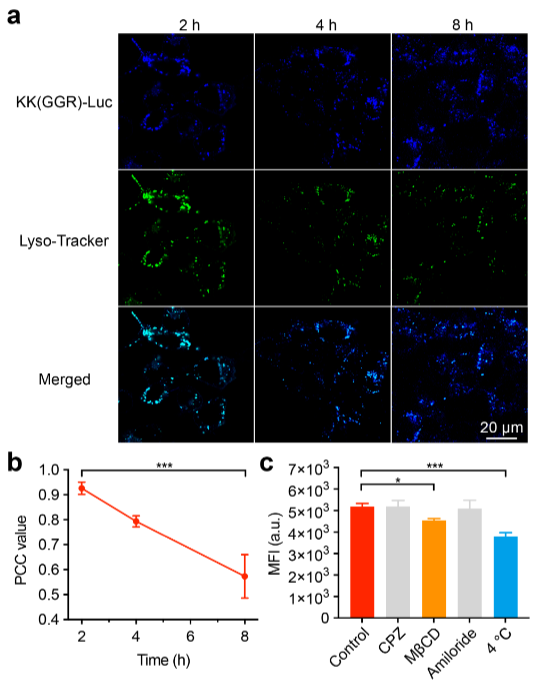
图3:KK (GGR)-Luc 在 4T1 细胞中的定位、溶酶体逃逸及内吞途径分析
图 3a 的激光共聚焦成像结果显示,探针与溶酶体在 2h 时共定位程度高(皮尔逊相关系数 PCC=0.93),4h 和 8h 时 PCC 值分别降至 0.79 和 0.57,表明探针随时间推移成功实现溶酶体逃逸,可能与探针的正电荷诱导质子海绵效应相关;图 3b 为不同时间点的 PCC 值统计,量化了探针与溶酶体的共定位变化趋势;图 3c 的流式细胞术结果显示,网格蛋白介导的内吞抑制剂氯丙嗪(CPZ)对探针内吞影响较小,而小窝蛋白介导的内吞抑制剂甲基 -β- 环糊精(MβCD)和 4℃低温处理(抑制能量依赖型内吞)显著降低了探针的细胞内吞水平,表明探针主要通过小窝蛋白介导和能量依赖型内吞途径进入细胞。
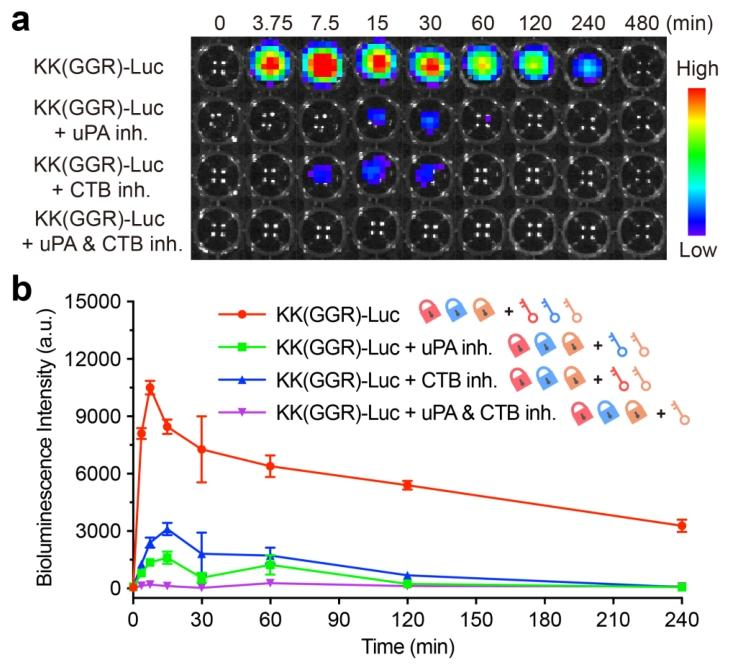
图4:fLuc 转染 4T1 细胞的生物发光成像及信号强度分析
图 4a 为不同处理组细胞在不同时间点的生物发光成像图,直观显示仅探针组的发光信号显著强于各抑制剂处理组,且信号在 7.5 分钟时达到峰值;图 4b 的信号强度定量分析表明,仅探针组的生物发光强度较其他组高 4.4 倍以上,uPA 抑制剂组和 CTB 抑制剂组的发光信号显著抑制,双抑制剂组几乎无发光信号;此外,仅探针组的生物发光信号可维持至 240 分钟,发光半衰期长达 117.2 分钟,分别是 uPA 抑制剂组和 CTB 抑制剂组的 2.6 倍和 1.9 倍,证实该逻辑门探针具有持续的信号激活能力,在细胞水平展现出优异的乳腺癌成像潜力。
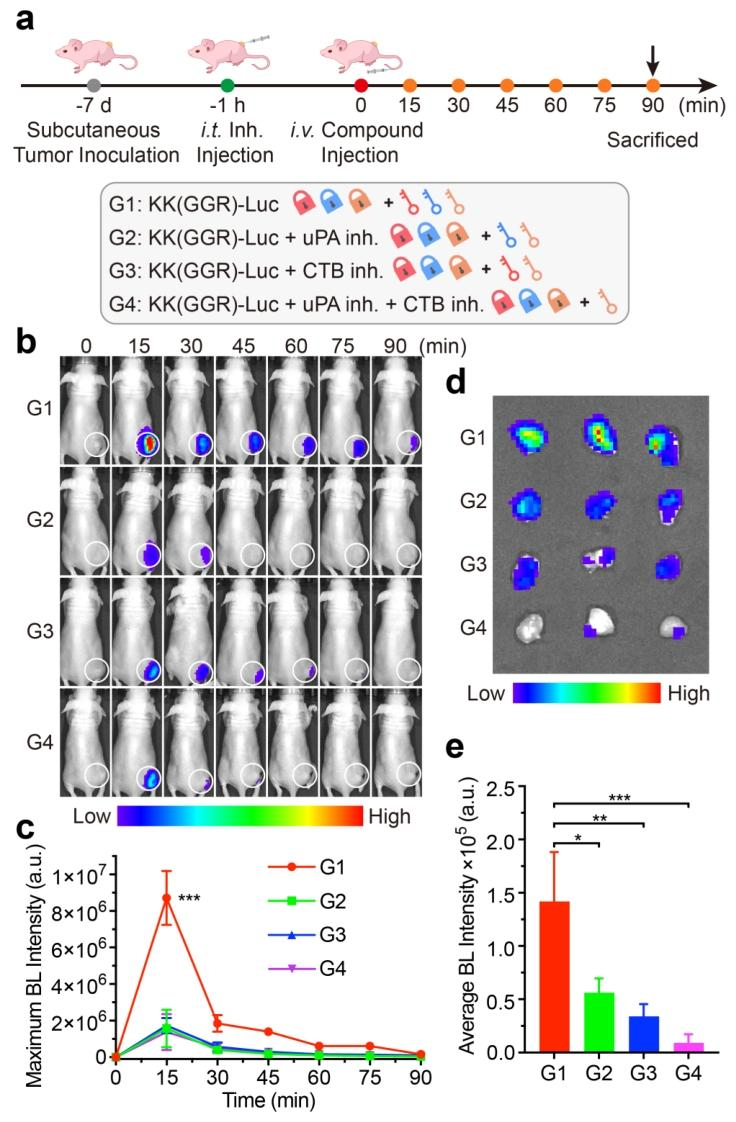
图5:裸鼠体内及肿瘤离体生物发光成像分析
图 5a 为体内实验流程:裸鼠肿瘤接种 7 天后,肿瘤内预注射抑制剂 1 小时,再尾静脉注射探针,随后不同时间点进行体内成像,90 分钟后处死小鼠进行离体成像;图 5b 为不同处理组裸鼠在各时间点的体内生物发光成像图,白色圆圈标记肿瘤区域,仅探针组的肿瘤区域发光信号明显强于抑制剂处理组;图 5c 的定量结果显示,仅探针组在 15 分钟时发光强度达到峰值,其强度分别是探针 + uPA 抑制剂组、探针 + CTB 抑制剂组、探针 + 双抑制剂组的 5.6 倍、5.0 倍和 6.3 倍,发光半衰期为 11.4 分钟;图 5d 和 e 的离体成像及定量分析表明,仅探针组的肿瘤组织发光强度分别是其他三组的 2.5 倍、4.2 倍和 15.5 倍,差异具有统计学意义,且探针在主要器官中几乎无明显发光信号,证实探针具有良好的肿瘤靶向性,体内成像特异性高。
本研究成功设计合成了空间有序三输入逻辑门探针 KK (GGR)-Luc,该探针以乳腺癌细胞中 uPA、CTB 和 fLuc 为输入,通过串联响应实现特异性生物发光激活。HPLC 验证了探针对 uPA 和 CTB 的逻辑正交性和串联响应特性,4T1 细胞裂解液可使 45% 的探针转化为 D-AmLuc;体外实验表明,探针仅在 uPA、CTB 和 fLuc 共同存在时产生强生物发光信号,选择性高达 9.3-12.5 倍,细胞水平成像中探针发光强度较对照组高 3.5 倍以上,发光半衰期长达 117.2 分钟,且探针主要通过小窝蛋白介导和能量依赖型内吞进入细胞,能成功实现溶酶体逃逸;体内实验显示,探针处理组的肿瘤区域发光强度较各抑制剂处理组高 5.0 倍以上,离体肿瘤发光强度高 2.5 倍以上,且探针在正常器官中分布少、发光信号弱;MTT 法、血液学分析和 H&E 染色证实探针具有良好的细胞毒性和体内生物安全性。该空间有序三输入逻辑门通过整合肿瘤特异性酶和报告基因的有序响应,显著提升了乳腺癌成像的特异性和灵敏度,为乳腺癌的精准无创诊断提供了新工具,也为构建更先进的有序逻辑门用于肿瘤病理检测奠定了基础。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:依赖 HBV 的 “致命病毒”丨HDV 感染的诊疗挑战与突破
下一篇:NanoLuc-GFP 双报告系统解锁基因表达定量新方式