常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-25 09:00:00 细胞资源库平台 访问量:94
丁型肝炎病毒(HDV)需与乙肝病毒(HBV)共感染,是最严重的病毒性肝炎,30%-70% 患者 5-10 年内进展为肝硬化,但现有治疗存在局限:PEG - 干扰素疗效低、患者依从性差,新型进入抑制剂(如 Bulevirtide)无法清除肝细胞内病毒。核心问题在于HDV 特异性 CD8⁺T 细胞反应不足,导致感染持续;同时,传统研究模型存在缺陷 —— 原代肝细胞培养功能易丢失、HepG2-NTCP 细胞与原代肝细胞差异大、动物模型(如小鼠)天然抵抗 HDV,肝类器官模型多依赖非 FDA 合规的 Matrigel,限制临床转化。本研究通过建立 FDA 合规的 HBV/HDV 共感染肝类器官,探究泛素化小 HDV 抗原(Ub-S-HDAg)如何通过调控树突状细胞(DC)和 CD8⁺T 细胞免疫反应抑制 HDV 复制,填补 “HDV 免疫治疗靶点” 与 “生理相关模型” 的双重空白。
来自中国上海交通大学医学院附属第六人民医院、英国帝国理工学院的团队在《Antiviral Research》发表题为Ubiquitinated hepatitis D antigen-induced CD8⁺T-cell responses inhibit HDV replication in HDV-infected liver organoids的研究。
(1)研究方法
1.HBV/HDV 共感染肝类器官构建
细胞分化:人诱导多能干细胞(iPSCs)分步分化为肝细胞样细胞(HLC)—— 经定型内胚层(DE)→肝内胚层(HE)→肝母细胞→HLC(21 天),通过 qPCR(ALB、AFP、NTCP)和免疫荧光(HNF-4α、NTCP)验证肝特性;
支架培养:HLC 接种于倒置胶体晶体(ICC)支架(PEG 材料,FDA 合规),8 天形成成熟肝类器官;
病毒感染:HLC-ICC 先感染 HBV(MOI=100 vge/cell,4% PEG+2% DMSO),48 小时后超感染 HDV,qPCR 检测病毒载量,免疫荧光 / WB 验证 HBsAg、HDAg 表达。
2.Ub-S-HDAg 慢病毒构建与免疫细胞处理
载体构建:将 Ub-S-HDAg、S-HDAg(对照)克隆至慢病毒载体 pGWLV01-new,转染 DC(从健康人 PBMC 分离,GM-CSF+IL-4 诱导),设空白载体(NC)、TNF-α(DC 成熟阳性对照)组;
免疫共培养:DC 与 T 细胞(PBMC 分离,CD3/CD28 激活)共培养 3 天,磁珠分选 CD8⁺T 细胞,流式检测 DC 成熟标志物(CD80/CD83/CD86),ELISA 检测细胞因子(IFN-γ、IL-2、IL-12 等),LDH 法测 CD8⁺T 细胞毒性。
3.机制验证与体内实验
转录组测序:分析 Ub-S-HDAg 组与 NC 组 CD8⁺T 细胞的差异基因,KEGG/GO 富集通路;
通路阻断:用 JAK2 抑制剂 AG490 处理,WB/qPCR 检测 JAK1/JAK2/STAT1/STAT4 及其磷酸化水平;
小鼠模型:AAV-HDV1.2 建立慢性 HDV 感染小鼠,尾静脉注射 Ub-S-HDAg 转染的 DC,检测肝内 HDAg 和血清 HDV RNA。
(2)关键结果
1.肝类器官模型有效模拟 HBV/HDV 共感染:HLC-ICC 高表达 NTCP(HDV 受体),感染后 3 天检测到 HDV RNA,峰值达 10⁶ copies/mL(第 6 天),且能分泌具有感染性的 HBV/HDV 颗粒,可二次感染 Huh7-NTCP 细胞。
2.Ub-S-HDAg 促进 DC 成熟:与 S-HDAg/NC 组相比,Ub-S-HDAg 组 DC 的 CD80(99.33% vs 23.93%)、CD83(25.00% vs 0.55%)、CD86(99.40% vs 0.57%)表达显著升高,形态上出现更多树突状突起。
3.Ub-S-HDAg 通过 JAK/STAT 激活 CD8⁺T 细胞:
转录组显示 Ub-S-HDAg 组 CD8⁺T 细胞中 JAK/STAT 通路显著富集(GSEA 富集 score=1.8);
WB 证实 Ub-S-HDAg 组 JAK1/p-JAK1、JAK2/p-JAK2、STAT1/p-STAT1、STAT4/p-STAT4 表达升高 2-3 倍,AG490 可完全阻断;
CD8⁺T 细胞功能增强:Ub-S-HDAg 组 IFN-γ(+60%)、IL-2(+55%)、IL-12(+45%)分泌增加,对 HDV 感染细胞的毒性率达 55.48%(E/T=1:20),是 S-HDAg 组的 2 倍。
4.Ub-S-HDAg 抑制 HDV 复制:肝类器官中,Ub-S-HDAg 组 HDV RNA 载量较 NC 组降低 60%,HDAg 蛋白减少 50%,AG490 处理后抑制效果消失;小鼠模型中,Ub-S-HDAg 组血清 HDV RNA 降低 40%,肝内 HDAg 阳性细胞减少 35%。
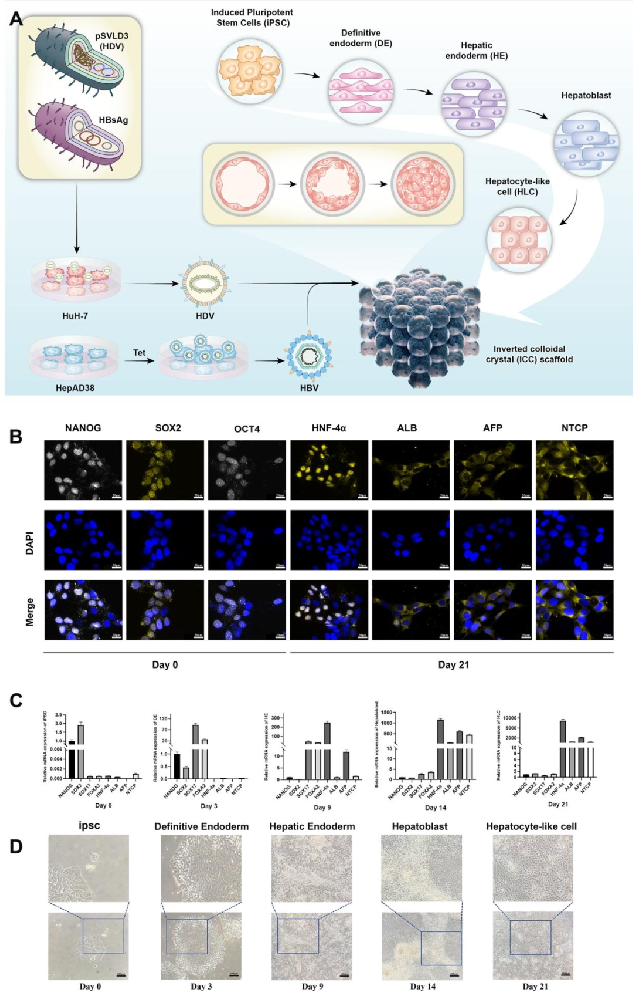
图 1:iPSCs 分步分化为 HLC
该图验证细胞分化有效性:(A)分化流程:iPSC→DE→HE→肝母细胞→HLC→ICC 支架;(B)qPCR:分化过程中多能基因(OCT4/NANOG)下降,肝基因(ALB、AFP、NTCP)升高,第 21 天 HNF-4α 表达达峰值;(C)明场图:细胞从圆形(iPSC)变为多边形(HLC);(D)免疫荧光:iPSC 高表达 NANOG/SOX2/OCT4,HLC 高表达 HNF-4α/ALB/AFP/NTCP。图示 iPSC 可成功分化为功能型 HLC。
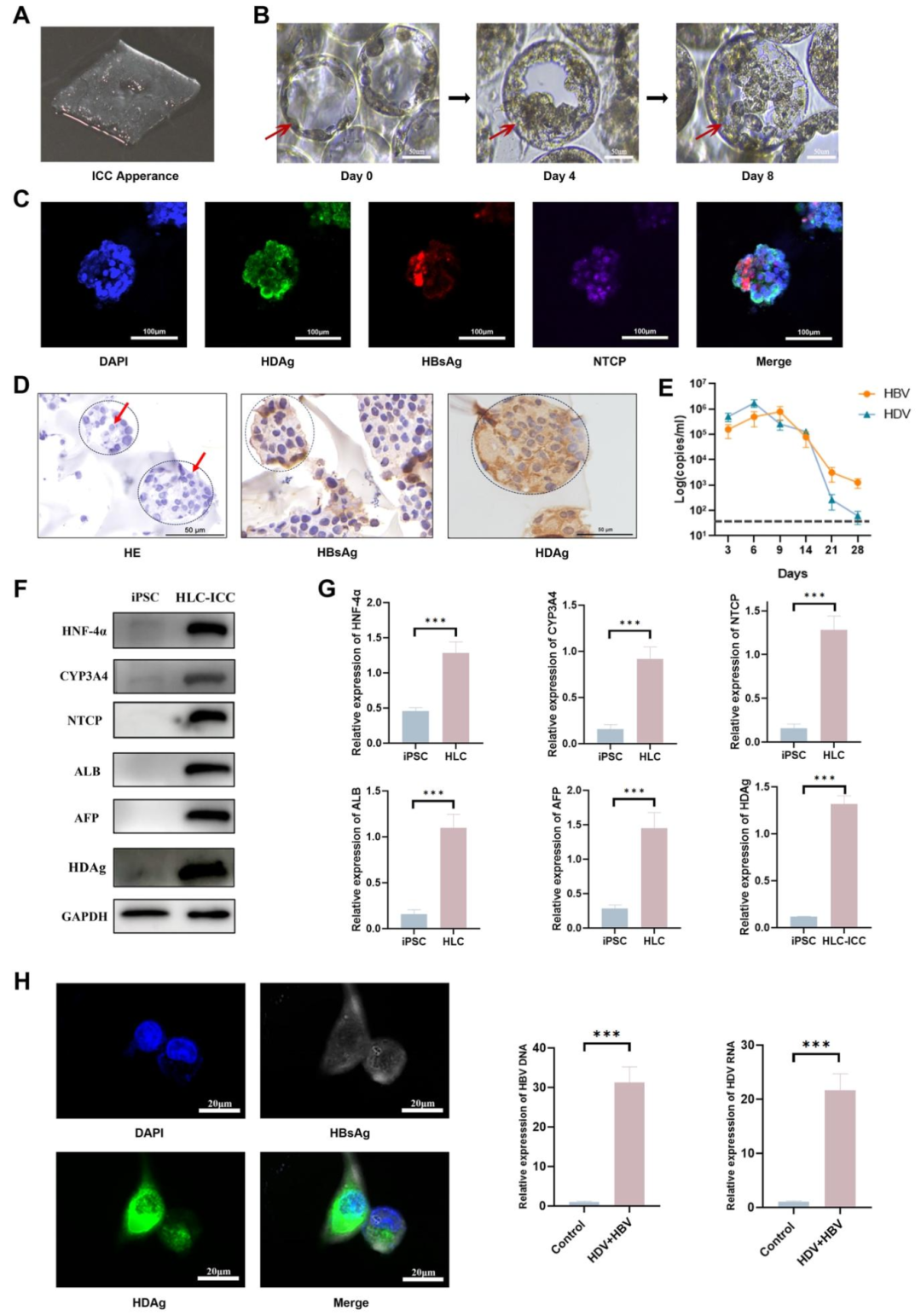
图 2:HBV/HDV 共感染肝类器官构建与验证
该图确认模型可行性:(A-B)ICC 支架外观与类器官生长:HLC 从支架边缘向中心生长,8 天覆盖支架;(C-D)免疫荧光 / HE 染色:类器官中 NTCP、HBsAg、HDAg 共定位,HE 显示典型肝细胞形态;(E)病毒载量:HDV RNA 在第 6 天达 1.73×10⁶ copies/mL,28 天仍可检测;(F-H)WB:类器官表达肝标志物(HNF-4α、CYP3A4)和 HDAg,分泌的病毒可二次感染 Huh7-NTCP 细胞。图示肝类器官可支持 HBV/HDV 共感染与病毒复制。
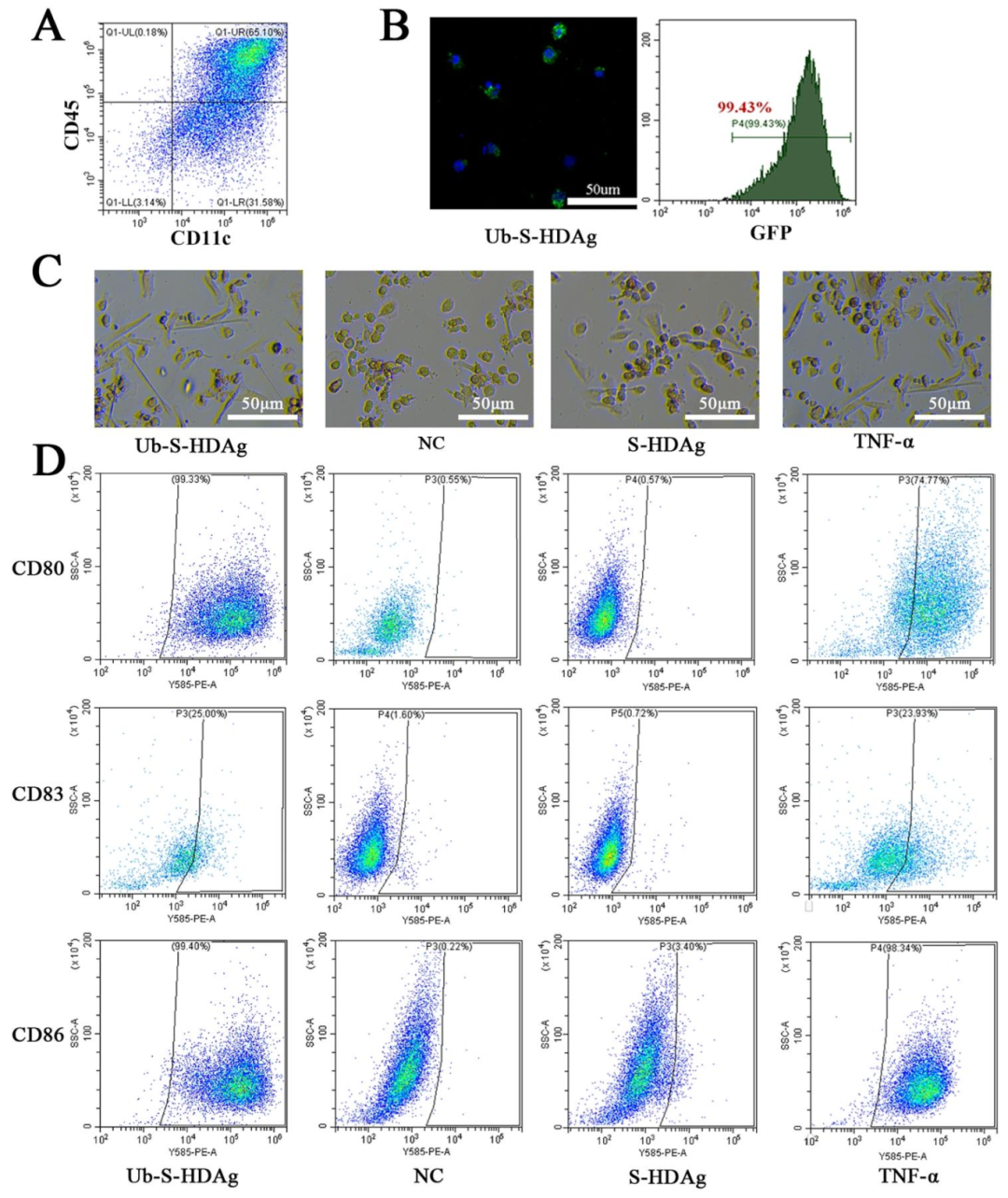
图 3:Ub-S-HDAg 诱导 DC 成熟
该图展示 DC 活化效果:(A)DC 分离纯度:PBMC 分离的 DC 中 CD45⁺CD11c⁺细胞占 65.10%;(B)Ub-S-HDAg 转染:免疫荧光 / 流式证实 DC 中 Ub-S-HDAg(GFP 标记)阳性率 > 90%;(C)形态:Ub-S-HDAg 组 DC 形成悬浮细胞簇,树突突起更丰富;(D)流式定量:CD80/CD83/CD86 在 Ub-S-HDAg 组表达显著高于 S-HDAg/NC 组,接近 TNF-α 阳性对照。图示 Ub-S-HDAg 可有效诱导 DC 成熟。
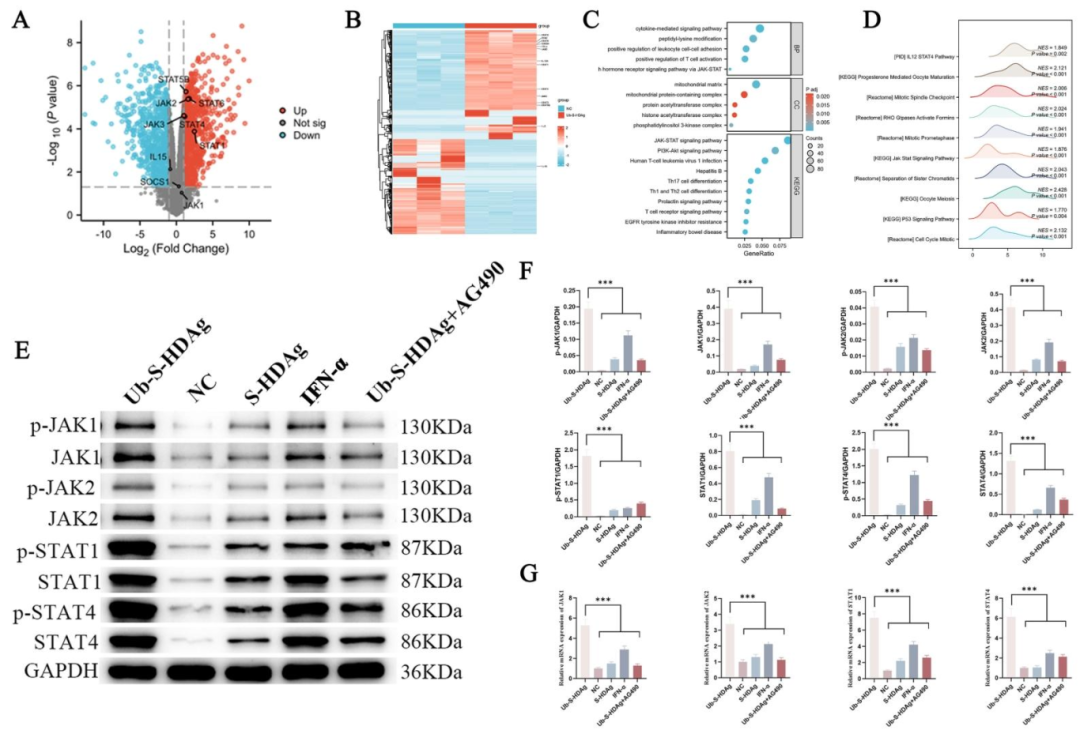
图 4:Ub-S-HDAg 激活 CD8⁺T 细胞的 JAK/STAT 通路
该图解析机制:(A-B)转录组:火山图显示 4499 个差异基因,热图显示 JAK/STAT 相关基因上调;(C-D)KEGG/GO/GSEA:JAK/STAT 通路富集最显著(FDR<0.001);(E-G)WB/qPCR:Ub-S-HDAg 组 JAK1/JAK2/STAT1/STAT4 及其磷酸化水平升高,AG490 可阻断,mRNA 水平与蛋白一致。图示 JAK/STAT 通路是 Ub-S-HDAg 激活 CD8⁺T 细胞的核心通路。
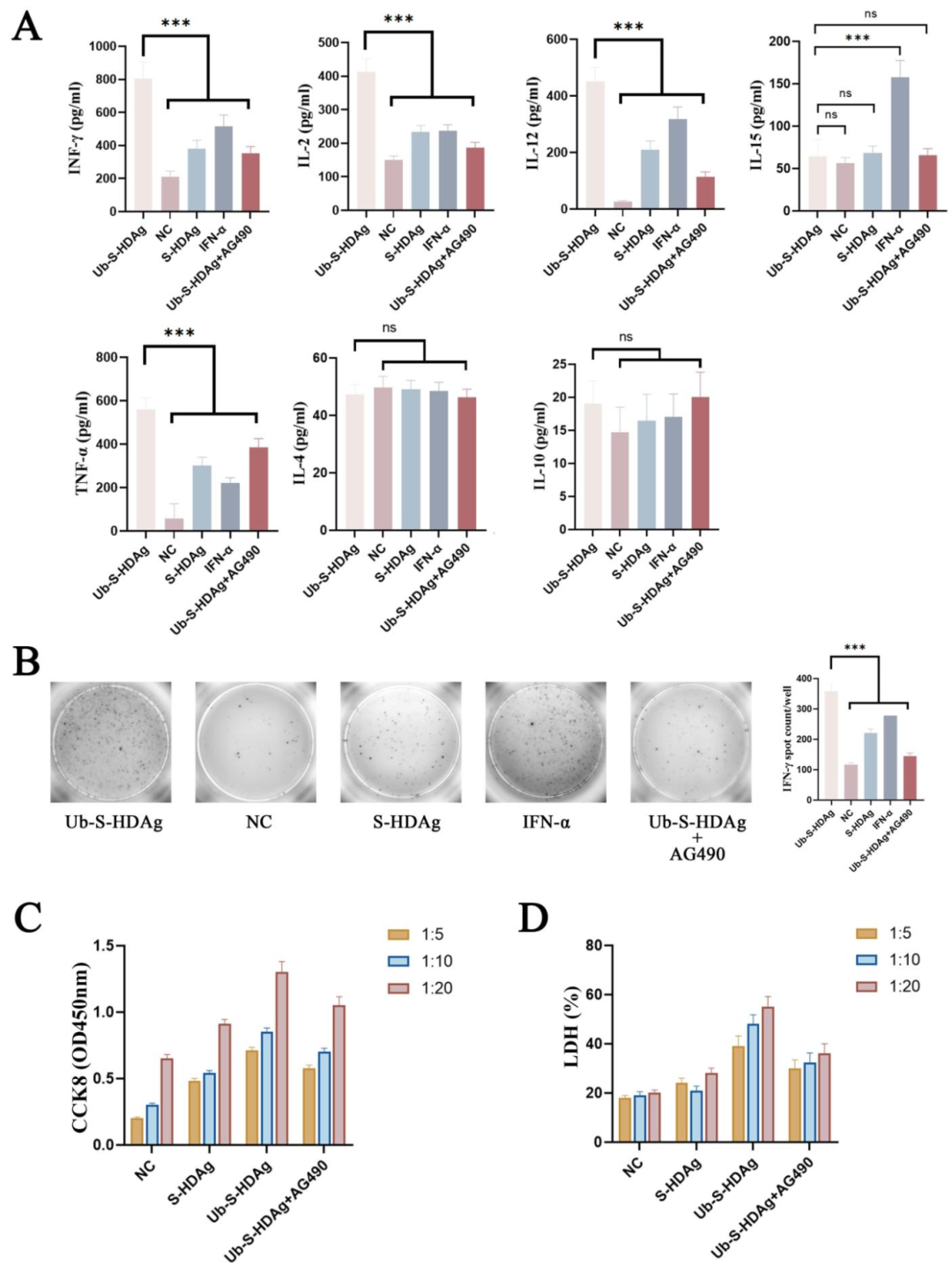
图 5:Ub-S-HDAg 增强 CD8⁺T 细胞免疫功能
该图验证 CD8⁺T 细胞效应:(A)ELISA:Ub-S-HDAg 组 IFN-γ、IL-2、IL-12、TNF-α 显著升高,IL-4/IL-10 无差异;(B)ELISPOT:Ub-S-HDAg 组 IFN-γ 分泌斑点数是 NC 组的 3 倍;(C-D)增殖与毒性:CCK-8 显示 Ub-S-HDAg 组 CD8⁺T 细胞增殖率升高 40%,LDH 法显示 E/T=1:20 时细胞毒性达 55.48%,AG490 可抑制。图示 Ub-S-HDAg 通过 JAK/STAT 增强 CD8⁺T 细胞的增殖与细胞毒性。
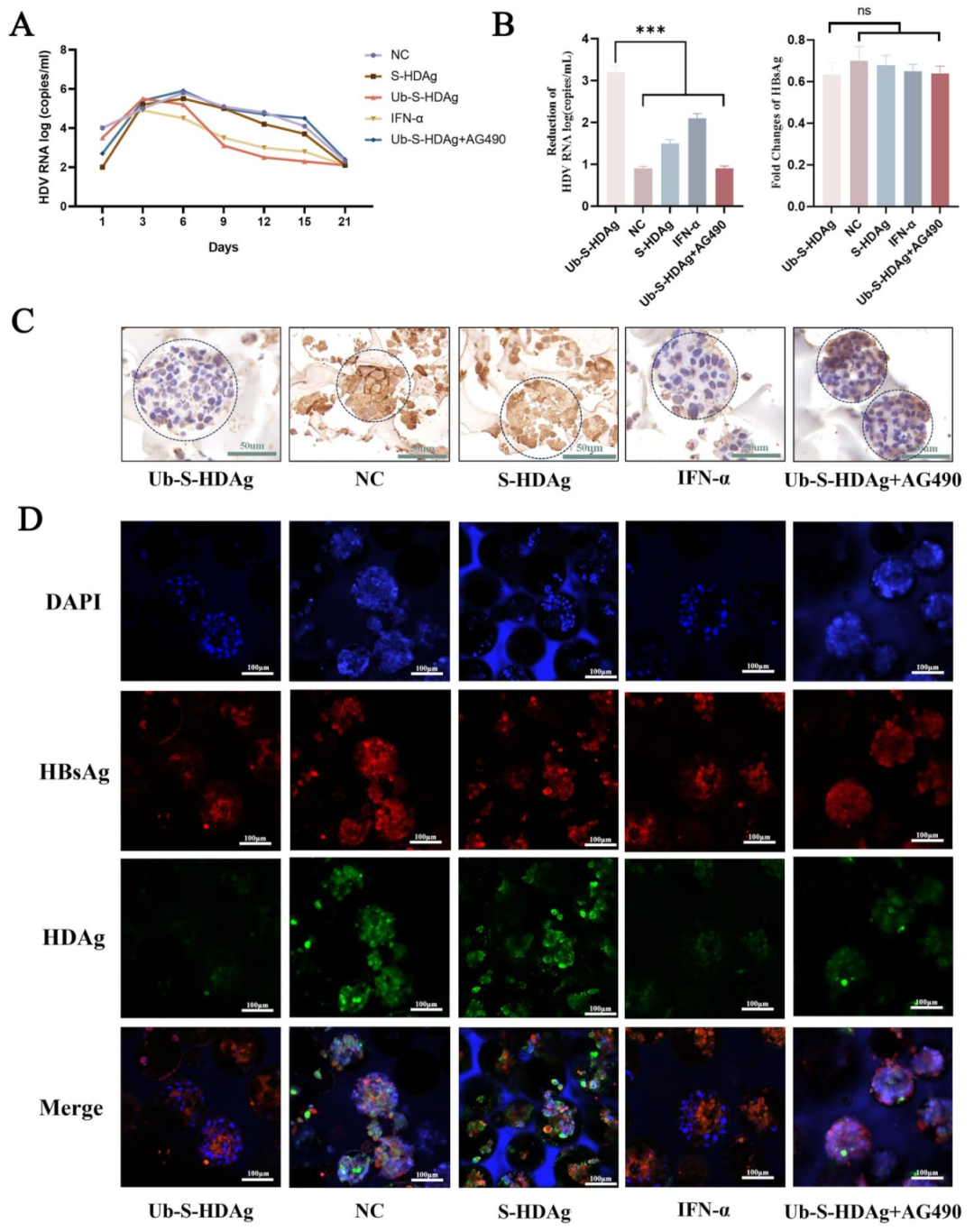
图 6:Ub-S-HDAg 抑制肝类器官中 HDV 复制
该图呈现抗病毒效果:(A)病毒载量:Ub-S-HDAg 组 HDV RNA 随时间持续下降,21 天较 NC 组低 60%,AG490 处理后下降幅度缩小;(B)HBsAg:各组无显著差异,排除对 HBV 的影响;(C-D)免疫组化 / 荧光:Ub-S-HDAg 组 HDAg 阳性区域减少 50%,效果接近 IFN-α 阳性对照。图示 Ub-S-HDAg 诱导的 CD8⁺T 细胞可特异性抑制 HDV 复制。
上海六院与英国帝国理工团队在《Antiviral Research》发表研究,基于 FDA 合规的 PEG-ICC 支架构建 iPSC 来源 HBV/HDV 共感染肝类器官(可支持病毒复制与分泌),发现泛素化 HDAg(Ub-S-HDAg)能促进 DC 成熟,通过 JAK/STAT 通路激活 CD8⁺T 细胞(增强细胞因子分泌与毒性),在类器官和小鼠模型中均抑制 HDV 复制;局限性为模型仅维持 28 天、未用患者 iPSC 验证。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
下一篇:炎症与肝脂质代谢研究新工具丨THP-1 条件培养基诱导的 HepG2 细胞模型