常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-14 09:04:07 细胞资源库平台 访问量:182
在生物医学研究和药物开发领域,生物发光成像技术因其高信噪比而被广泛应用于细胞测定和动物成像研究。然而,传统的荧光素酶种类有限,限制了同时成像多个分子和细胞事件的能力。为了突破这一限制,科学家们开发了一种新型的ATP非依赖性荧光素酶——NanoLuc(NL),它源自深海虾Oplophorus gracilirostris,并经过工程改造以增强蛋白质稳定性。NanoLuc作为一种小型(19 kDa)、高亮度的荧光素酶,其亮度是传统萤火虫或海肾荧光素酶的100倍,并且使用furimazine作为底物产生明亮的辉光型发光。NanoLuc的意义在于其为双报告基因生物发光分子成像提供了新的可能。它不仅可以在活体小鼠的表层和深层组织中成像,而且其生物发光随时间的变化可以用来定量肿瘤生长,甚至在少量血清中也能检测到分泌的NL。此外,NanoLuc与萤火虫荧光素酶的结合使用,为在完整细胞和活体小鼠中定量TGF-β信号传导的两个关键步骤提供了一种新型双荧光素酶成像策略,从而在正常生理、疾病和药物开发中扩展了信号转导的成像能力。NanoLuc的作用不仅体现在其高灵敏度和高稳定性上,它还具有更小的尺寸,这使得在标记细胞和蛋白质时对样本的侵入性更小,有助于保持细胞或组织的天然状态。NanoLuc的快速反应、低背景发光和多样灵活等特点,使其在生物学和医学研究中具有广泛的应用前景。因此,NanoLuc作为一种新的报告基因,不仅增强了我们对生物过程的理解和疾病机理的研究,而且在开发潜在治疗方法和疗法方面发挥了重要作用。
英文标题:Ratiometric bioluminescent detection of Cu(II) ion based on differences in enzymatic reaction kinetics of two luciferase variants
中文标题:基于两种荧光素酶变体酶促反应动力学差异的铜离子比率型生物发光检测
发表期刊:《Talanta》
影响因子:6.1
作者单位:
1.Graduate School of Pharmaceutical Science, Osaka University, Suita, Osaka, 565-0871, Japan
2.SANKEN (The Institute of Scientific and Industrial Research), Osaka University, Ibaraki, Osaka, 567-0047, Japan
3.Transdimensional Life Imaging Division, Institute for Open and Transdisciplinary Research Initiative, Osaka University, Suita, Osaka, 565-0871, Japan
4.Research Institute for Electronic Science, Hokkaido University, Sapporo, Hokkaido, 001-0020, Japan
作者信息:
Ti Wu、Md Nadim Hossain、Mitsuru Hattori、Takeharu Nagai*(* 为通讯作者)
铜(Cu)是人体必需的微量元素,参与细胞呼吸、神经递质代谢等生理过程,但过量摄入会引发重金属中毒,产生活性氧并造成器官氧化损伤,还与威尔逊病等疾病相关。水体中的铜离子(Cu²⁺)是人类铜暴露的主要来源之一,铜管道腐蚀及工业生产排放均会导致水体 Cu²⁺污染,威胁公共健康和生态系统。世界卫生组织(WHO)和美国环境保护署(USEPA)分别设定了饮用水中 Cu²⁺的安全限值(<2 mg/L 和 < 1.3 mg/L),因此建立高效的 Cu²⁺检测方法至关重要。传统检测方法(如电化学分析、原子吸收光谱、电感耦合等离子体质谱)虽灵敏度高,但成本高、操作复杂且需专业仪器;基于化学染料的比色和荧光检测方法需大型光学设备,便携性差。生物发光技术无需外部激发光,背景低、适合现场分析,但现有 Cu²⁺生物发光检测均为强度型,缺乏比率型检测方法的直观信号响应优势。因此,研究人员开发了基于两种荧光素酶变体酶促反应动力学差异的比率型生物发光检测方法(DERK-Cu (II)),实现 Cu²⁺的快速、便携、精准检测。
构建并纯化多种 NanoLuc(Nluc)荧光素酶变体(包括单点突变体 D9R、H57A 等,环形排列变体 cp53、cp70,以及融合型 fNanoBiT),通过生物发光强度检测筛选对 Cu²⁺抑制敏感性差异显著的变体;将高催化效率且对 Cu²⁺敏感的 Nluc (D9R) 与绿色荧光蛋白 mNeonGreen 融合,构建 Green-Nluc (D9R)(发射绿色光),以低催化效率且对 Cu²⁺不敏感的 fNanoBiT(发射蓝色光)作为另一信号源;优化两种蛋白的混合比例(最终确定 2:1),基于 Cu²⁺浓度依赖性的发光颜色变化(绿色→蓝色)建立比率型检测体系;采用智能手机相机(华为 P40 Pro)捕获生物发光图像,通过 ImageJ 软件拆分蓝、绿、红三色通道并计算蓝 / 绿通道强度比,构建 Cu²⁺浓度与颜色比率的标准曲线;评估方法的离子选择性(针对 Li⁺、Na⁺、Fe³⁺等 13 种常见金属离子);通过检测铜污染水(模拟家庭用水铜腐蚀污染)和环境水样(河流、护城河 water),并与电感耦合等离子体发射光谱(ICP-OES)结果对比,验证方法的实际应用准确性。
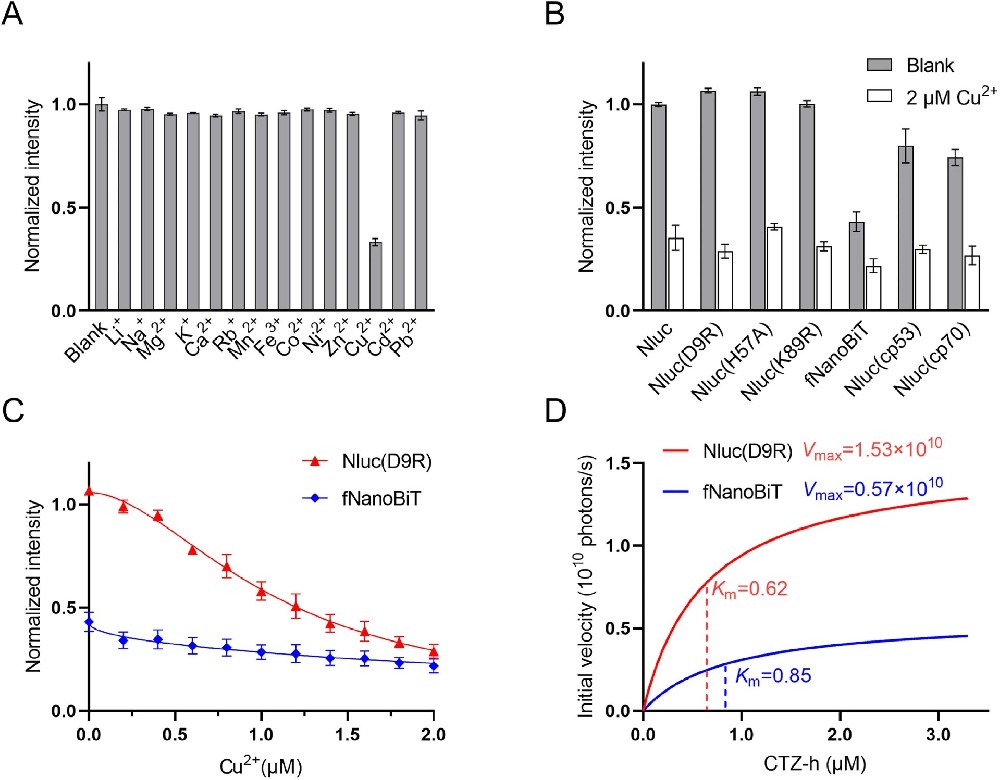
图1:Nluc 及其变体的 Cu²⁺抑制特性与酶促动力学分析
(A)离子选择性实验显示,Cu²⁺能特异性抑制 Nluc 的生物发光,其他常见金属离子(如 Li⁺、Na⁺、Mg²⁺、Fe³⁺等)无明显抑制作用,证实 Nluc 对 Cu²⁺的特异性响应;
(B)不同 Nluc 变体的 Cu²⁺抑制率对比表明,D9R 变体抑制率最高(73%),fNanoBiT 抑制率最低(49%),二者差异显著;
(C)Cu²⁺剂量 - 响应曲线显示,Nluc (D9R) 的抑制斜率(-1.84)显著高于 fNanoBiT(-0.46),表明 Cu²⁺对 Nluc (D9R) 的抑制作用更强;
(D)底物滴定实验显示,Nluc (D9R) 的最大反应速率(Vmax=1.53×10¹⁰)高于 fNanoBiT(Vmax=0.57×10¹⁰),米氏常数(Km=0.62)低于 fNanoBiT(Km=0.85),证实 Nluc (D9R) 的催化效率更高,而高催化效率酶更易受底物消耗影响,因此对 Cu²⁺介导的底物失活更敏感。
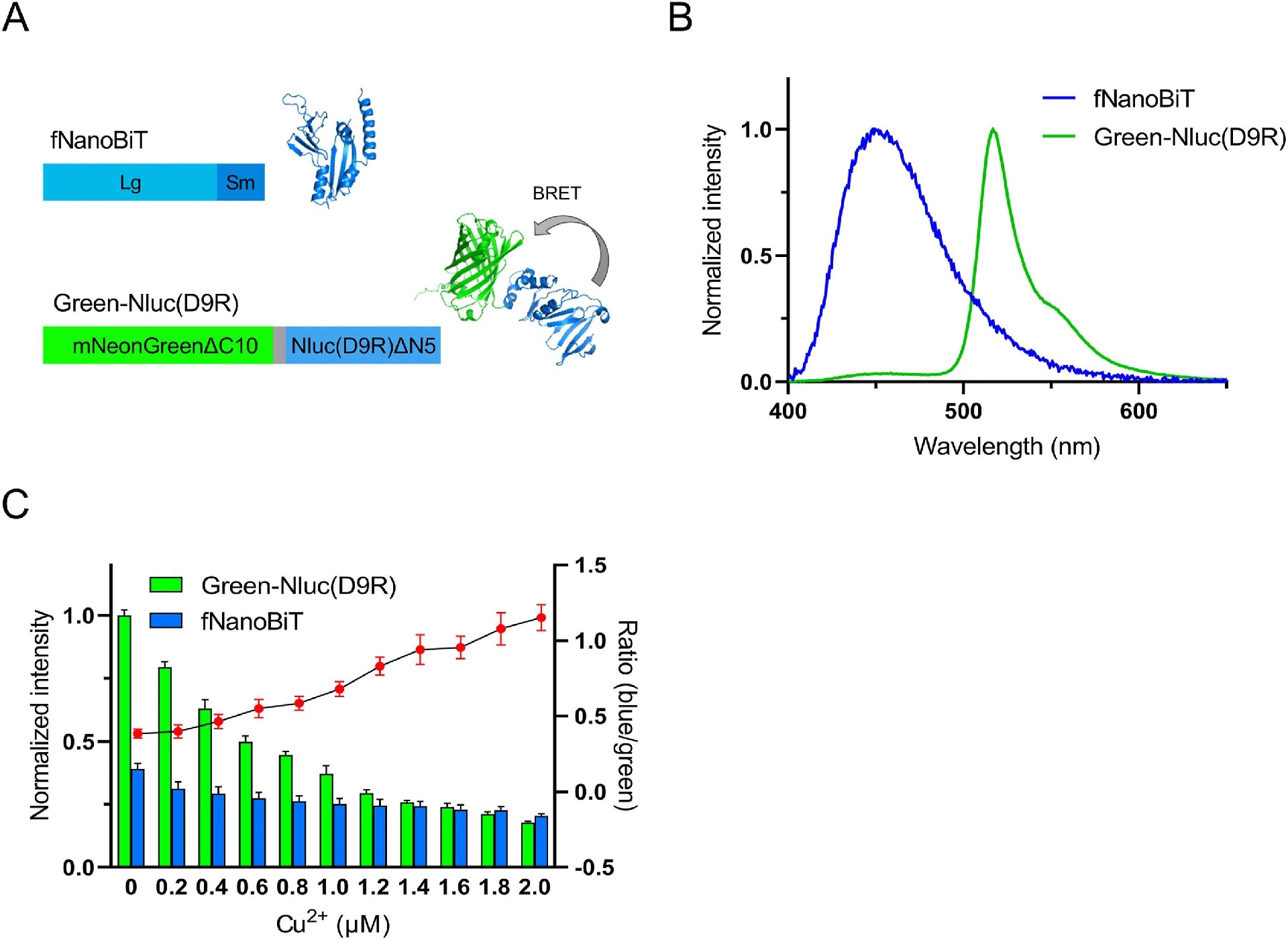
图2:两种不同颜色及 Cu²⁺响应特性的生物发光蛋白构建
(A)蛋白结构示意图:fNanoBiT 由 Nluc 的大亚基(LgBiT)和小亚基(SmBiT)融合而成;Green-Nluc (D9R) 由截短的 mNeonGreen 与 Nluc (D9R) 通过 GGGTTT linker 融合而成;
(B)生物发光光谱显示,fNanoBiT 发射蓝色光(峰值 460 nm),Green-Nluc (D9R) 因生物发光共振能量转移(BRET)发射绿色光(峰值 520 nm),二者光谱差异显著,可实现颜色区分;
(C)Cu²⁺剂量 - 响应曲线显示,随着 Cu²⁺浓度升高(0-2 μM),Green-Nluc (D9R) 的发光强度显著下降,fNanoBiT 的发光强度下降平缓,二者的发光强度比呈浓度依赖性变化,为比率型检测奠定基础。
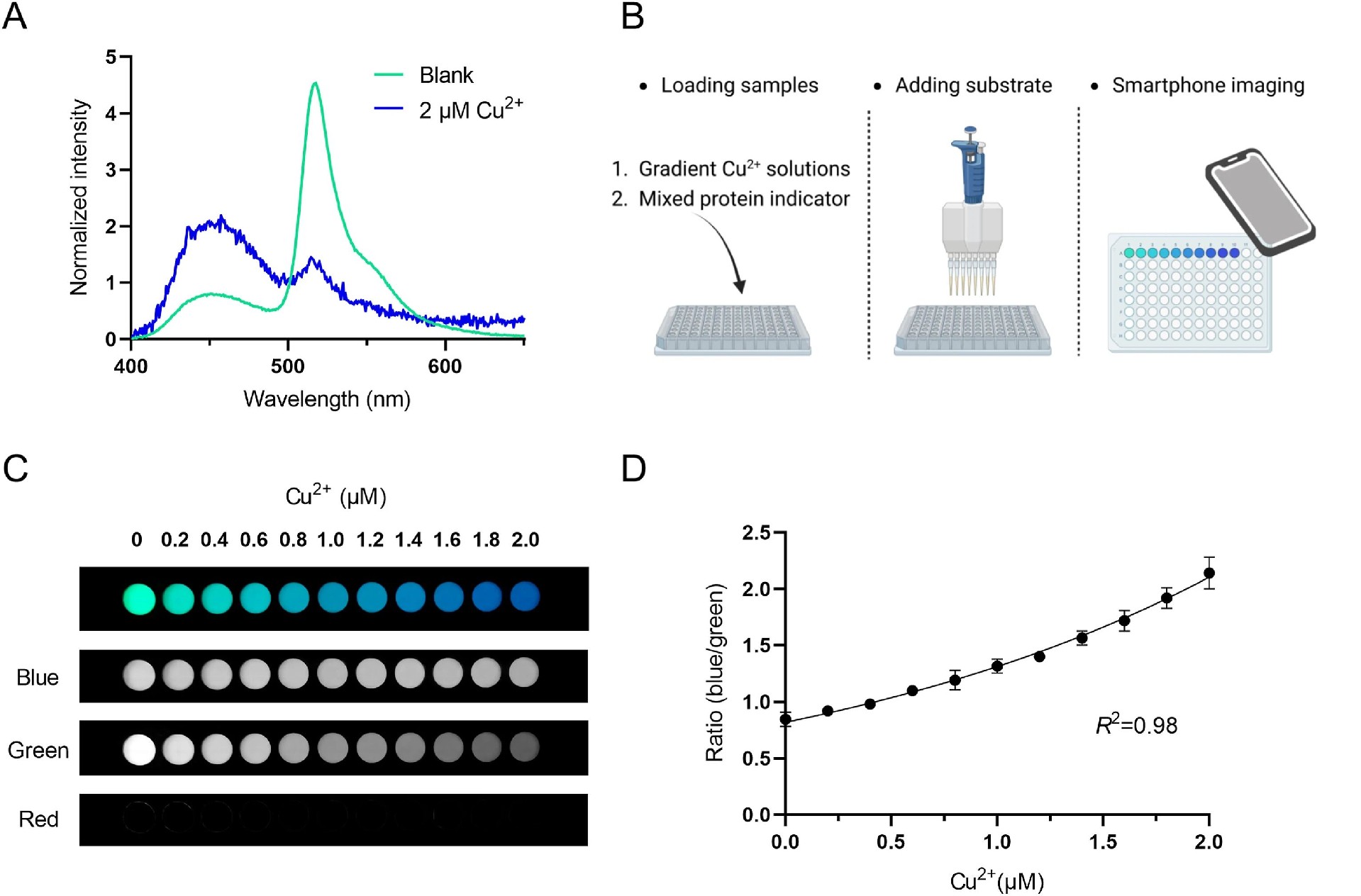
图3:智能手机相机介导的 Cu²⁺比率型检测
(A)混合蛋白的生物发光光谱显示,无 Cu²⁺时绿色光占主导,加入 2 μM Cu²⁺后蓝色光占主导,光谱峰值从 520 nm 偏移至 460 nm;
(B)检测流程示意图:依次加入梯度 Cu²⁺溶液、混合蛋白指示剂,同步添加底物后用智能手机相机成像;
(C)智能手机捕获的生物发光图像显示,随着 Cu²⁺浓度升高(0-2 μM),发光颜色从绿色逐渐梯度转变为蓝色,三色通道拆分后蓝、绿通道差异明显;(D)蓝 / 绿通道强度比与 Cu²⁺浓度的拟合曲线显示,二者呈指数增长关系(R²=0.98),检测限(LOD)低至 0.16 μM,该方法被命名为 DERK-Cu (II)(基于酶促反应动力学差异的 Cu²⁺检测)。
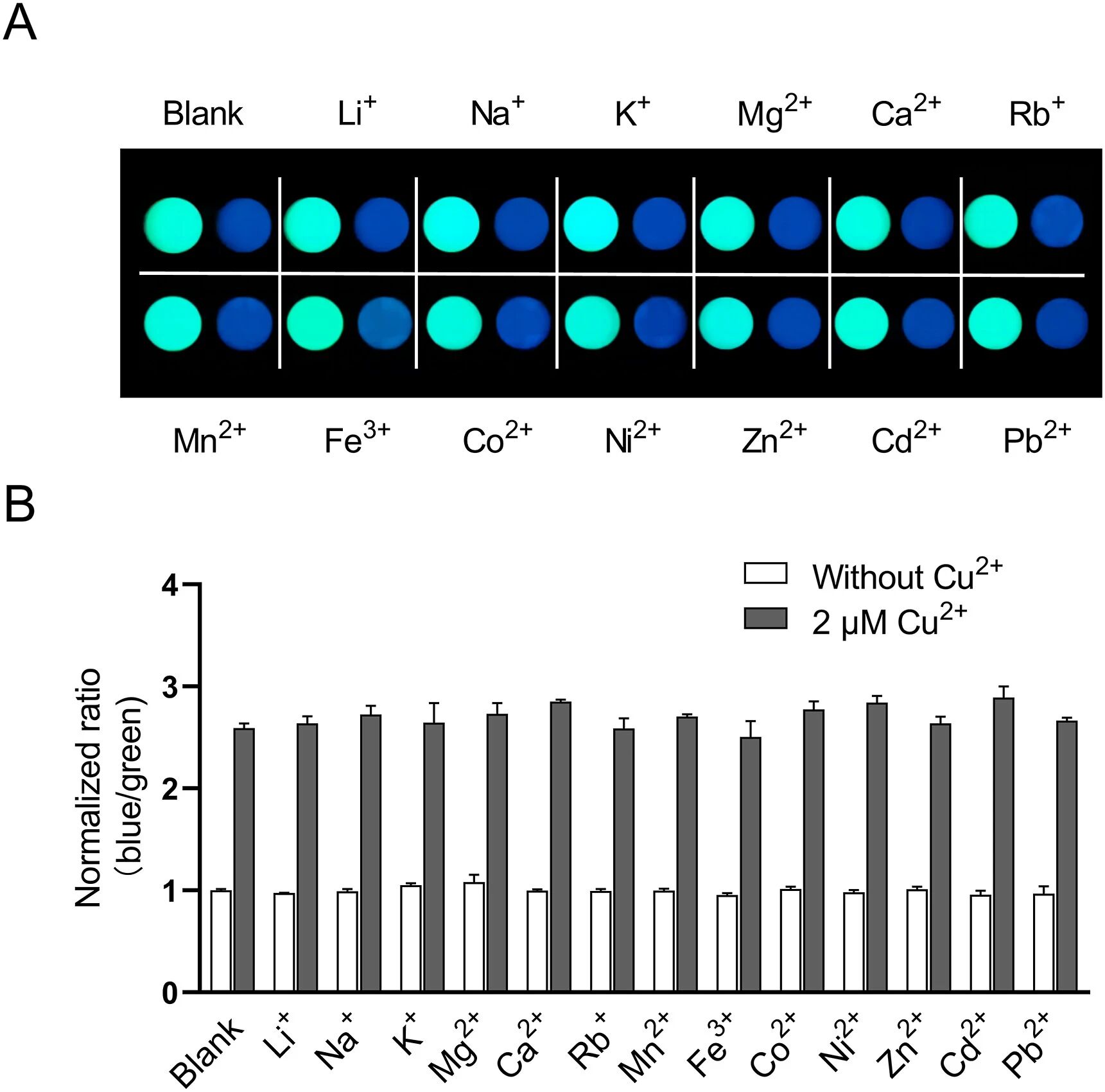
图4:DERK-Cu (II) 的离子选择性验证
(A)智能手机成像显示,20 μM 的其他金属离子(Li⁺、Na⁺、Mg²⁺等 13 种)单独存在时,混合蛋白的发光颜色与空白组无差异;与 2 μM Cu²⁺共孵育时,发光颜色仍呈现典型的 Cu²⁺依赖性蓝色转变;
(B)定量分析表明,其他金属离子对蓝 / 绿通道强度比无显著影响,既不单独激活信号,也不干扰 Cu²⁺的检测信号,证实 DERK-Cu (II) 对 Cu²⁺具有高选择性。
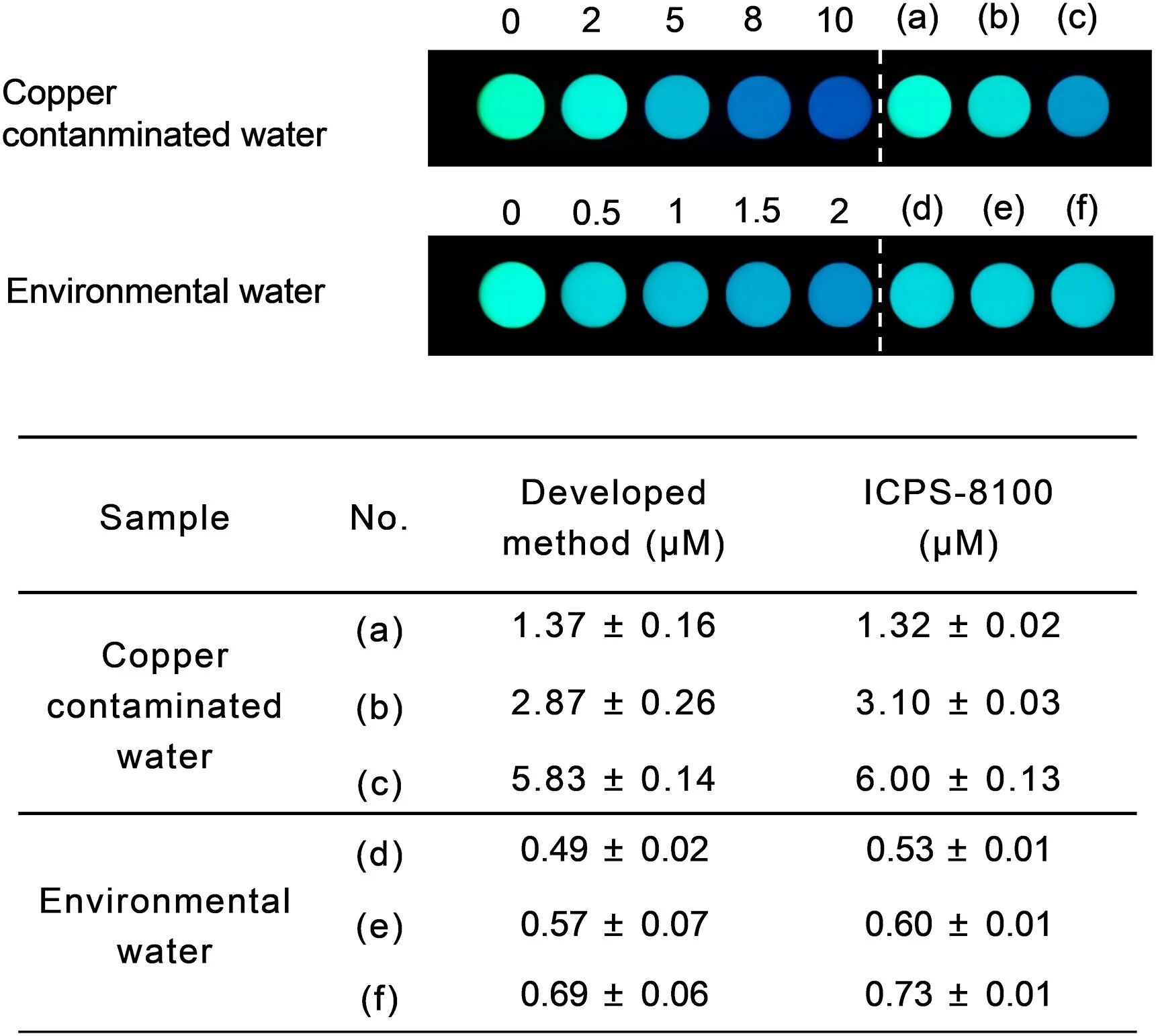
图5:实际水样中 Cu²⁺的检测应用
智能手机成像显示,铜污染水(50 μL)和环境水(100 μL)样品的发光颜色与对应浓度的 Cu²⁺标准溶液一致;定量分析结果显示,DERK-Cu (II) 检测铜污染水的 Cu²⁺浓度为 1.37-5.83 μM,检测环境水的浓度为 0.49-0.69 μM,与 ICP-OES 的检测结果误差均小于 8%,证实该方法对实际水样中 Cu²⁺的定量检测具有高准确性。
本研究开发了一种基于两种荧光素酶变体酶促反应动力学差异的比率型生物发光 Cu²⁺检测方法(DERK-Cu (II)),首次实现了 Cu²⁺的生物发光比率型检测。该方法利用 Cu²⁺对咪唑并吡嗪类荧光素酶底物的特异性失活作用,筛选出催化效率差异显著的两种 Nluc 变体 —— 高催化效率且 Cu²⁺敏感的 Green-Nluc (D9R)(发射绿色光)和低催化效率且 Cu²⁺不敏感的 fNanoBiT(发射蓝色光)。通过优化二者混合比例(2:1),实现了 Cu²⁺浓度依赖性的发光颜色从绿色到蓝色的梯度转变,可通过智能手机相机捕获并定量分析(蓝 / 绿通道强度比)。该方法对 Cu²⁺具有高灵敏度(LOD=0.16 μM)和高选择性,不受其他常见金属离子干扰,且无需专业仪器,操作简便、便携性强。实际应用验证显示,其对铜污染水和环境水样中 Cu²⁺的检测结果与 ICP-OES 高度一致,误差小于 8%。此外,该基于酶促反应动力学差异的比率型检测策略(DERK)具有普适性,可扩展至抗体检测等其他目标分析领域,为现场快速检测和床旁诊断提供了新工具。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:牛磺胆酸钠共转运多肽缺乏通过调控药物代谢酶表达减轻对乙酰氨基酚诱导的肝毒性
下一篇:液态金属纳米粒介导线粒体损伤增强免疫原性细胞死亡用于癌症疫苗治疗