常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-13 09:00:00 细胞资源库平台 访问量:75
Reporter THP1 Cell Line 细胞系是以 THP-1 为工具细胞,采用慢病毒感染的方式,构建稳定表达报告基因的细胞系,可用于检测信号通路转导。在被PMA、INF-α等刺激后,目标信号通路被激活,会启动下游特定基因的表达,这个表达过程会同时带动“报告基因”的表达。通过检测报告基因的信号强度,可以间接、定量、灵敏地衡量该信号通路的激活程度。
THP-1细胞本身来源于人单核细胞,可以分化为巨噬细胞样细胞,是研究先天免疫的经典模型。报告基因株的建立使其功能更强大。THP-1报告基因株是免疫学、炎症性疾病、药物研发等领域不可或缺的强大工具。它可以将一个复杂的、内在的生物学过程(信号通路激活/基因表达)转变为一个易于检测、可定量的物理信号(光或荧光)。这使得研究人员能够高通量地筛选药物,精确地量化免疫反应强度,直观地研究信号通路机制。
英文标题:Assessment of costimulation and coinhibition in a triple parameter T cell reporter line: Simultaneous measurement of NF-κB, NFAT and AP-1
中文标题:三参数 T 细胞报告细胞系的建立与应用:同时检测 NF-κB、NFAT 和 AP-1 活性
发表期刊:《Journal of Immunological Methods》
影响因子:1.6
作者单位:
1.Division of Immune Receptors and T Cell Activation, Institute of Immunology, Center for Pathophysiology, Infectiology and Immunology, Medical University of Vienna, Vienna, Austria
2.Department of Laboratory Medicine, Medical University of Vienna, Vienna, Austria
3.Institute for Hygiene and Applied Immunology, Center for Pathophysiology, Infectiology and Immunology, Medical University of Vienna, Vienna, Austria
作者信息:
Sabrina Jutz、Judith Leitner、Klaus Schmetterer、Peter Steinberger*(* 为通讯作者)
T 细胞激活依赖 T 细胞受体(TCR)信号与共刺激信号的协同作用,同时受共抑制信号调控,最终通过转录因子 NF-κB、NFAT 和 AP-1 激活下游基因表达,驱动细胞增殖、细胞因子产生及分化。现有研究多依赖单一或双参数报告系统,无法同时分析三种转录因子的活性,限制了对 T 细胞信号网络的全面解析。Jurkat T 细胞系是研究 T 细胞信号的经典模型,但缺乏部分内源性共刺激 / 共抑制受体。因此,研究人员构建了可同时检测 NF-κB、NFAT 和 AP-1 活性的三参数报告细胞系(TPR),并验证其在共刺激(CD2、CD28、4-1BB)和共抑制(PD-1、BTLA)信号评估中的应用价值。
构建模块化逆转录病毒报告载体:NF-κB 响应元件驱动青色荧光蛋白(CFP)表达,NFAT 响应元件驱动增强型绿色荧光蛋白(eGFP)表达,AP-1 响应元件驱动单体樱桃红色荧光蛋白(mCherry)表达;将三种载体共转染人 Jurkat E6.1 T 细胞,通过单克隆筛选获得静息状态下低荧光、激活后高荧光的三参数报告细胞系(TPR);构建表达膜结合抗 CD3 单链抗体的 T 细胞刺激细胞(TCS),并分别表达共刺激配体(CD58、CD80、4-1BBL)或共抑制配体(PD-L1、HVEM);通过共培养或板结合抗体刺激 TPR 细胞,流式细胞术检测 CFP、eGFP、mCherry 荧光强度,评估转录因子活性;利用 shRNA 敲低靶转录因子(NF-κB1、NFATc3、c-Fos)验证报告系统特异性;通过环孢素 A(CsA)、佛波酯(PMA)、离子霉素(Ionomycin)处理验证信号通路特异性;在 TPR 细胞中异位表达 4-1BB、PD-1、BTLA,评估非内源性共信号分子对转录因子活性的影响。
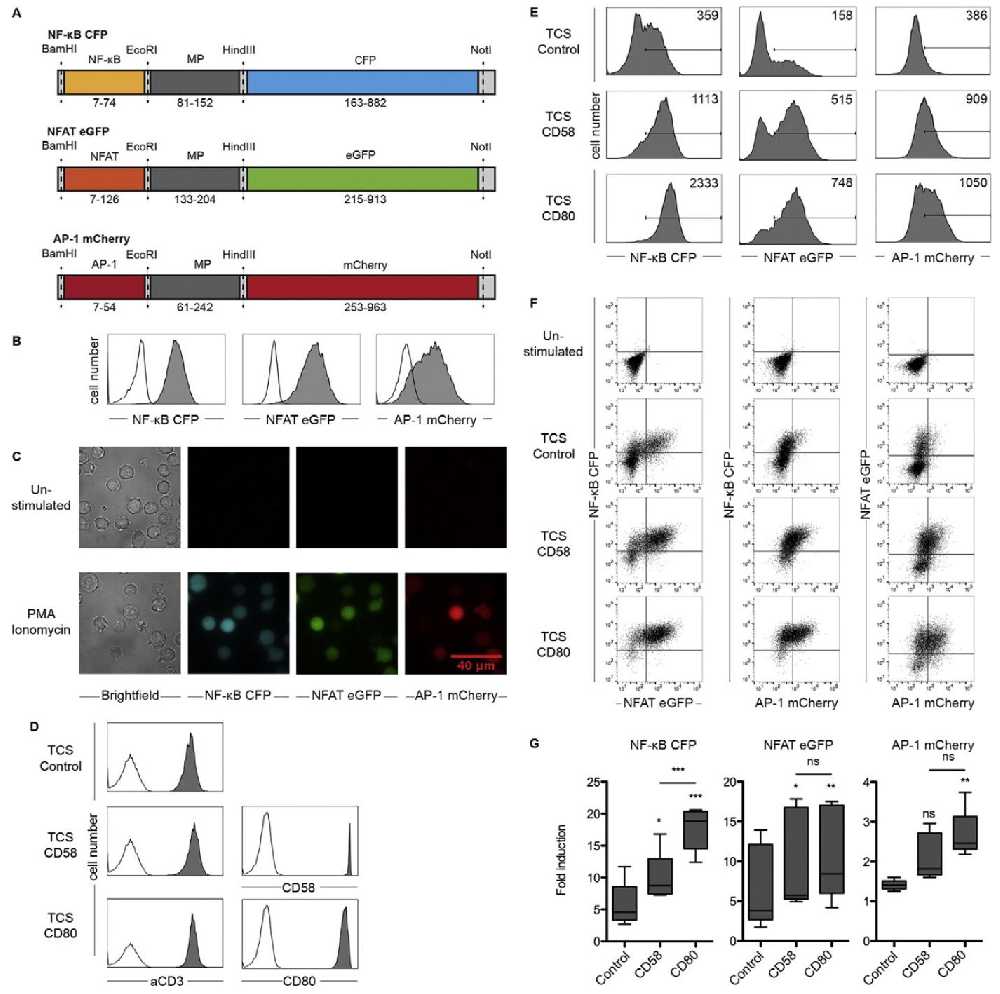
图1:三参数报告细胞系(TPR)的构建与验证
(A)报告载体示意图:含转录因子响应元件(RE)、最小启动子(MP)及对应荧光蛋白基因,含独特酶切位点便于模块替换;(B)PMA + 离子霉素激活后,TPR 细胞的 CFP、eGFP、mCherry 荧光强度显著升高,证实报告系统有效;(C)荧光显微镜显示,激活后 TPR 细胞呈现三色荧光,静息细胞无明显荧光;(D)FACS 验证 TCS 表面分子表达:TCS-control 无共刺激配体,TCS-CD58、TCS-CD80 分别高表达 CD58、CD80;(E、F)共培养实验显示,TCS-control 仅诱导适度荧光,TCS-CD58、TCS-CD80 可显著增强三种荧光强度;(G)定量分析表明,CD28(CD80 介导)对 NF-κB 的激活作用显著强于 CD2(CD58 介导),二者对 NFAT 和 AP-1 的激活无显著差异。
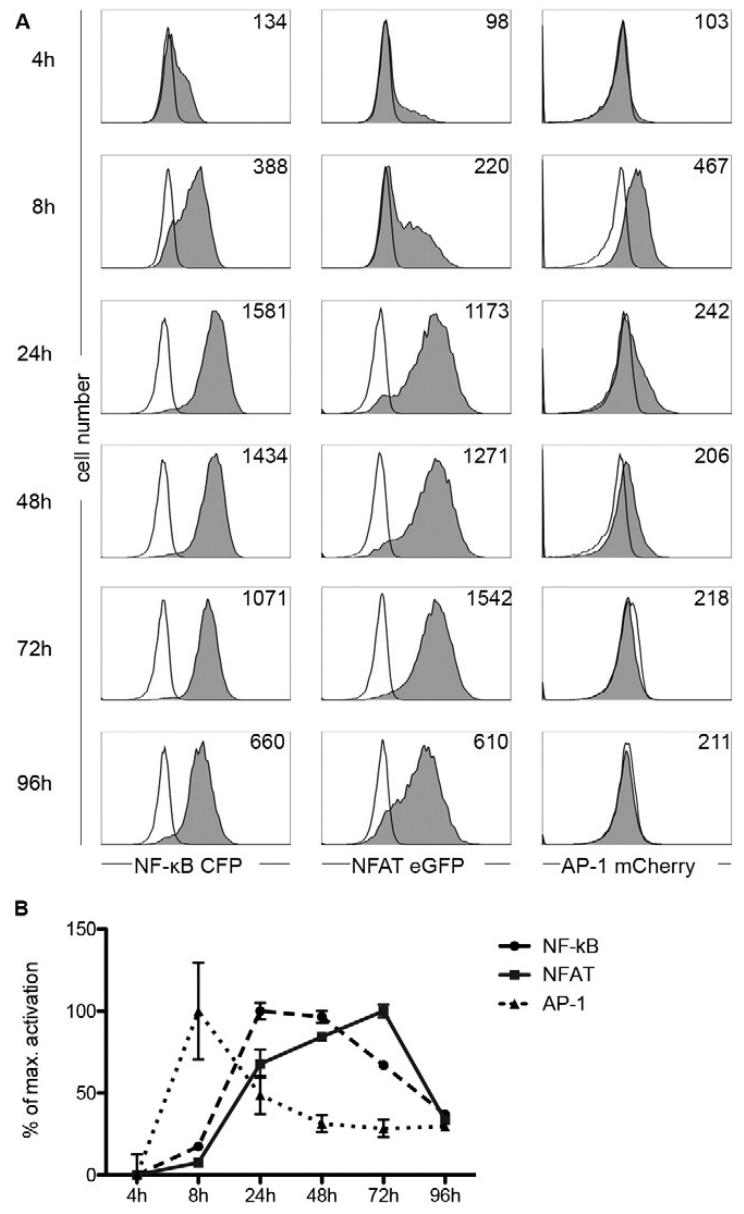
图2:NF-κB、NFAT 和 AP-1 的激活动力学
TPR 细胞与 TCS-CD80 共培养后,AP-1 活性在 8 小时达峰,NF-κB 在 24 小时达峰,NFAT 激活最慢,72 小时达峰,随后三者活性均逐渐下降,证实三种转录因子的激活时序存在差异。
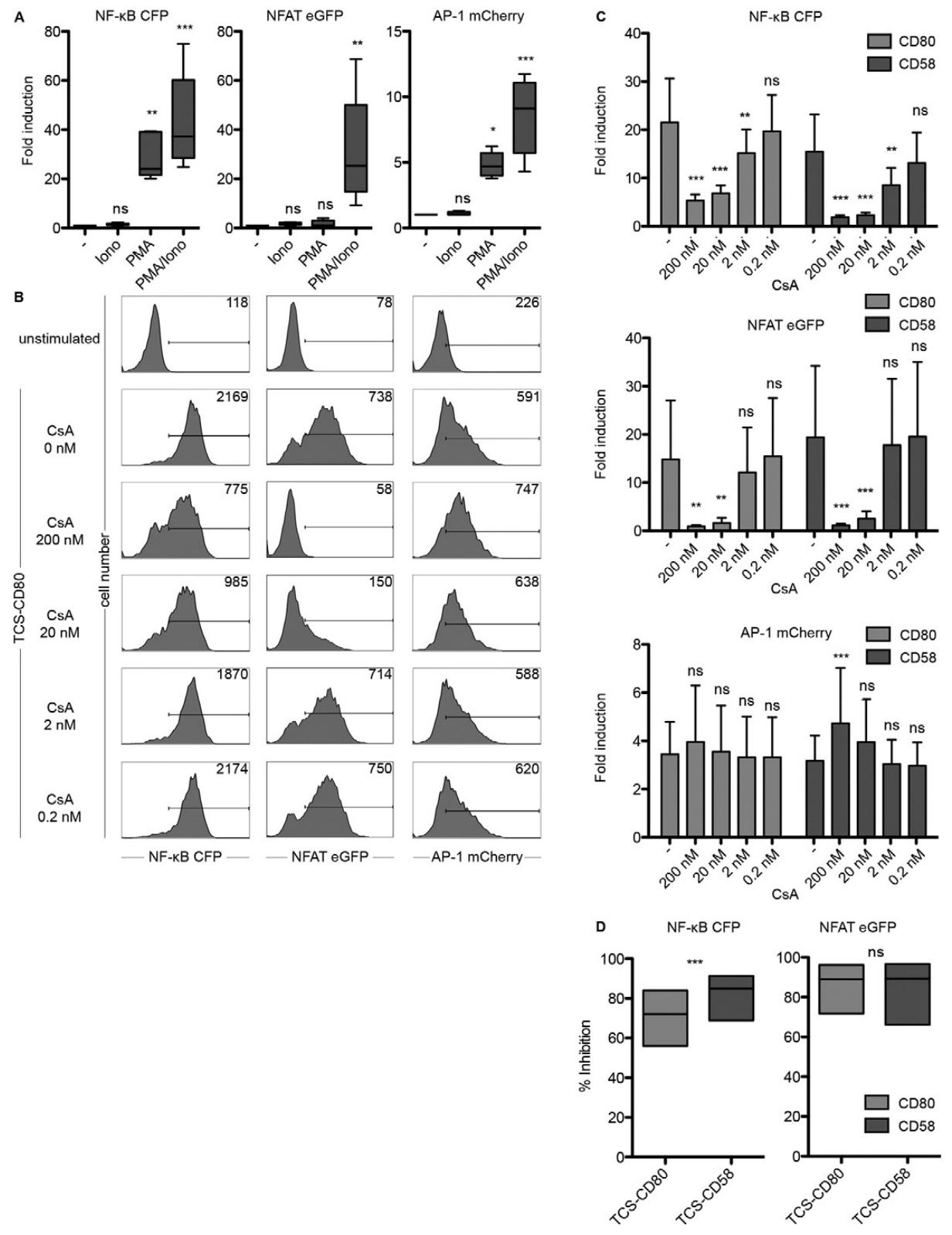
图3:PMA、离子霉素和环孢素 A 对报告系统的影响
(A)PMA 单独处理可激活 NF-κB 和 AP-1,离子霉素单独无激活作用,二者联合可显著激活 NFAT,并进一步增强 NF-κB 和 AP-1 活性;(B、C)CsA 可剂量依赖性抑制 NF-κB 和 NFAT 活性,对 AP-1 无显著影响;(D)CsA 对 CD2 介导的 NF-κB 抑制作用强于 CD28 介导的信号,对 NFAT 的抑制无通路差异。
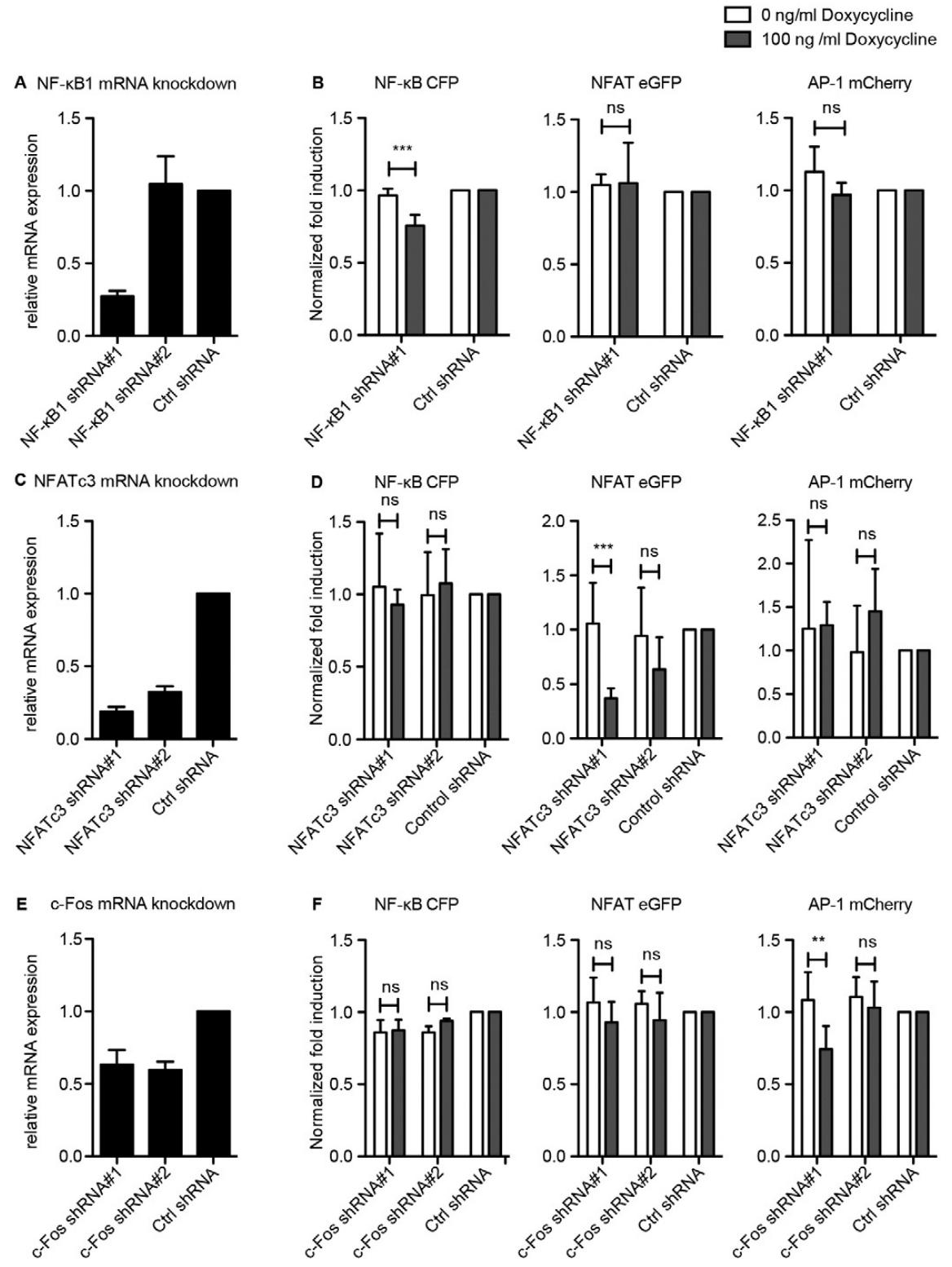
图4:报告系统的特异性验证(shRNA 敲低实验)
(A、C、E)qRT-PCR 证实,靶向 NF-κB1、NFATc3、c-Fos 的 shRNA 可有效敲低对应基因 mRNA 表达;(B、D、F)FACS 分析显示,NF-κB1 敲低仅抑制 CFP 荧光,NFATc3 敲低仅抑制 eGFP 荧光,c-Fos 敲低仅抑制 mCherry 荧光,证实报告系统具有高度特异性。
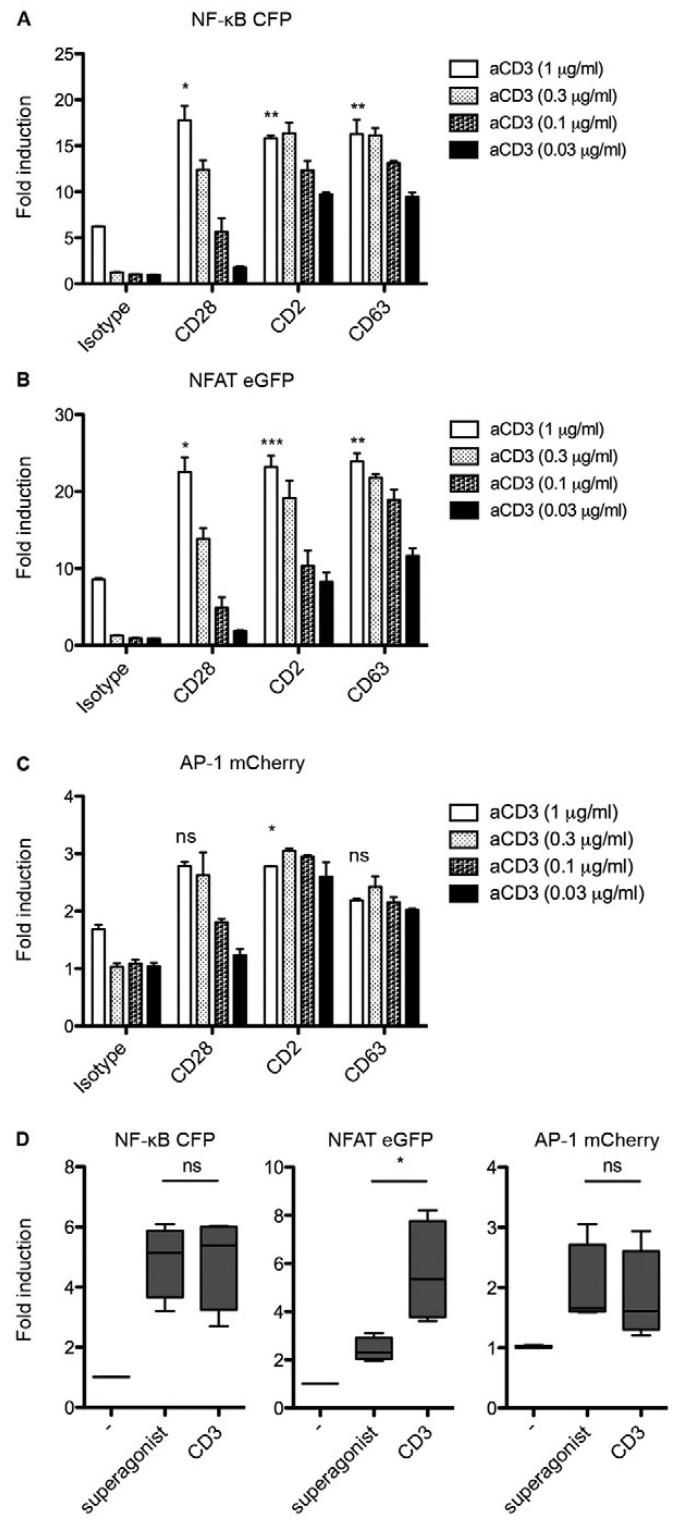
图5:抗体介导的共刺激对转录因子活性的影响
(A-C)板结合抗 CD3 抗体可适度激活报告系统,联合抗 CD2、CD28 或 CD63 抗体可显著增强三种荧光强度,且 CD63 抗体的共刺激效果与 CD2、CD28 抗体相当;(D)CD28 超激动剂可在无 TCR 信号时激活 NF-κB 和 AP-1,但对 NFAT 的激活显著弱于抗 CD3 抗体。
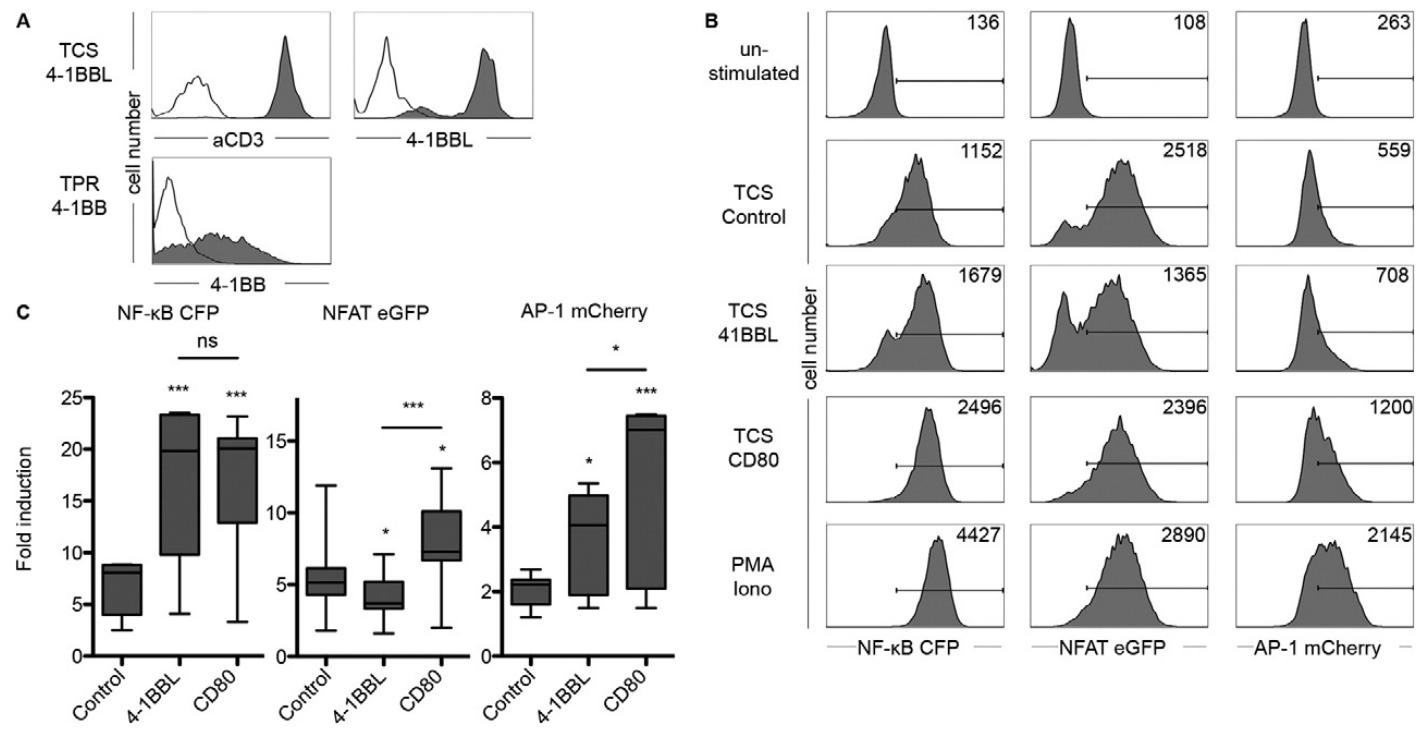
图6:4-1BB 共刺激对转录因子活性的影响
(A)FACS 验证 TPR-4-1BB 细胞高表达 4-1BB,TCS-4-1BBL 高表达 4-1BBL;(B、C)共培养实验显示,4-1BBL 可显著增强 NF-κB 和 AP-1 活性,抑制 NFAT 活性,且 CD80 的共刺激效果强于 4-1BBL。
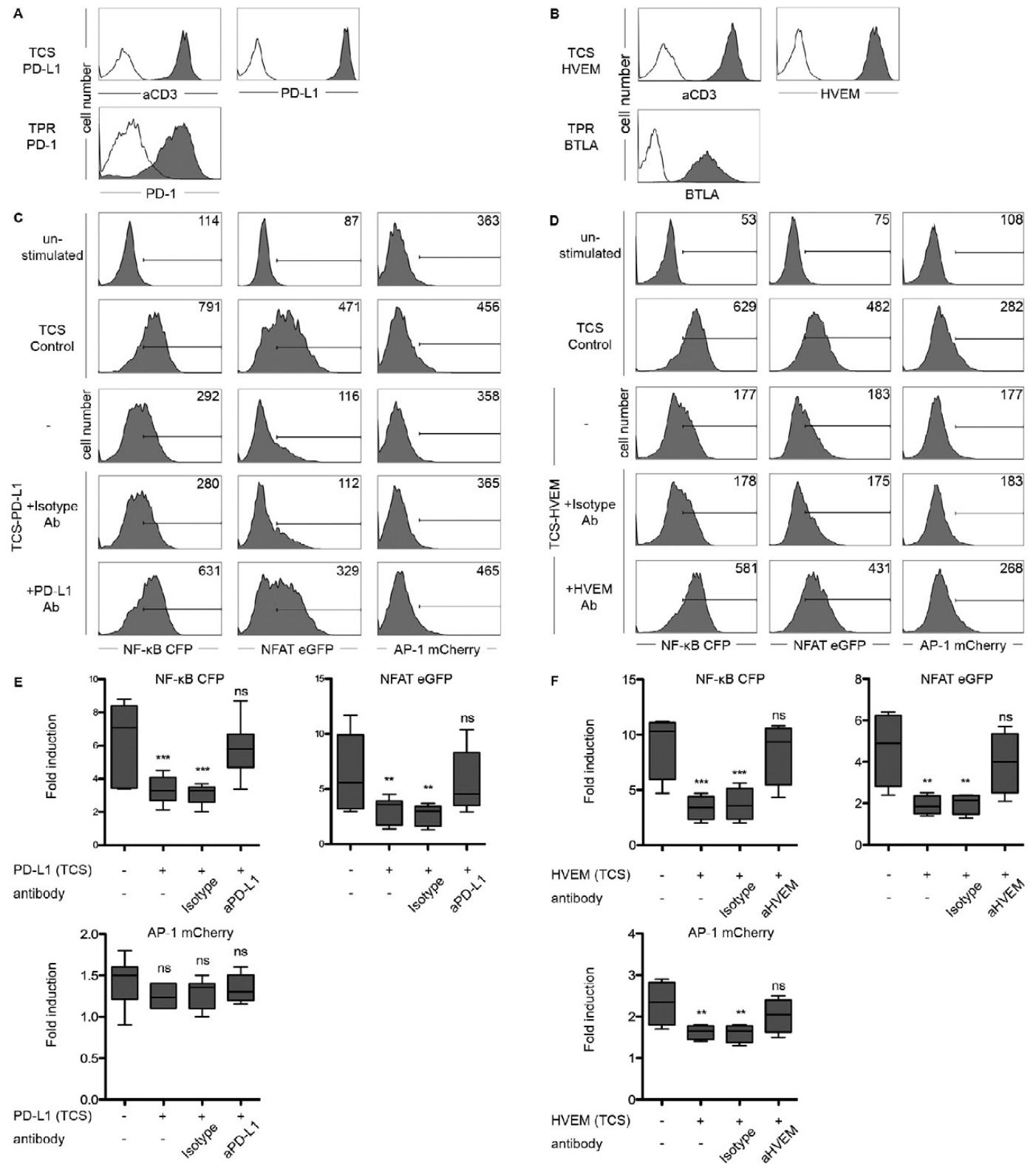
图7:PD-1 和 BTLA 共抑制对转录因子活性的影响
(A、B)FACS 验证 TPR-PD-1、TPR-BTLA 细胞分别高表达 PD-1、BTLA,TCS-PD-L1、TCS-HVEM 分别高表达 PD-L1、HVEM;(C、E)PD-1 与 PD-L1 结合可显著抑制 NF-κB 和 NFAT 活性,对 AP-1 无显著抑制;(D、F)BTLA 与 HVEM 结合可显著抑制 NF-κB、NFAT 和 AP-1 活性,且抗 HVEM 抗体可阻断该抑制作用。
本研究成功构建了基于 Jurkat 细胞的三参数报告系统(TPR),可通过 CFP、eGFP、mCherry 三种荧光信号同时、特异性检测 NF-κB、NFAT 和 AP-1 的活性。该系统可有效区分不同共刺激信号(CD2、CD28、CD63、4-1BB)的作用差异,明确共抑制信号(PD-1、BTLA)对三种转录因子的选择性调控:PD-1 主要抑制 NF-κB 和 NFAT,BTLA 可同时抑制三种转录因子。此外,TPR 细胞可通过异位表达非内源性共信号受体,拓展对新型共刺激 / 共抑制通路的研究。该工具为解析 T 细胞信号网络、筛选免疫调节剂、优化嵌合抗原受体(CAR)设计等提供了高效、便捷的平台,具有广泛的应用前景。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:干细胞治疗阿尔茨海默病的机制、研究进展、临床挑战及技术整合综述
下一篇:牛磺胆酸钠共转运多肽缺乏通过调控药物代谢酶表达减轻对乙酰氨基酚诱导的肝毒性