常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2024-06-06 15:59:46 细胞资源库平台 访问量:376
今天推荐的文献《TLR3 activation enhances abscopal effect of radiotherapy in HCC by promoting tumor ferroptosis》引用,影响因子为11.1。
英文标题:TLR3 activation enhances abscopal effect of radiotherapy in HCC by promoting tumor ferroptosis
中文标题:TLR3信号激活通过促进肿瘤铁死亡增强肝癌放疗的远端效应
发表期刊:《EMBO Molecular Medicine》
影响因子:11.1
作者单位:福建医科大学
作者信息:邱丽满(一作),季洪兵,王凯,蔡志雄(通讯)和刘小龙(通讯)
肝癌(HCC)是全球第六大常见肿瘤。放疗(RT)在治疗HCC中很少使用,因为传统上认为它会引起严重的肝脏损伤。现代精确放疗能够对肿瘤进行高剂量照射,对周围正常组织损伤可忽略不计。放疗能够引起肿瘤细胞的DNA损伤,导致肿瘤细胞死亡或生长停滞。放疗还可能在某些情况下诱导非照射部位的肿瘤退缩,称为“远端效应”。
本研究构建了双侧HCC皮下肿瘤小鼠模型,研究聚肌胞苷酸(poly(I:C))对放疗期间远隔效应的影响及其分子机制。通过转录组测序分析了不同处理后小鼠肿瘤细胞死亡的调控情况。评估了poly(I:C)对肿瘤细胞铁死亡的影响,以及通过树突细胞的肿瘤新抗原呈递能力增强激活CD8+ T细胞浸润到远处肿瘤组织中的作用。
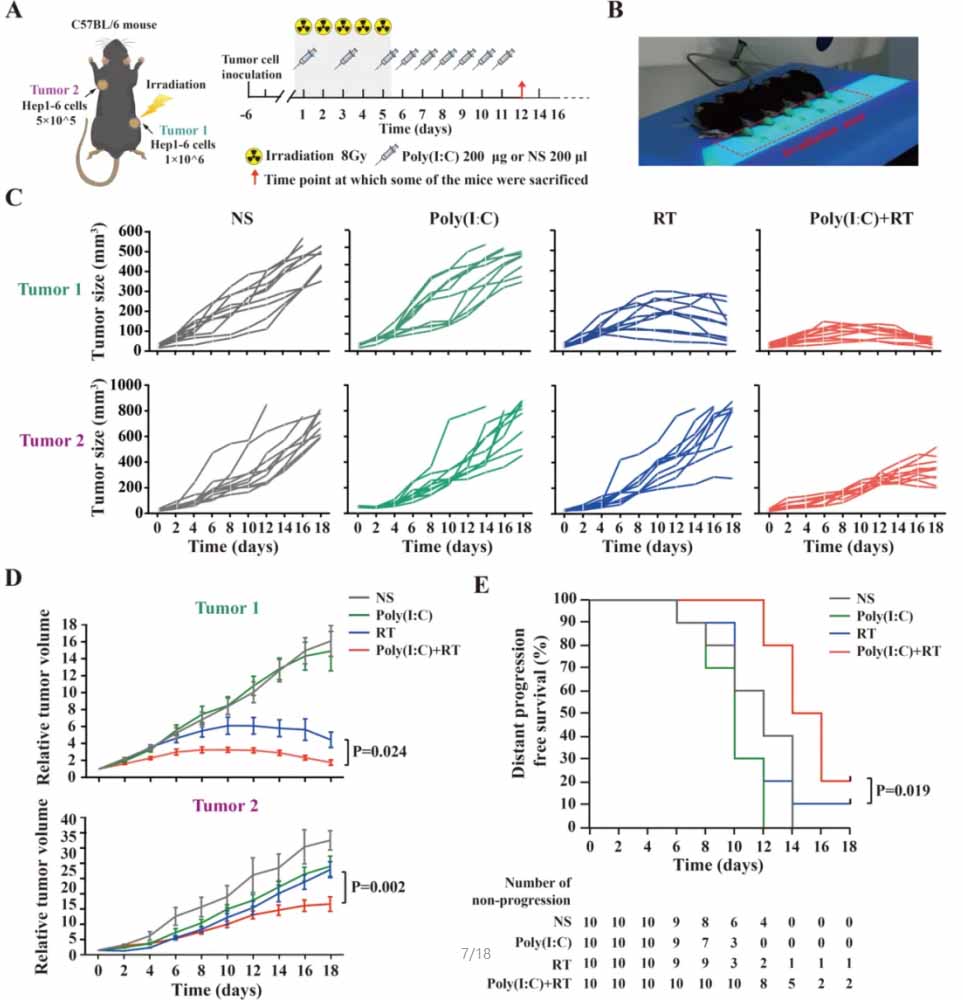
图1. 聚肌苷酸(Poly(I:C))增强放射疗法在肝细胞癌(HCC)小鼠模型中的远距效应。
(A)描述了小鼠皮下HCC肿瘤建模和治疗的流程。
(B)展示了如何将小鼠后肢的肿瘤固定在平板上并进行放射治疗。
(C)展示了直接接受放射治疗的肿瘤(Tumor1)和远距离的肿瘤(Tumor2)的生长曲线。
(D)使用方差分析(ANOVA)来分析不同治疗组之间的肿瘤体积差异。
研究证明聚肌苷酸可以增强放射疗法的远距效应,抑制了肝细胞癌的生长。这表明聚肌苷酸在放射治疗中具有潜在的协同作用,并可能成为一种新的治疗策略。
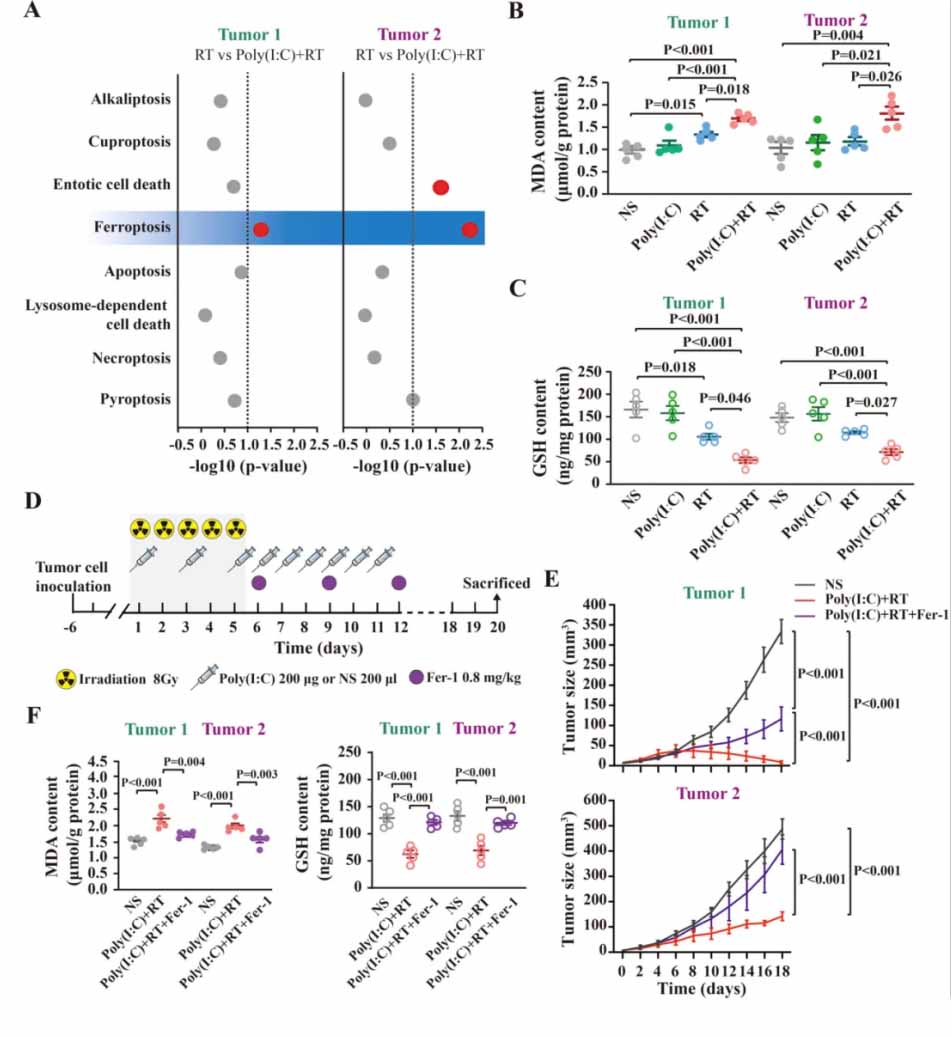
图2. 聚肌苷酸(Poly(I:C))促进放射治疗后肝癌小鼠的肿瘤铁死亡。
(A)使用t检验分析接受放射治疗和聚肌苷酸+放射治疗的肝癌小鼠Tumor1和Tumor2的RCD富集分数。
(B)和(C)描述了Tumor1和Tumor2在不同治疗组中的丙二醛(MDA)含量(氧化应激标志物)和谷胱甘肽(GSH)含量(抗氧化剂)的变化。
(D)描述了铁死亡抑制剂Fer-1在接受聚肌苷酸+放射治疗的肝癌小鼠模型中的治疗。
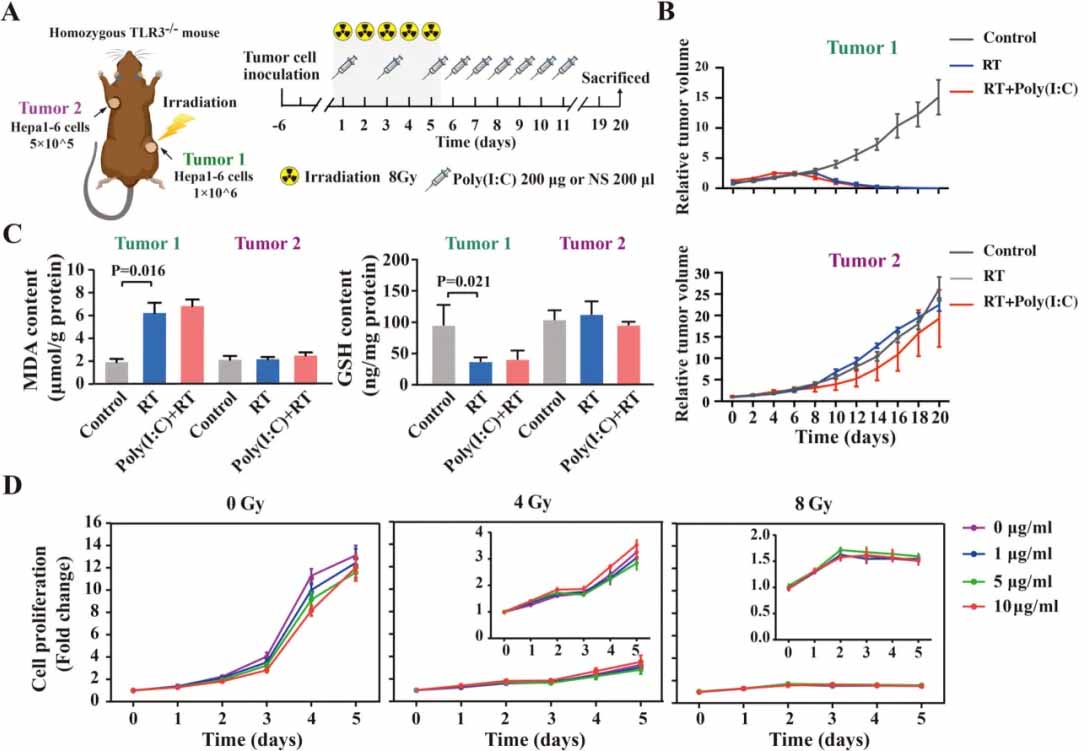
图3. 聚肌苷酸(Poly(I:C))增强放射疗法引起的远距效应依赖于TLR3信号。
(A)描述了TLR3基因敲除小鼠皮下HCC肿瘤建模和治疗的流程。
(B)和(C)展示了Tumor1在不同治疗组中的相对肿瘤体积,以及MDA和GSH含量的变化。
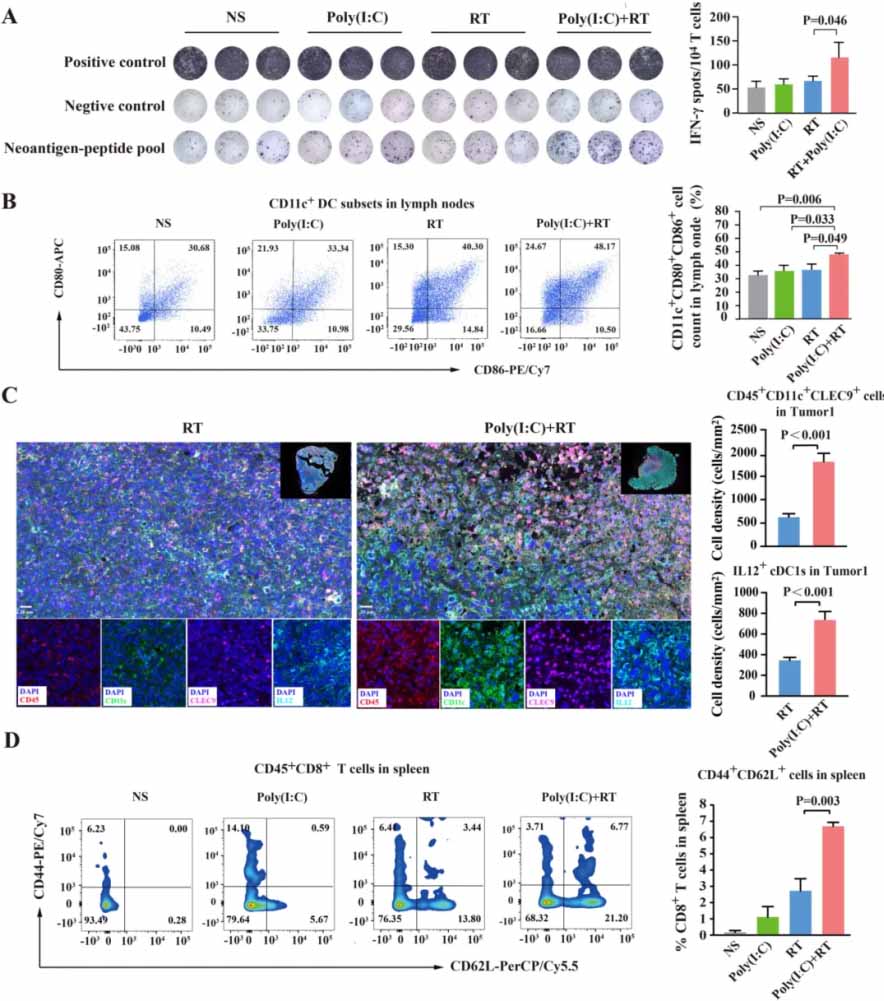
图4. 聚肌苷酸(Poly(I:C))促进DC摄取从放射治疗后的肿瘤组织释放的新抗原。
(A)ELISpot实验显示了新抗原肽池与HCC Hepa1-6细胞系中确定的7种突变新抗原之间的特异性反应。
(B)和(C)展示了不同治疗组中Tumor1中CD80+CD86+(激活抗原呈递细胞)和CD45+CD11c+CLEC9+(type 1树突状细胞)的比例和数量。
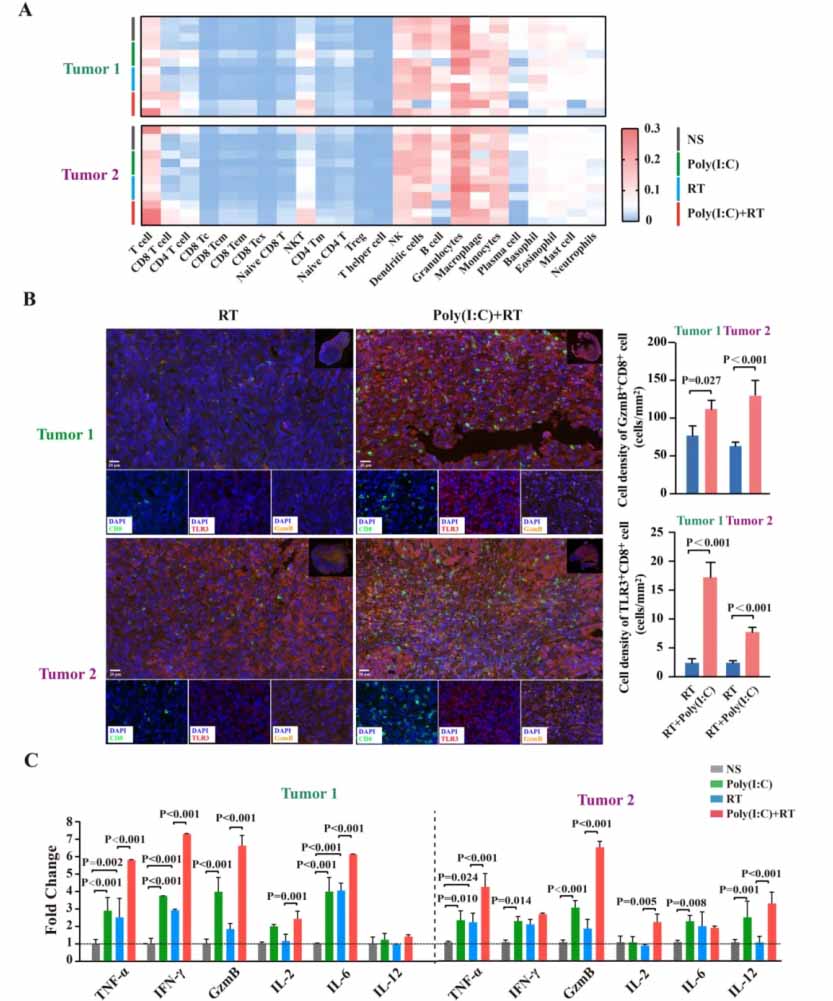
图5. 聚肌苷酸(Poly(I:C))促进放射治疗后肿瘤组织的T细胞浸润。
(A)根据RNA测序数据,分析了肿瘤组织中免疫细胞的浸润评分。
(B)和(C)展示了不同治疗组中TLR3+CD8+ T细胞和GzmB+CD8+ T细胞的数量。
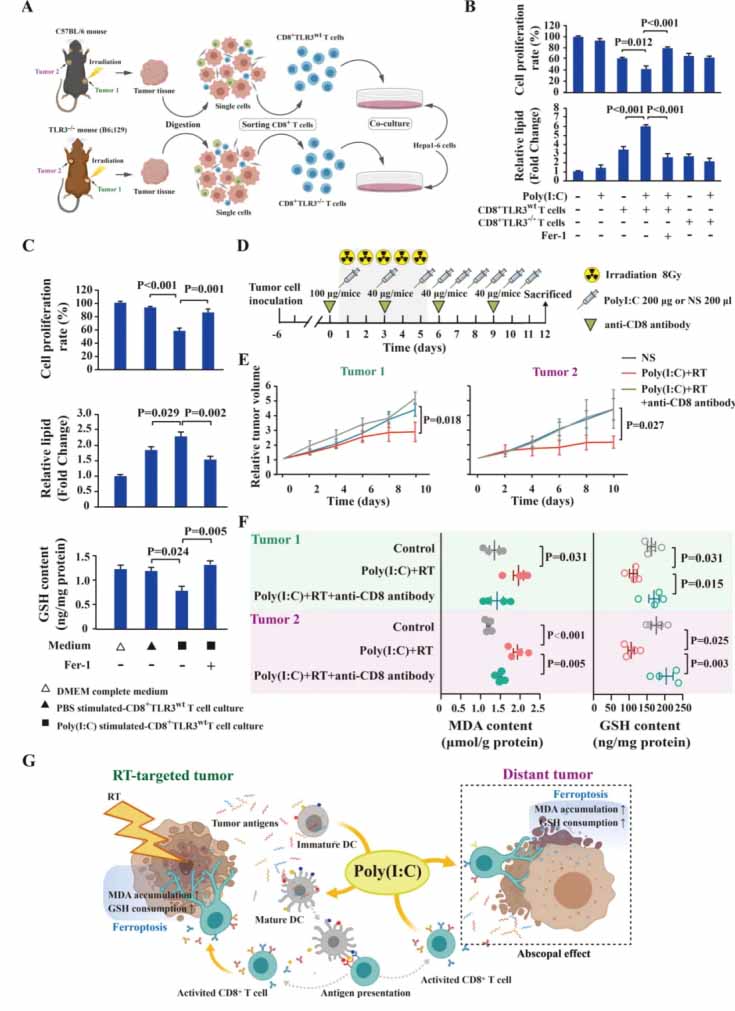
图6. 聚肌苷酸(Poly(I:C))增强放射治疗引起的肿瘤铁死亡效应依赖于组织浸润CD8+ T细胞的TLR3信号激活。
(A)描述了从双侧皮下HCC肿瘤模型中分离肿瘤浸润CD8+ T细胞并在Hepa1-6细胞上共培养的流程。
(B)和(C)展示了Hepa1-6细胞在不同干预下的细胞增殖率和相对脂质含量。

图7. 聚肌苷酸(Poly(I:C))改善放射疗法在 advanced HCC 患者中的远距效应。
(A)描述了 enrolled patients 的治疗时间表和临床事件的时间线。
(B)和(C)展示了两位患者的放射治疗方案和影像学结果。
(D)描述了根据RECIST1.1标准,入组患者和对照组患者在治疗前后的肿瘤直径长度变化。
图7展示了聚肌苷酸在人类晚期肝细胞癌患者中的应用。临床实验结果显示,聚肌苷酸联合放射疗法在患者中显著改善了远距效应,并导致肿瘤的显著缩小。这个结果对于临床治疗策略的制定和优化具有重要的指导价值。
本研究表明,在双侧HCC皮下肿瘤小鼠模型中,皮下给予toll样受体3 (TLR3)激动剂poly(I:C)可以通过激活肿瘤细胞铁下垂信号来增强RT期间的远端效应,而这一现象可被TLR3敲除或铁死亡抑制剂ferrostatin-1消除。此外,poly(I:C)可促进树突状细胞呈递肿瘤新抗原,促进活化的CD8+ T细胞向远处肿瘤组织募集,诱导肿瘤细胞铁死亡。
本研究表明,在放疗期间增强TLR3信号通路的激活可以为增强远端效应提供新策略,改善晚期HCC患者的临床效益。结合poly(I:C)与放疗的安全性和可行性在一项前瞻性临床试验中得到了验证。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:通过碳基纳米酶的双重催化增强肿瘤微环境敏化以提高光动力治疗效果
下一篇:具有抗氧化和抗黑色素生成活性的紫芝多糖在皮肤保健保护中的应用