常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-05-03 17:04:23 细胞资源库平台 访问量:23
脊髓损伤(SCI)尤其是完全横断损伤,因胶质瘢痕形成、轴突再生受阻及炎症微环境,临床修复难度极大 —— 现有干细胞移植或支架治疗难以同时满足 “模拟脊髓结构”“支持长期细胞存活”“引导神经再生” 三大需求。人脊髓类器官(HSCO)虽能模拟脊髓发育特征,但传统培养依赖 Matrigel,存在机械强度低、易坍塌、无法引导定向再生等问题。
基于此背景,来自香港城市大学生物医学工程系、香港中文大学、电子科技大学等机构的团队,在《Biomaterials》上发表题为“Generation of engineered human spinal cord organoid in channel-patterned collagen and transplantation for spinal cord regeneration”的研究,开发出基质胶填充的通道图案化 II 型胶原支架(CPCol II-M) ,将人运动神经祖细胞球状体诱导为 HSCO-CPCol II-M,该类器官不仅能长期存活并表达脊髓成熟神经元标志物,移植到裸鼠完全横断 SCI 模型后,还能显著促进运动功能恢复、减少胶质瘢痕、引导轴突再生并调节免疫微环境,为 SCI 修复提供新策略。
1.CPCol II-M 支架制备:先制备 II 型胶原支架,用手术打孔器制作贯穿通道(体外直径 3mm、体内 1.5mm),将支架浸泡于液态 Matrigel 中 4℃静置 24h 使其饱和,37℃孵育凝胶化,形成含通道的 II 型胶原 - Matrigel 复合支架。
2.HSCO-CPCol II-M 生成:hiPSC 来源的人运动神经祖细胞用 Accutase 消化,离心后接种于超低吸附 96 孔板形成球状体;将球状体转移至 CPCol II-M 通道中心,37℃聚合 30min 后,在摇床(60rpm)上用脊髓类器官培养基长期培养,形成 HSCO-CPCol II-M。
3.支架与类器官表征:用扫描电镜(SEM)观察支架微观形态,通过乙醇浸泡法测孔隙率,流变仪和 Instron 测试仪分别测储存模量和压缩模量;免疫荧光染色检测神经元(TUJ1、NeuN)、星形胶质细胞(GFAP)、运动神经元(ChAT、ISL1)等标志物;单细胞 RNA 测序和蛋白质组学分析类器官细胞组成与蛋白表达。
4.裸鼠 SCI 模型构建与移植:麻醉后暴露 T10 脊髓,完全横断后移植 HSCO-CPCol II-M(对照组为空白、Matrigel、CPCol II-M),术后每日人工排尿至自主排尿恢复;8 周后取材,通过 BMS 评分评估后肢运动功能,MRI 观察脊髓连续性,H&E 染色和免疫荧光检测组织修复情况。
5.安全性评估:取移植后小鼠心、肝、脾、肺、肾做 H&E 染色,检测器官病理变化;采集血液检测肝肾功能指标(如 ALT、AST、尿素、肌酐),评估全身毒性。
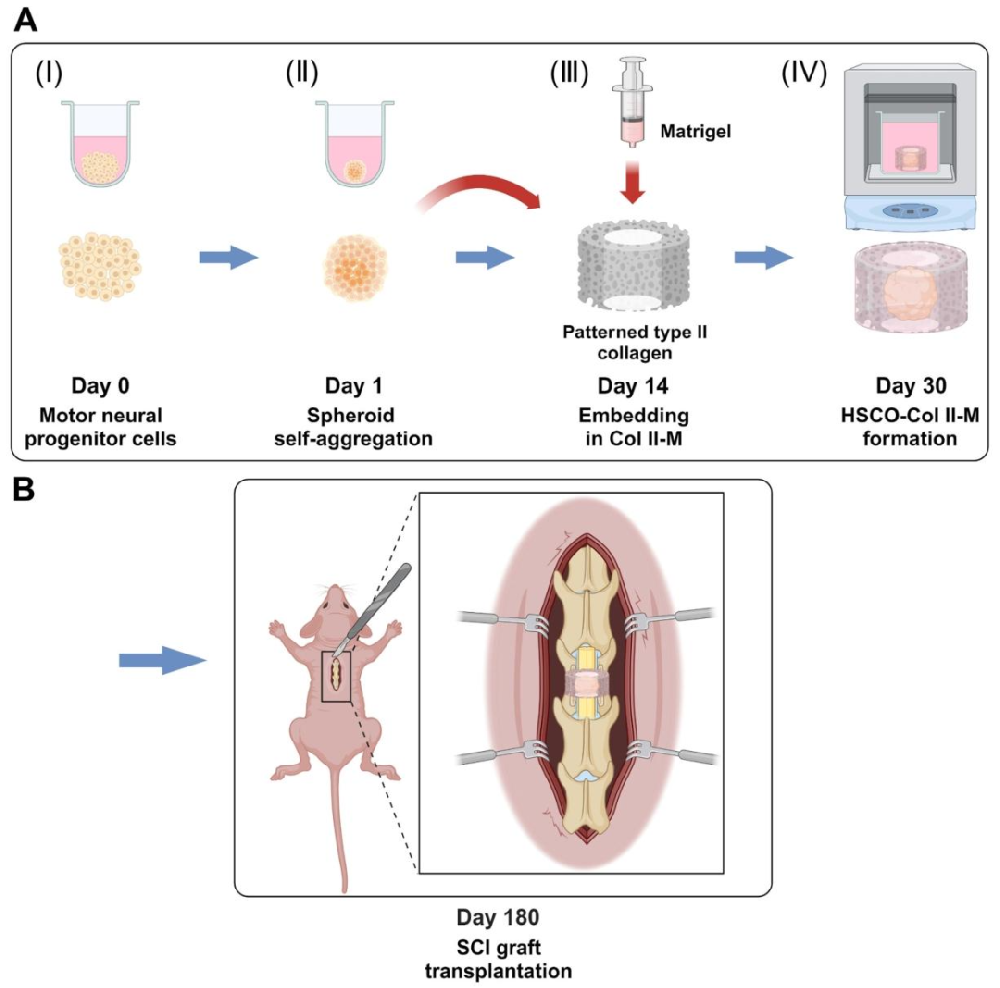
图1:HSCO-CPCol II-M 培养与 SCI 移植流程示意图
该图清晰呈现研究核心流程:A 部分展示类器官构建步骤 ——(I)培养人运动神经祖细胞,(II)祖细胞自聚集形成球状体,(III)将球状体嵌入 CPCol II-M 通道,(IV)培养 14-30 天形成成熟 HSCO-CPCol II-M,可长期培养至 180 天;B 部分为移植流程 —— 将 HSCO-CPCol II-M 移植到裸鼠完全横断 SCI 的损伤部位,通过支架通道引导神经再生。整个流程突出 “支架引导类器官定向分化” 与 “移植修复 SCI” 的逻辑链,为后续实验提供清晰框架。
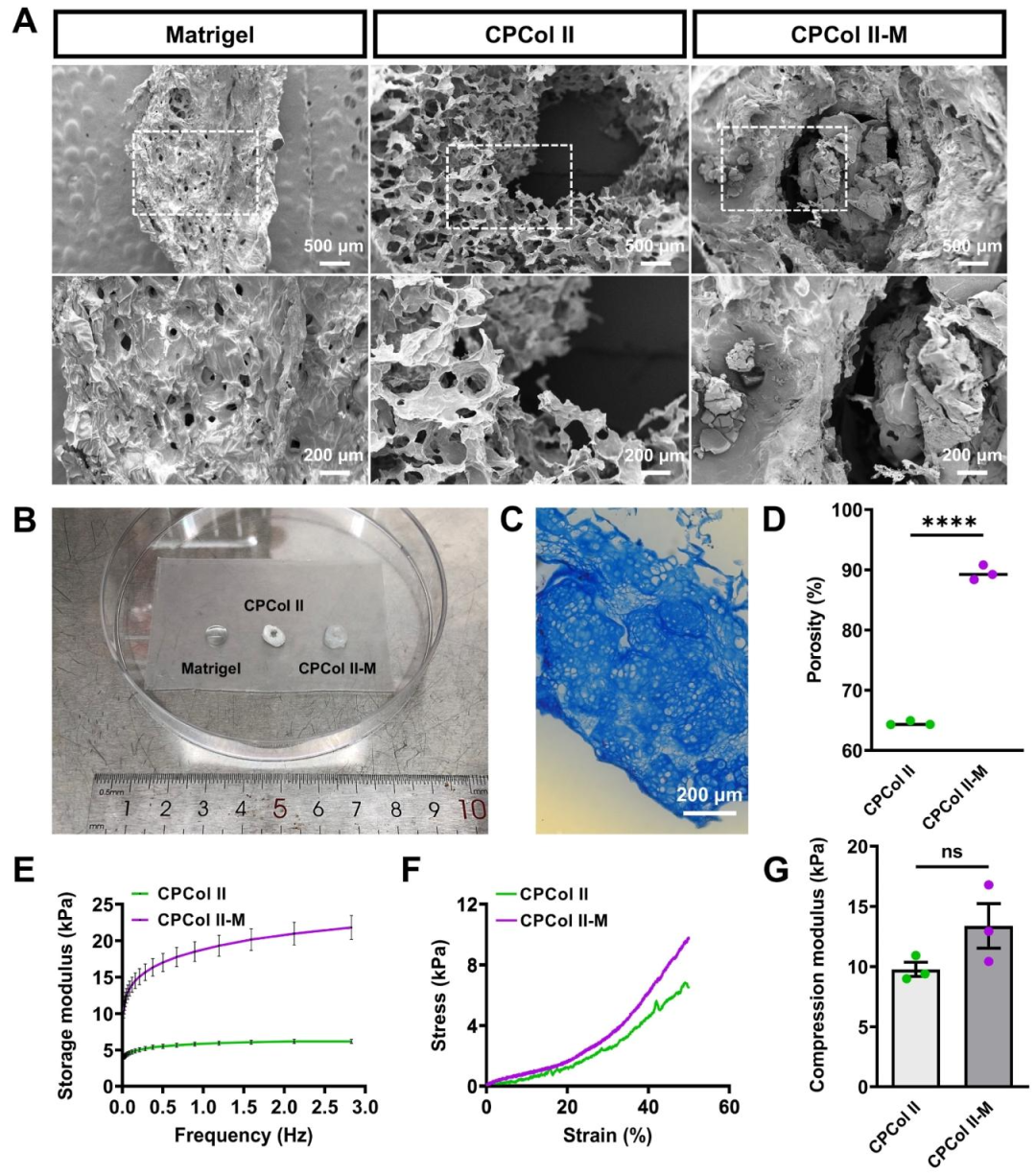
图2:CPCol II-M 支架的形态与力学特征
该图通过多维度验证支架性能:A 为 SEM 图像,显示 Matrigel 致密少孔,CPCol II 呈疏松网状结构,CPCol II-M 保留网状结构且通道内填充 Matrigel;B 为实物图,CPCol II 呈白色海绵状,CPCol II-M 因 Matrigel 填充呈半透明;C 为 Masson 染色,可见胶原纤维在支架中均匀分布;D-F 显示,CPCol II-M 孔隙率(89.47%)显著高于 CPCol II(64.51%),储存模量(10.33-21.81kPa)和压缩模量(13.38kPa)均优于 CPCol II,证实 Matrigel 与 II 型胶原结合后,既提升孔隙率利于营养交换,又增强力学强度满足移植需求。
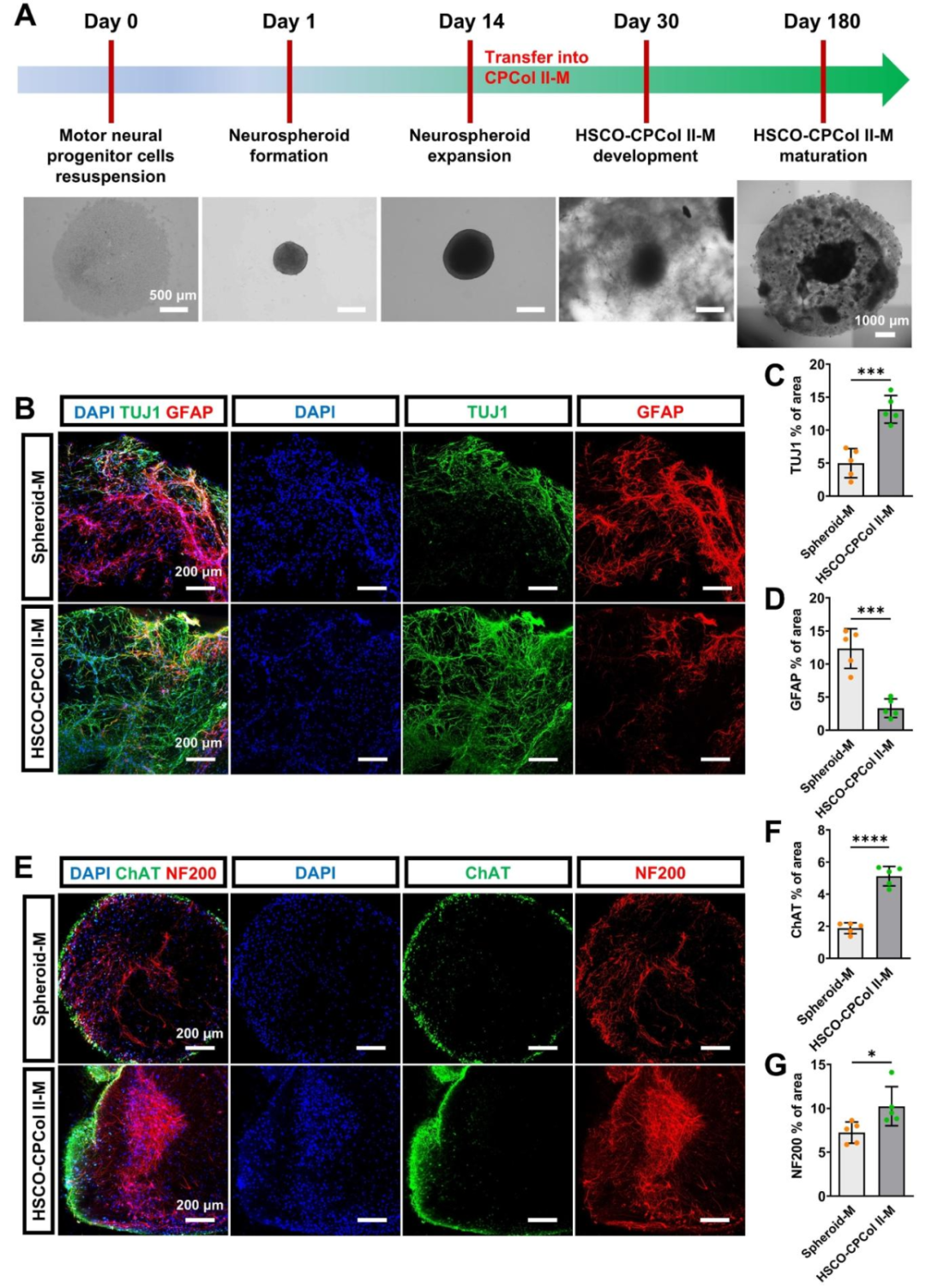
图3:HSCO-CPCol II-M 的生成与早期分化特征
该图追踪类器官从球状体到成熟的过程:A 为时间序列图,显示第 0 天祖细胞悬浮、第 1 天形成球状体、第 14 天嵌入支架后扩展、第 30-180 天形成成熟类器官;B-D 为第 30 天免疫荧光,HSCO-CPCol II-M 的神经元标志物 TUJ1 阳性面积(13.10%)显著高于 Matrigel 单独培养组(Spheroid-M,4.99%),星形胶质细胞标志物 GFAP 阳性面积(3.32%)显著低于 Spheroid-M(12.3%);E-G 为第 90 天染色,HSCO-CPCol II-M 的运动神经元标志物 ChAT(5.12%)和轴突标志物 NF200(10.20%)表达均显著高于 Spheroid-M,证实 CPCol II-M 支架更利于神经分化而非胶质细胞过度增殖。
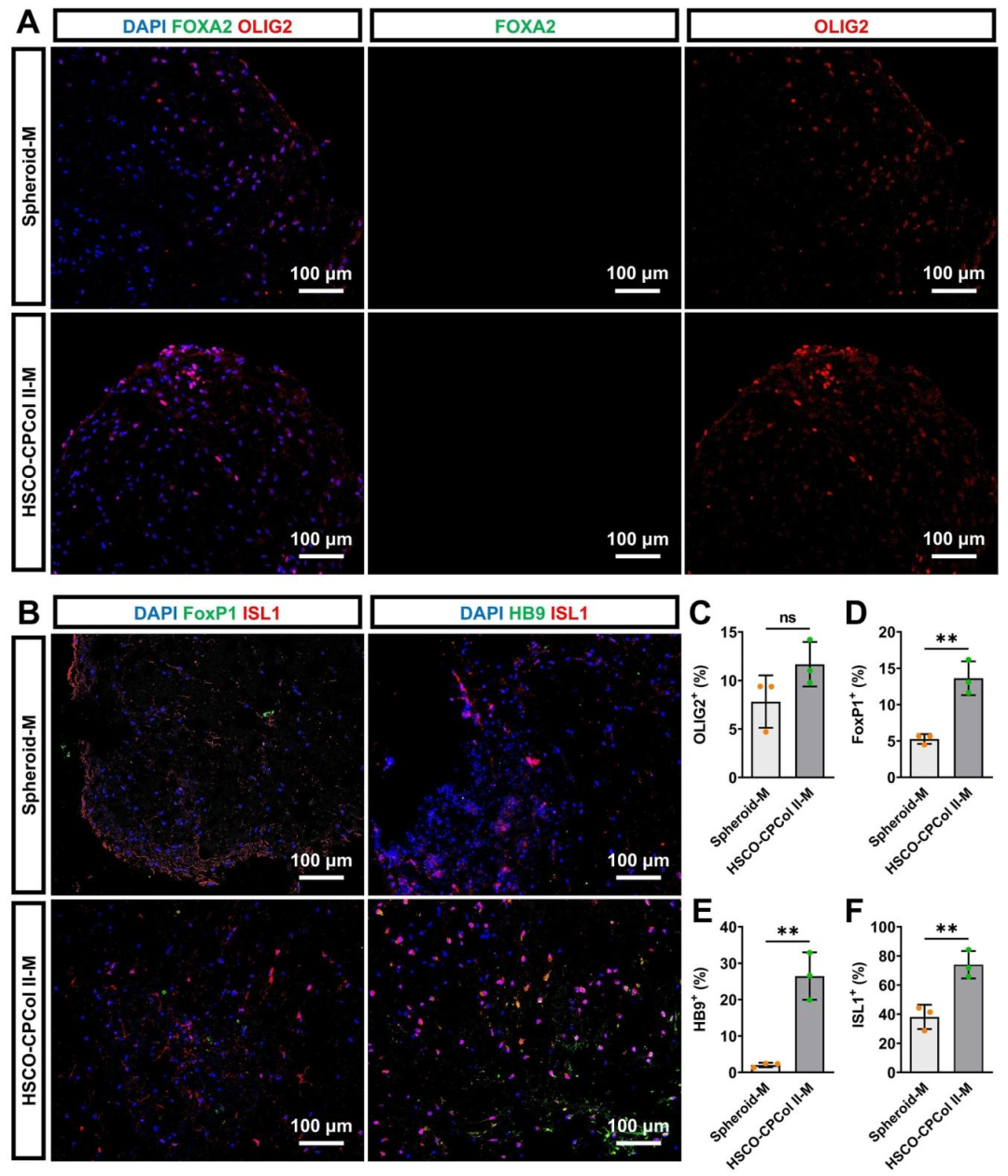
图4:HSCO-CPCol II-M 的脊髓运动神经元特征
该图验证类器官的脊髓特异性:A 为第 90 天染色,FOXA2(中脑 / 后脑标志物)在两组均不表达,OLIG2(腹侧祖细胞标志物)在两组均有表达(无显著差异),证明类器官定向分化为脊髓而非其他脑区;B-D 显示,HSCO-CPCol II-M 中 “ISL1+FoxP1+” 侧方运动神经元(支配肢体肌肉)比例显著高于 Spheroid-M;E-F 显示,“ISL1+HB9+” 腹外侧运动神经元(脊髓特有)比例在 HSCO-CPCol II-M 中达 26.50%(HB9+)和 74.00%(ISL1+),远高于 Spheroid-M 的 2.03% 和 38.10%,证实支架能诱导类器官形成脊髓特异性运动神经元。
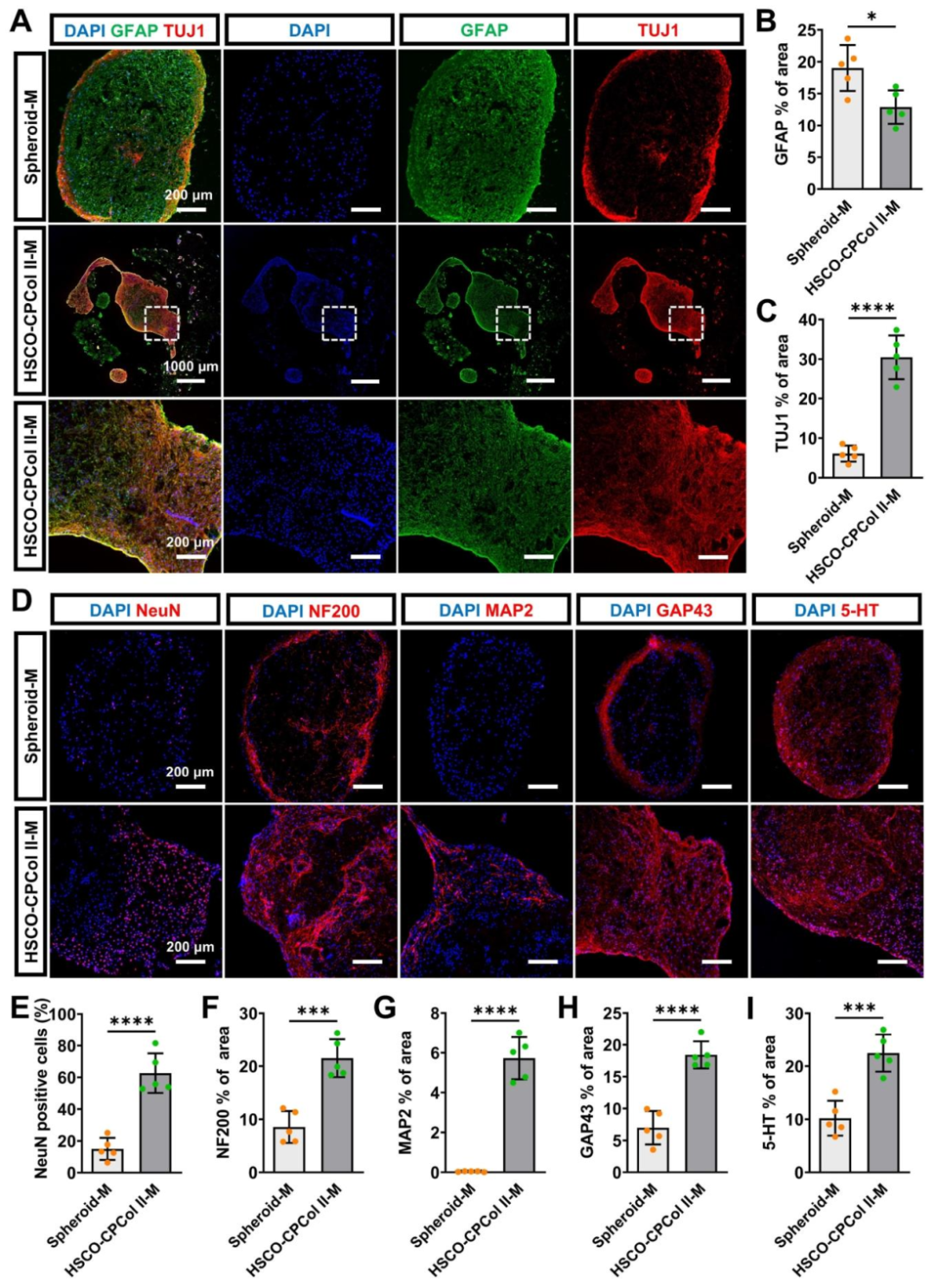
图5:HSCO-CPCol II-M 的长期成熟特征(第 180 天)
该图评估类器官长期培养后的成熟度:A-C 显示,HSCO-CPCol II-M 的 TUJ1 阳性面积(显著高于 Spheroid-M)和 GFAP 阳性面积(显著低于 Spheroid-M)的差异持续存在,说明支架支持长期神经分化;D-I 为成熟标志物染色,HSCO-CPCol II-M 的神经元核标志物 NeuN、轴突标志物 NF200、突触可塑性标志物 MAP2、轴突再生标志物 GAP43 及神经递质 5-HT 的表达均显著高于 Spheroid-M;同时 TUNEL 染色显示,Spheroid-M 核心存在大量凋亡,而 HSCO-CPCol II-M 凋亡显著减少,证实支架通道改善营养交换,减少细胞死亡。
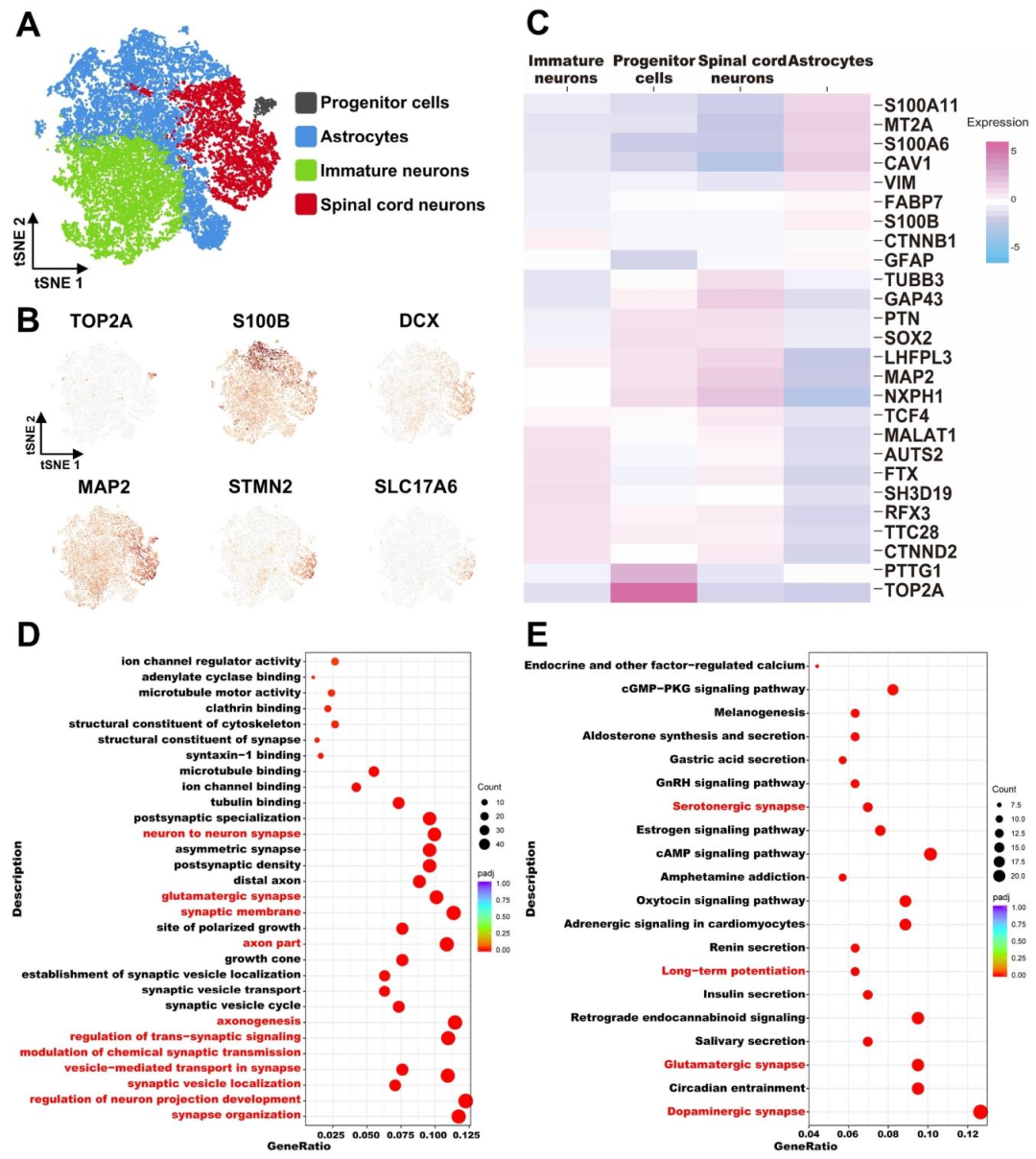
图6:HSCO-CPCol II-M 的单细胞 RNA 测序分析
该图解析类器官的细胞组成与功能:A 为 t-SNE 聚类,将 18452 个细胞分为祖细胞、星形胶质细胞、未成熟神经元、脊髓神经元 4 类;B 为标志物表达图,TOP2A(祖细胞)、S100B(星形胶质细胞)、DCX(神经母细胞)、MAP2(成熟神经元)、STMN2(脊髓神经元)在对应聚类中特异性表达;C 为热图,进一步验证各类细胞的特征基因差异;D-E 为 GO 和 KEGG 富集,脊髓神经元聚类显著富集 “轴突结构”“突触组织”“血清素能突触”“谷氨酸能突触” 等通路,从转录组层面证实类器官具备脊髓神经元的功能特征。
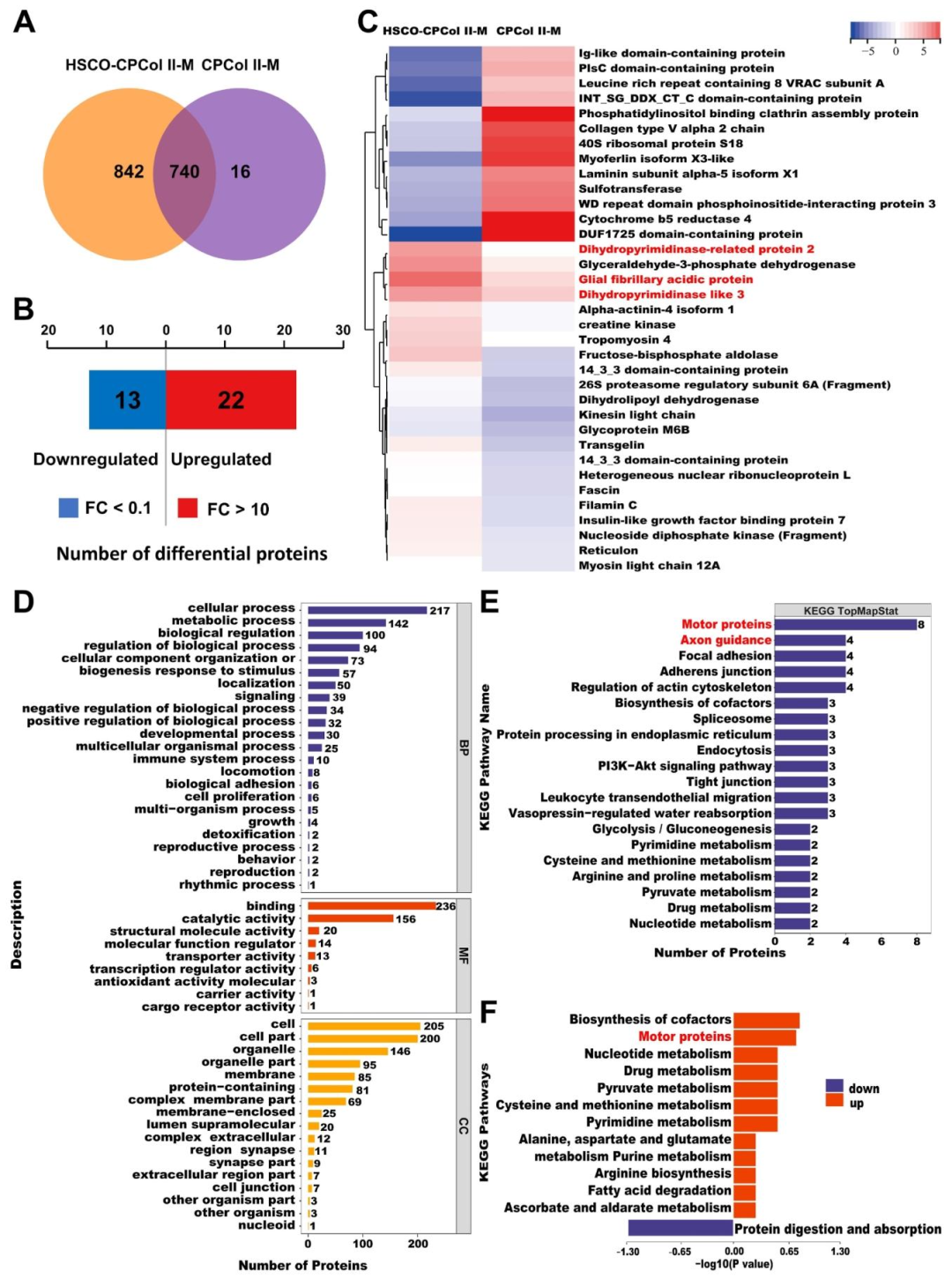
图7:HSCO-CPCol II-M 的蛋白质组学分析
该图从蛋白层面验证类器官成熟:A 为韦恩图,HSCO-CPCol II-M 与 CPCol II-M 共鉴定 740 个蛋白,HSCO-CPCol II-M 特有 842 个蛋白;B-C 显示,共筛选出 35 个差异蛋白(22 个上调、13 个下调),上调蛋白包括轴突生长相关的二氢嘧啶酶相关蛋白 2/3;D 为 GO 注释,差异蛋白主要参与 “细胞过程”“代谢过程”,分子功能以 “结合” 和 “催化活性” 为主,体现活跃的细胞功能;E-F 为 KEGG 富集,上调通路包括 “轴突导向”“运动蛋白相关通路”,下调通路为 “蛋白质消化吸收”,证实类器官在蛋白层面具备神经再生相关功能。
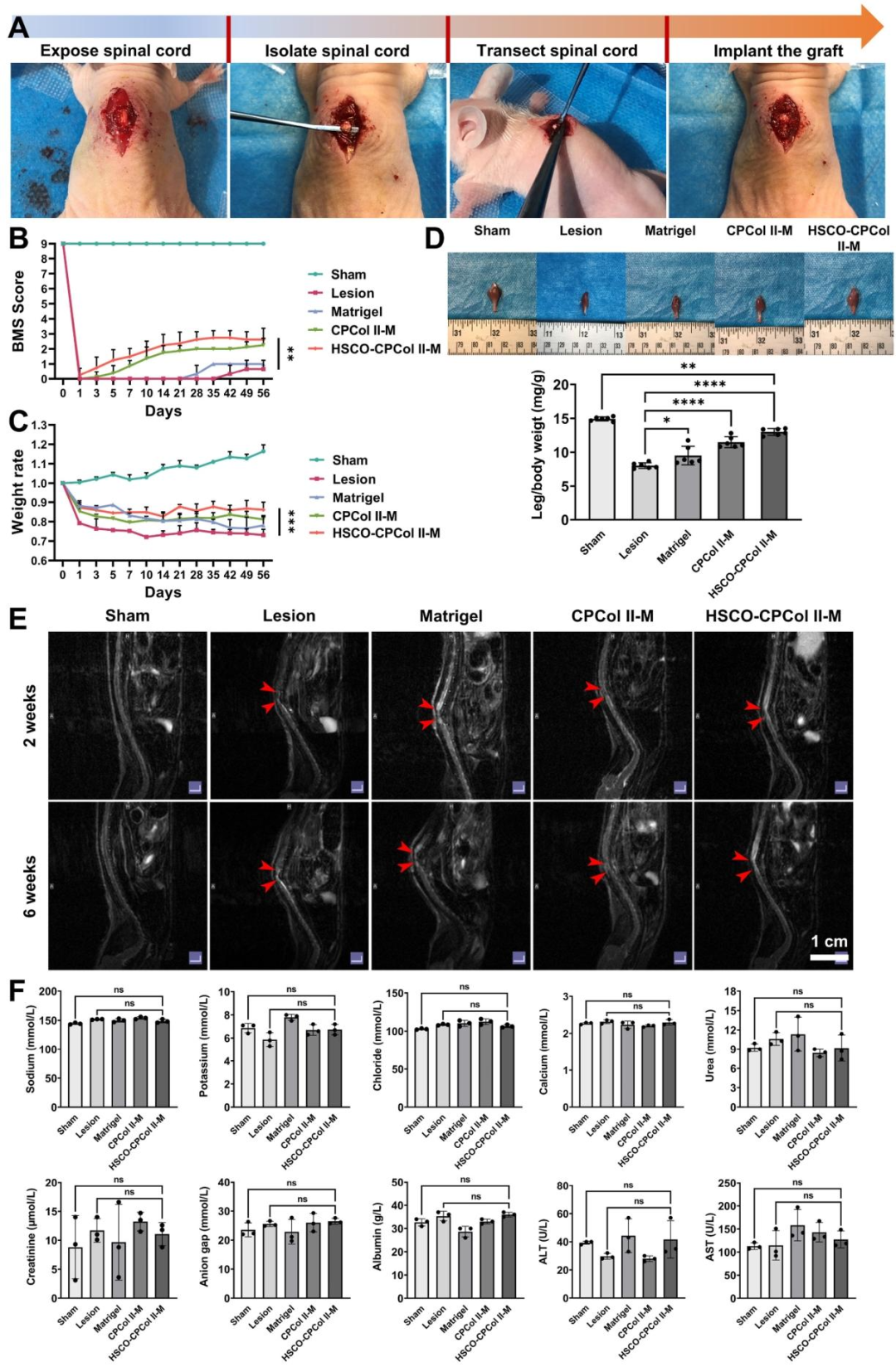
图8:HSCO-CPCol II-M 移植后的 SCI 功能恢复与安全性
该图评估移植后的体内效果:A 为手术流程,显示暴露、分离、横断脊髓并移植支架;B 为 BMS 评分,术后 56 天 HSCO-CPCol II-M 组评分显著高于损伤组,证明运动功能恢复;C 为体重变化,HSCO-CPCol II-M 组体重下降幅度小于损伤组,提示生存状态改善;D 为后肢肌肉重量比,HSCO-CPCol II-M 组(后肢重量 / 体重)显著高于损伤组,减少肌肉萎缩;E 为 MRI,损伤组和 Matrigel 组脊髓持续断裂,HSCO-CPCol II-M 组损伤部位信号连续,提示神经再生;F 为血液生化,各组肝肾功能指标无显著差异,H&E 染色显示心肝肾无病理异常,证实移植安全性。
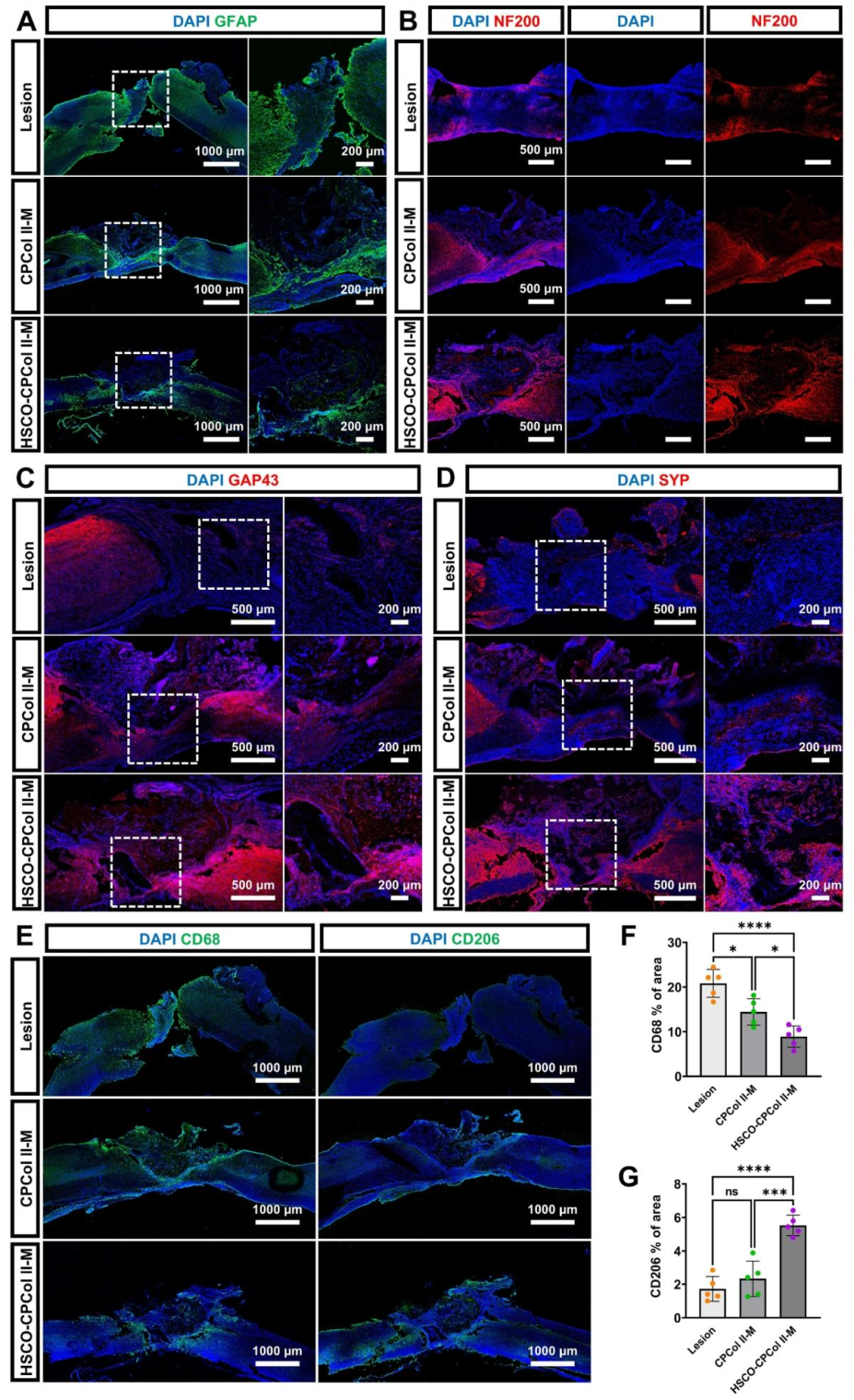
图9:HSCO-CPCol II-M 移植后的内源性修复机制
该图解析移植后的组织与免疫调节:A 为 GFAP 染色,损伤组形成致密胶质瘢痕,HSCO-CPCol II-M 组 GFAP 阳性细胞减少且沿支架通道纵向排列,为轴突再生提供通道;B-D 显示,HSCO-CPCol II-M 组的轴突标志物 NF200、再生标志物 GAP43 及突触标志物 SYP 在损伤区广泛分布,证实轴突再生与突触重建;E-G 为巨噬细胞染色,HSCO-CPCol II-M 组的总巨噬细胞标志物 CD68 阳性率(8.90%)显著低于损伤组(20.82%),抗炎 M2 巨噬细胞标志物 CD206 阳性率(5.53%)显著高于损伤组(1.72%),说明类器官可抑制过度炎症并促进抗炎微环境形成。
本研究开发了基质胶填充的通道图案化 II 型胶原支架(CPCol II-M),成功将人运动神经祖细胞诱导为具有脊髓特异性的 HSCO-CPCol II-M 类器官 —— 该支架通过 “高孔隙率 + 增强力学” 支持类器官长期存活(达 180 天),并定向诱导其分化为脊髓运动神经元(表达 ChAT、ISL1 等标志物),同时抑制星形胶质细胞过度增殖;移植到裸鼠完全横断 SCI 模型后,HSCO-CPCol II-M 能通过 “引导胶质细胞纵向排列减少瘢痕”“促进轴突再生与突触重建”“调节巨噬细胞向 M2 型极化减轻炎症” 三大机制,显著改善后肢运动功能、减少肌肉萎缩,且无全身毒性。该研究不仅解决了传统类器官培养的力学与定向分化问题,还为 SCI 的再生治疗提供了 “支架 - 类器官” 一体化的新方案,为后续临床转化奠定基础。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:突破 DCIS 类器官培养瓶颈:细针穿刺活检(FNAB)成高效新选择
下一篇:卵巢癌类器官模型精准反映铂类敏感性:PDO 与 PDXO 的一致性与临床价值