常见细胞污染类型如何辨别及预防解决方法
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
发布时间:2026-03-12 09:00:00 细胞资源库平台 访问量:130
史密斯 - 马吉尼斯综合征(SMS)由 17p11.2 染色体缺失导致 RAI1 基因单倍体不足引起,患者常伴自闭症(男女患病比例 1:3,与其他自闭症 4:1 相反)、皮质缺陷(皮质体积减小、轻度脑室扩张)及癫痫等症状。现有 SMS 小鼠模型虽能复现肥胖、社交障碍等表型,但皮质结构基本完整,无法模拟人类特有的皮质发育异常;且传统 2D 培养无法复现 3D 神经微环境,导致疾病机制研究受限。为此,研究团队利用人诱导多能干细胞(hiPSC)构建 2D 皮质神经元和 3D 皮质类器官模型,探究 17p11.2 缺失对染色质结构、转录调控、细胞发育及神经功能的影响,填补人类 SMS 神经病理建模的空白。
来自加拿大麦吉尔大学的团队在《The American Journal of Human Genetics》(2025 年,Vol. 112)发表题为Molecular and developmental deficits in Smith-Magenis syndrome human stem cell-derived cortical neural models的研究。
(1)研究方法
hiPSC 培养与分化:获取 4 株健康对照(Ctrl)和 4 株 SMS 患者来源 hiPSC(含 17p11.2 缺失),经多能性验证(核型分析、 pluripotency 标志物表达)后,用 STEMdiff 试剂盒分化为 2D 神经祖细胞(NPC)、皮质神经元及 3D 定向皮质类器官(培养至 75 天),其中类器官通过 AggreWell 系统构建,分形成期、扩张期、分化期培养。
分子与结构表征:采用 Hi-C 技术分析 hiPSC 和类器官的染色质 3D 拓扑结构(检测 TAD 融合、染色质互作变化);通过单细胞核 RNA-seq(snRNA-seq)和 bulk RNA-seq 解析细胞类型特异性转录组(聚焦神经精神疾病相关基因、细胞周期 / 代谢通路基因);免疫荧光检测 NPC(PAX6、SOX2)、神经元(NEUN、CAMKIIα)及突触标志物(VGLUT1、PSD95);流式细胞术结合 PI 染色分析 NPC 细胞周期。
功能与形态分析:EdU 脉冲追踪实验评估类器官 NPC 增殖与细胞周期退出;膜片钳技术记录神经元电生理(动作电位、钾 / 钠电流);慢病毒介导 myrGFP 标记神经元,Neurolucida 软件 3D 重建树突结构,Sholl 分析树突复杂度;TUNEL 和 γ-H2AX/p-53BP1 染色检测基因组稳定性。
(2)关键结果
染色质 3D 结构异常:17p11.2 缺失导致局部拓扑关联域(TAD)融合 ——Ctrl 的 17p11.2 区域含多个小 TAD,而 SMS 的该区域融合为单个大 TAD;同时引发全局染色质互作紊乱,SMS 类器官(75 天)的差异染色质接触数(1910 个减少、180 个增加)显著多于 SMS hiPSC(862 个减少、64 个增加),且差异 TAD 与 70%-77% 的非 17p11.2 差异表达基因(DEG)相关,提示染色质重构驱动转录失调。
转录组与细胞类型紊乱:snRNA-seq 显示 75 天 SMS 类器官含 16 种细胞类型(如循环放射状胶质细胞、外放射状胶质细胞、谷氨酸能神经元),其中循环放射状胶质细胞比例升高;DEG 富集神经精神疾病(自闭症、精神分裂症)签名,且细胞周期基因(如 CCNB1)上调、代谢 / 细胞器组装基因(如 HMGCS1)下调;scvelo 分析证实 SMS 谷氨酸能神经元成熟加速(潜伏时间更高,偏向成熟状态)。
类器官与 NPC 发育缺陷:SMS 类器官体积显著小于 Ctrl(75 天最大体积组直径减少 20%),且出现轻度脑室扩张 ——PAX6⁺脑室面积增加 150%,脑室数量增多但脑室周围 PAX6⁺细胞厚度减少;EdU 追踪显示 SMS NPC S 期细胞比例降低、细胞周期退出加速;2D NPC 出现 G1 期停滞,γ-H2AX/p-53BP1⁺细胞增多,提示基因组不稳定。
神经元形态与功能异常:SMS 神经元 4 周时胞体体积增大、树突总长增加(Sholl 分析 10-40μm 半径内分支更复杂),8 周时形态恢复正常;膜片钳记录显示 SMS 神经元自发动作电位比例升高(Ctrl vs SMS:30% vs 50%),动作电位阈值降低、半幅宽度变窄,且快速 / 慢速钾电流密度降低,钠电流正常,提示钾通道功能异常导致神经元过度兴奋。
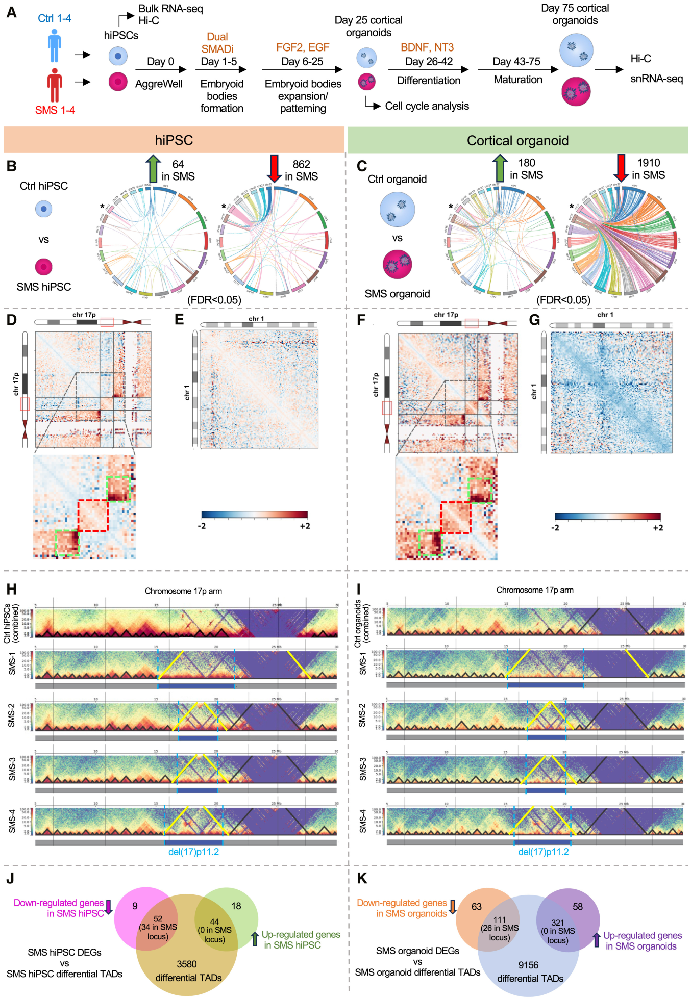
图 1:SMS 的染色质 3D 结构变化
该图展示 Hi-C 分析结果。(A)实验流程:Ctrl/SMS hiPSC 分化为 75 天皮质类器官,进行 Hi-C 和测序;(B-C)Circos 图:SMS hiPSC(B)和类器官(C)的基因组间 / 内染色质接触变化,红色线为接触增加,蓝色为减少,星号标注 17 号染色体,可见 17 号染色体相关接触紊乱最显著;(D-G)热图:SMS hiPSC(D)和类器官(F)的 17 号染色体染色质接触增加(红色),而 1 号染色体无明显变化(E、G),证实 17p11.2 缺失的局部效应;(H-I)TAD 分析:Ctrl 的 17p11.2 区域含多个小 TAD,SMS 则融合为单个大 TAD(黄色线);(J-K)Venn 图:差异 TAD 与 SMS hiPSC / 类器官的 DEG 显著重叠,提示染色质重构驱动基因失调。
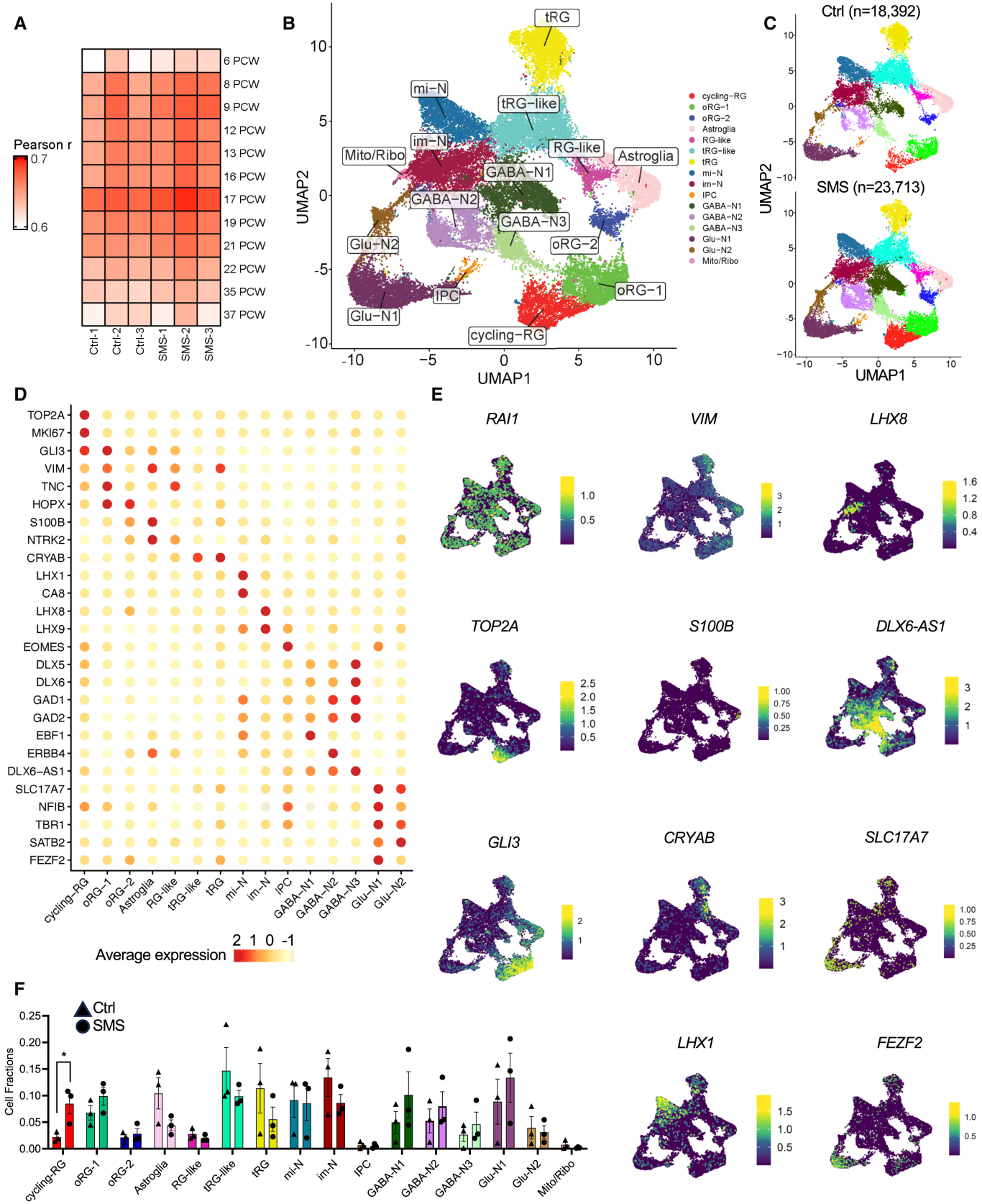
图 2:SMS 类器官的细胞类型与转录特征
该图为 snRNA-seq 结果。(A)发育年龄匹配:75 天类器官转录组与人类妊娠 17 周 neocortex 最相似;(B-C)UMAP 聚类:16 种细胞类型(如循环 RG、oRG、谷氨酸能神经元),SMS 与 Ctrl 细胞组成相似,但循环 RG 比例升高;(D-E)标志物表达:TOP2A/MKI67 标记循环 RG,SLC17A7 标记谷氨酸能神经元,RAI1 在 SMS 中全细胞类型表达降低;(F)细胞比例:SMS 循环 RG 比例显著高于 Ctrl,其他细胞类型无差异。
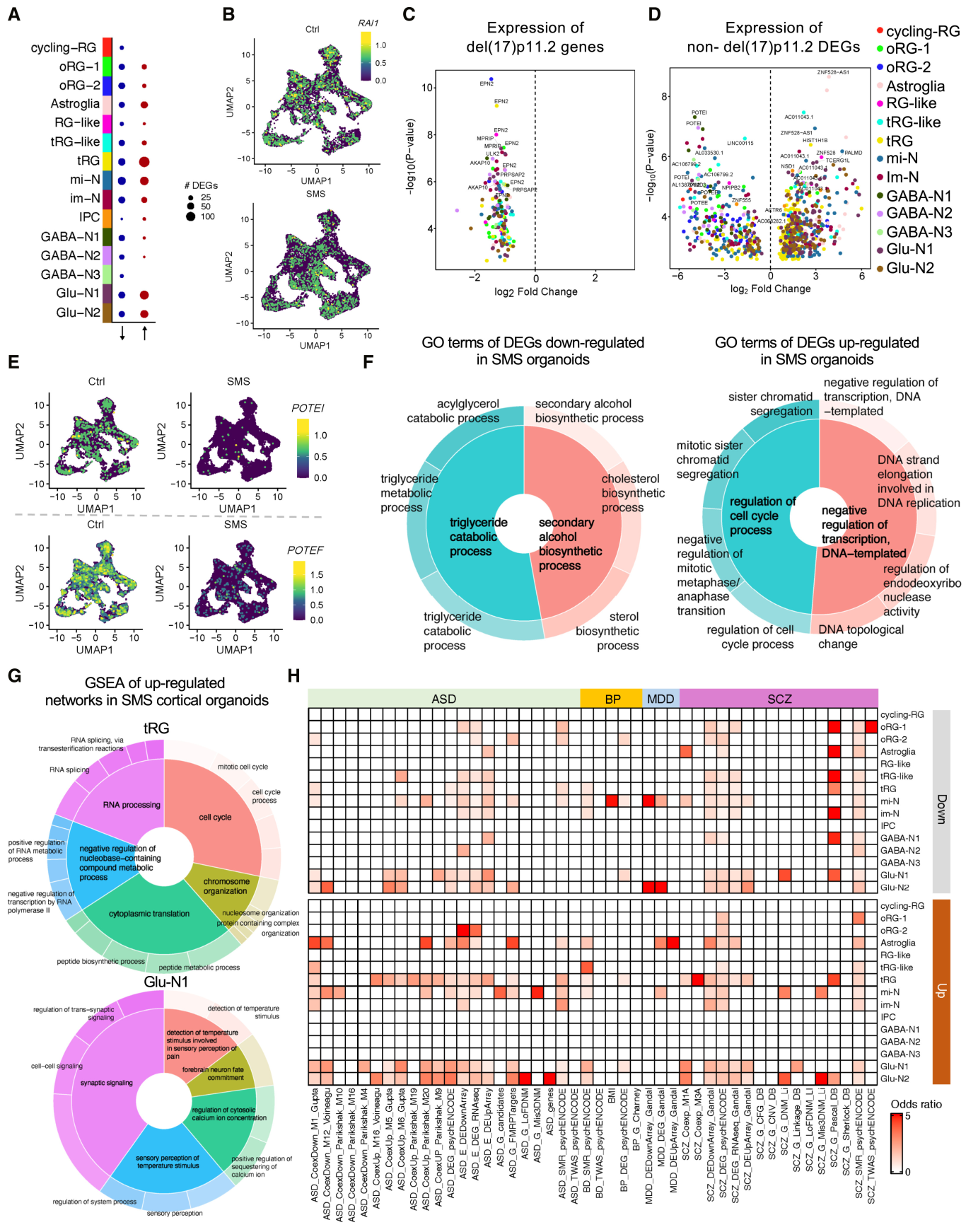
图 3:SMS 类器官的 DEG 与通路富集
该图分析 DEG 功能。(A-B)DEG 分布:SMS 各细胞类型均有 DEG,RAI1 等 17p11.2 基因全细胞类型下调;(C-D)火山图:非 17p11.2 基因在 SMS 中显著失调;(E)关键基因:灵长类特异性细胞黏附基因 POTEI/POTEF 在多细胞类型下调;(F-G)GO 富集:DEG 下调代谢通路(甘油三酯分解)、上调细胞周期 / 转录抑制通路;(H)疾病基因重叠:SMS DEG 与自闭症、精神分裂症相关基因显著富集,提示共同病理机制。
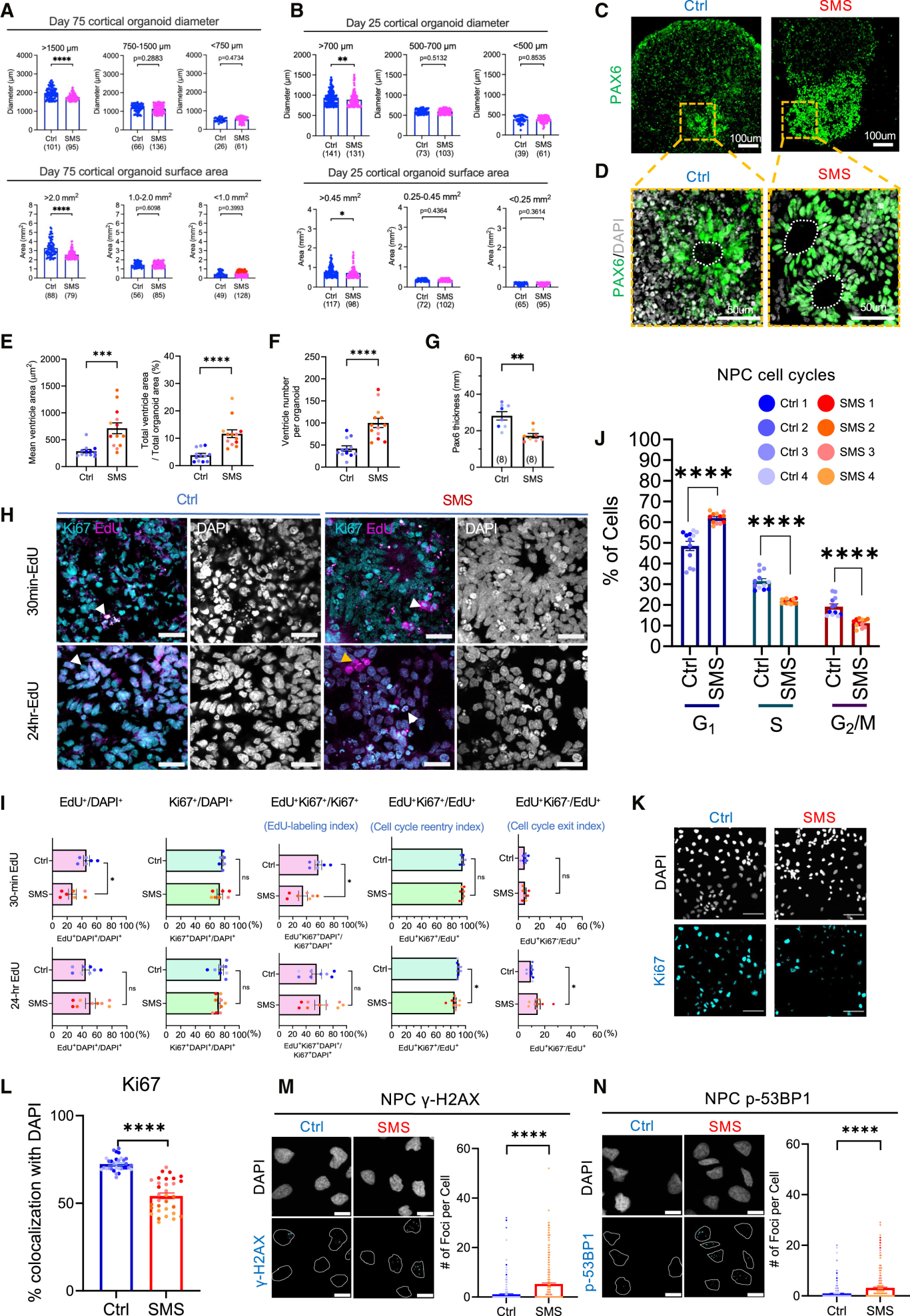
图 4:SMS 类器官的生长与细胞周期缺陷
该图展示类器官表型与 NPC 功能。(A-B)体积分析:75 天(A)和 25 天(B)SMS 类器官最大体积组显著小于 Ctrl;(C-G)脑室表型:SMS PAX6⁺脑室面积增加、数量增多、周围细胞厚度减少,模拟脑室扩张;(H-I)EdU 追踪:30 分钟脉冲显示 SMS EdU⁺细胞减少(S 期缺陷),24 小时脉冲显示细胞周期退出加速;(J-N)NPC 细胞周期:SMS NPC G1 期比例升高、S/G2/M 期降低,Ki67⁺细胞减少,γ-H2AX/p-53BP1⁺细胞增多,提示基因组不稳定。
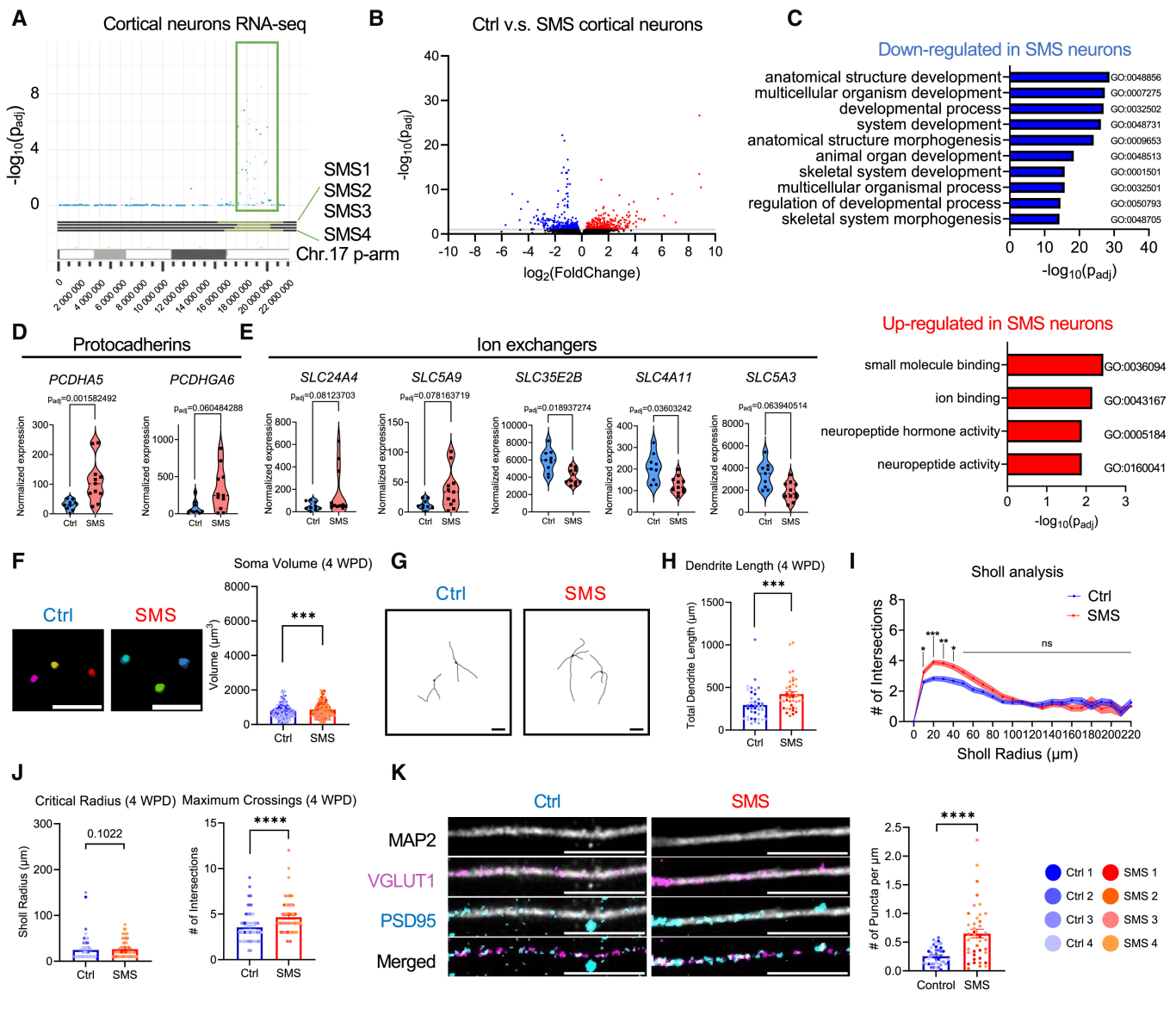
图 5:SMS 神经元的形态异常
该图为神经元形态分析。(A-B)转录组:17p11.2 基因在 SMS 神经元显著下调,非 17p11.2 基因(如 protocadherins、离子转运体)失调;(C)GO 富集:上调离子结合 / 神经肽活性,下调解剖结构发育;(D-E)关键基因:PCDHA5/PCDHGA6(细胞黏附)、SLC24A4(离子转运)在 SMS 中失调;(F-H)形态量化:4 周 SMS 神经元胞体体积增大、树突总长增加;(I-J)Sholl 分析:4 周 SMS 神经元 10-40μm 半径内分支更复杂,最大交叉数增多;(K)突触密度:SMS 神经元 VGLUT1⁺PSD95⁺突触密度高于 Ctrl。
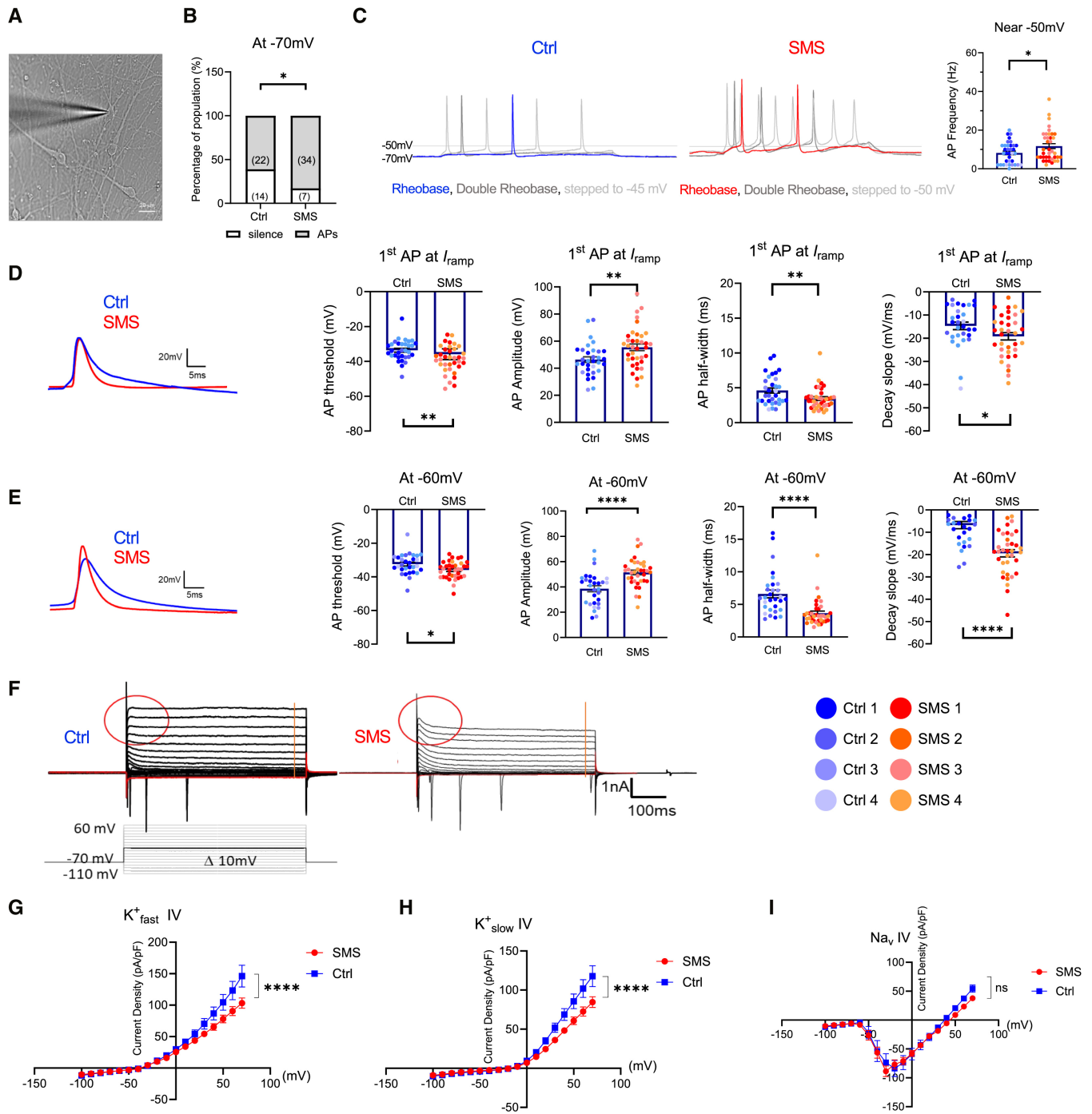
图 6:SMS 神经元的电生理异常
该图为膜片钳结果。(A)实验示意图:全细胞膜片钳记录皮质神经元;(B)自发动作电位:SMS 神经元自发 firing 比例显著高于 Ctrl;(C-E)动作电位特征:SMS 动作电位阈值降低、幅度增大、半幅宽度变窄,提示兴奋性升高;(F-I)离子电流:SMS 神经元快速 / 慢速钾电流(K⁺fast/K⁺slow)密度降低,钠电流(Naᵥ)无差异,证实钾通道功能异常导致过度兴奋。
本研究首次构建 SMS 的 hiPSC 衍生 2D/3D 神经模型,揭示 17p11.2 缺失的多层面致病机制:从染色质 3D 重构(局部 TAD 融合、全局互作紊乱),到转录组失调(神经精神疾病基因签名、细胞周期 / 代谢通路异常),再到细胞发育缺陷(类器官脑室扩张、NPC 增殖障碍)和神经功能异常(神经元过度兴奋),且模型复现 SMS 的核心临床表型(皮质体积减小、脑室扩张、癫痫倾向)。研究填补了人类 SMS 神经病理建模的空白,明确 “染色质 - 转录 - 细胞 - 功能” 的级联异常是疾病关键,为后续机制研究和药物筛选提供平台。局限性在于未涵盖 RAI1 单点突变型 SMS、样本以女性为主,未来需纳入男性样本并结合单细胞表观遗传分析,进一步解析 RAI1 的调控网络。
常见细胞污染类型如何辨别及预防解决方法:细胞培养中常见的生物污染类型有7种,分别是细菌污染,支原体污染,原虫污染,黑胶虫污染,真菌污染,病毒污染以及非细胞污染,真菌污染来源,一般是来自实验服,并且具有气候性,多雨······
细胞聚团的原因分析及如何避免:培养物中细胞可能聚集的一些原因包括:1.过度消化、2.环境压力、3.组织分解、4.过度生长、5.污染等;如何避免聚团细胞的生成;首先确认当前细胞生长密度及状态,80%左右的生长密度即可进行······
细胞有空泡原因分析及解决方法:出现细胞空泡情况有1.细胞老化2.培养液错误配制;3.细胞消化时操作不当;4.污染等等,如细胞老化,解决方法,原代细胞使用较低代次进行实验,传代细胞避免传代次数过高···
细胞半换液和全换液操作步骤:第一种方式:细胞全换液;如果是贴壁细胞,可以用全量换液法,直接吸去全部旧培养基,补充足量新鲜完全培养基;第二种方式:细胞半换液;"细胞半换液"又称"细胞半量换液",即弃掉一半旧的培养基,再······
细胞生长缓慢的可能原因有哪些:细胞培养外部因素包括细胞培养基的配方和质量问题,培养条件不理想,污染问题,细胞自身因素包含细胞的健康状态,细胞密度过高或过低,细胞老化现象,细胞特性,当细胞生长出现缓慢的问题时,我······
常用胰腺癌细胞株动物模型及胰腺癌细胞株有哪些:胰腺癌研究中常用的动物模型主要包括化学物质诱导胰腺癌动物模型,基因工程胰腺癌小鼠模型和胰腺癌移植模型,常用的胰腺细胞株MIA-PACA-2人胰腺癌细胞,Capan-2人胰腺癌细······
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
产品规格:1*10^6
¥3000
上一篇:低相干全息断层扫描结合机器学习实现小肠类器官无标记高分辨率 3D 成像与药物响应定量分析
下一篇:干细胞治疗阿尔茨海默病的机制、研究进展、临床挑战及技术整合综述